
【题目】已知充分燃烧ag乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量bkJ,则乙炔燃烧的热化学方程式正确的是( )
A.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH=-2bkJ·mol-1
B.C2H2(g)+![]() O2(g)=2CO2(g)+H2O(l) ΔH=+2bkJ·mol-1
O2(g)=2CO2(g)+H2O(l) ΔH=+2bkJ·mol-1
C.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH=-4bkJ·mol-1
D.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH=+bkJ·mol-1
科目:高中化学 来源: 题型:
【题目】500 mL AgNO3和Ca(NO3)2的混合溶液中c(NO![]() )=0.6 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是( )
)=0.6 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是( )
A.原混合溶液中c(Ca2+)为0.1 mol·L-1B.上述电解过程中共转移0.2 mol电子
C.电解得到的Ag的物质的量为0.1 molD.电解后溶液中c(H+)为0.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PNA是一种具有良好的热稳定性、耐腐蚀性和抗水性的高分子化合物,常用作增塑剂,其合成路线如下图所示:
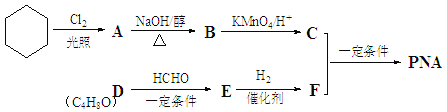
已知:
① R1CH=CHR2![]() R1COOH + R2COOH (R1、R2代表烃基)
R1COOH + R2COOH (R1、R2代表烃基)
②
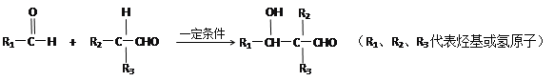
请回答:
(1)A分子中只有一个氯原子,A→B的化学方程式是 。
(2)C含有的官能团名称是 。
(3)D能发生银镜反应,且分子中有支链, D的结构简式是 。
(4)E→F的反应类型是 。
(5)E的结构简式是 。
(6)C与F在一定条件下生成增塑剂PNA的反应的化学方程式是: 。
(7)香豆素是一种重要的香料,与C具有相同的相对分子质量;14.6 g香豆素完全燃烧
生成39.6 g CO2和5.4 g H2O。
①香豆素的分子式是 。
②写出所有符合下列条件的香豆素的同分异构体的结构简式 。
a. 分子中含有![]() 基团
基团
b. 分子中除一个苯环外,无其他环状结构
c. 苯环上的氢原子被氯原子取代,得到两种一氯代物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸甲酯是一种重要的工业原料,有机化学中通过酯化反应原理,可以进行苯甲酸甲酯的合成。有关物质的物理性质、实验装置如下所示:
苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
熔点/℃ | 122.4 | ﹣97 | ﹣12.3 |
沸点/℃ | 249 | 64.3 | 199.6 |
密度/g.cm﹣3 | 1.2659 | 0.792 | 1.0888 |
水溶性 | 微溶 | 互溶 | 不溶 |
实验一:制取苯甲酸甲酯
在大试管中加入15g苯甲酸和一定量的甲醇,边振荡边缓慢加入一定量浓硫酸,按图A连接仪器并实验。

(1)苯甲酸与甲醇反应的化学方程式为______________________________________。
(2)中学实验室中制取乙酸乙酯时为了提高酯的产率可以采取的措施有___________________________
实验二:提纯苯甲酸甲酯
该实验要先利用图B装置把图A中制备的苯甲酸甲酯水洗提纯,再利用图C装置进行蒸馏提纯
(3)用图B装置进行水洗提纯时,B装置中固体Na2CO3作用是__________________。
(4)用图C装置进行蒸馏提纯时,当温度计显示____________时,可用锥形瓶收集苯甲酸甲酯。
(5)最终制取15g苯甲酸甲酯,计算得苯甲酸甲酯的产率为______________(小数点后保留1位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列说法不正确的是
A.等体积、等物质的量浓度的NaCl(aq) 离子总数大于NaClO(aq)中离子总数
B.pH=3的硫酸溶液中水的电离程度等于pH=11的氨水溶液中水的电离程度
C.0.1 mol/L的NaHA溶液pH=5,则溶液:c(HA-)>c(H+)>c(A2-)>c(H2A)
D.向NH4HSO4溶液中滴加NaOH溶液至中性,所得混合液:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,分别向容积固定的密闭容器中充入A和足量B,发生反应如下:2A(g)+B(s)![]() 2D(g)△H<0,测得相关数据如下,分析可知下列说法不正确的是
2D(g)△H<0,测得相关数据如下,分析可知下列说法不正确的是
实验Ⅰ | 实验Ⅱ | 实验Ⅲ | |
反应温度/℃ | 800 | 800 | 850 |
c(A)起始/mol·L-1 | 1 | 2 | 1 |
c(A)平衡/mol·L-1 | .0.5 | 1 | 0.85 |
放出的热量/kJ | a | b | c |
A.实验III的化学平衡常数K<1
B.实验放出的热量关系为b>2a
C.实验III在30min达到平衡时的速率v(A)为0.005mol L-1·min-1
D.当容器内气体密度不随时间而变化时上述反应达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“84”消毒液(工业利用Cl2与NaOH反应制得)可用于消毒和漂白,下列实验现象的分析不正确的是
实验操作 |
|
|
|
实验现象 | 混合后溶液的pH=9.9,短时间内未褪色,一段时间后蓝色褪去。 | 混合后溶液pH=5.0,蓝色迅速褪去,无气体产生。 | 混合后溶液pH=3.2,蓝色迅速褪去,并产生大量气体,使湿润的淀粉碘化钾试纸变蓝。 |
A.对比实验①和②,②中蓝色迅速褪去的原因是发生了反应ClO+H+═HClO
B.实验③中产生的气体是Cl2,由HClO分解得到:2HClO═Cl2↑+H2O
C.对比实验②和③,溶液的pH可能会影响ClO的氧化性或Cl的还原性
D.加酸可以提高“84”消毒液的漂白效果,但需要调控合适的pH才能安全使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质间反应的产物中一定不存在同分异构体的是
A. CH3-CH=CH2与HBr B. ![]() 与NaOH乙醇溶液共热
与NaOH乙醇溶液共热
C. CH3CH3与Cl2 D.  与NaHCO3溶液
与NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能量是一个世界性的话题,如何充分利用能量、开发新能源,为人类服务是广大科技工作者不懈努力的目标。
(1)如图所示,组成一个原电池:
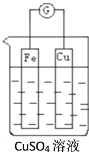
Cu电极是___(填“正”或“负”)极,其电极反应式为___;电子由___极流出。
(2)利用(1)图中的电极和电解液,在增加电源后可以实现电能转化为化学能,Fe接入电源负极,Cu接入电源正极,电解过程电极质量增加的是___(填“Fe”或“Cu”),Fe的腐蚀速度比正常在空气中的腐蚀速度___(填“快”或“慢”),溶液中c(Cu2+)___(填“增大”、“减小”或“不变”)。
(3)利用氢气与氧气的燃烧反应2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ·mol-1,作为燃料电池的反应原理,可以提高能量的利用率,填充H2的电极是____(填“正”或“负”)极;当有11.2L(折算成标准状况下的体积)H2反应,会放出___kJ热量;如果2H2(g)+O2(g)=2H2O(g) ΔH=-a kJ·mol-1,则a___571.6(填“>”、“<”或“=”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com