


 ,A与氯气光照生成B,B在氢氧化钠水溶液、加热条件下水解生成C,故A为
,A与氯气光照生成B,B在氢氧化钠水溶液、加热条件下水解生成C,故A为 ,B为
,B为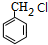 ,
, 与
与 反应取代反应生成E,结合反应信息可知,E为
反应取代反应生成E,结合反应信息可知,E为 ,据此解答.
,据此解答. ,A与氯气光照生成B,B在氢氧化钠水溶液、加热条件下水解生成C,故A为
,A与氯气光照生成B,B在氢氧化钠水溶液、加热条件下水解生成C,故A为 ,B为
,B为 ,
, 与
与 反应生成E,结合反应信息可知,E为
反应生成E,结合反应信息可知,E为 ,
, ,故答案为:
,故答案为: ;
; ,含有官能团为:氯原子,反应④是
,含有官能团为:氯原子,反应④是 与
与 反应取代反应生成
反应取代反应生成 ,
,
 ;
; 含有氧原子,不属于卤代烃,含有苯环,属于芳香族化合物,含有酯基、氯原子,能发生取代反应、能与氢氧化钠溶液反应,分子中含有-CH2-,具有甲烷的四面体结构,所有原子不可能在同一平面上,故BCD正确、AE错误;
含有氧原子,不属于卤代烃,含有苯环,属于芳香族化合物,含有酯基、氯原子,能发生取代反应、能与氢氧化钠溶液反应,分子中含有-CH2-,具有甲烷的四面体结构,所有原子不可能在同一平面上,故BCD正确、AE错误; 在水溶液中很不稳定,易发生水解反应,由反应信息可知,水解生成苯甲醇、二氧化碳、HCl,反应方程式为:
在水溶液中很不稳定,易发生水解反应,由反应信息可知,水解生成苯甲醇、二氧化碳、HCl,反应方程式为: +H2O→
+H2O→ +CO2↑+HCl,
+CO2↑+HCl, +H2O→
+H2O→ +CO2↑+HCl;
+CO2↑+HCl;

科目:高中化学 来源: 题型:
| A、稀盐酸与氢氧化镁反应:H++OH-=H2O |
| B、铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| C、铜与硝酸银溶液反应:Cu+Ag+=Cu2++Ag |
| D、碳酸氢钠溶液与盐酸反应:HCO3-+H+=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用盐酸清洗盛石灰水的试剂瓶内壁的白色固体:CO32-+2H+═CO2↑+H2O |
| B、用酸性KMnO4溶液判断FeCl2是否完全变质:5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O |
| C、用NaOH溶液除去乙酸乙酯中的少量乙酸:CH3COOH+OH-═CH3COO-+H2O |
| D、在Mg(0H)2悬浊液中滴几滴饱和FeCl3溶液证明Fe(0H)3溶解度小于Mg(OH)2:3Mg(OH)2+2Fe3+═3Mg2++2Fe(0H)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:丁>丙>乙>甲 |
| B、1mol A与足量B完全反应共转移了2mol电子 |
| C、丙元素在周期表中的位置为第二周期第ⅣA族 |
| D、A中既有离子键又有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某有机物A,分子中含两个碳原子,现用A来制取有芳香气味的有机物F和加聚高分子化合物E,其变化如下图所示:
某有机物A,分子中含两个碳原子,现用A来制取有芳香气味的有机物F和加聚高分子化合物E,其变化如下图所示:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com