
ЁОЬтФПЁПЖЁЯуШЉЃЈCH3ЁЊ![]() ЁЊCH2ЁЊCHO ЃЉЪЧГЃгУЕФвЛжжЪГгУЯуОЋЃЌвбжЊBжаКЌгавЛИіТШдзгЃЌИїЮяжЪжЎМфДцдкЯТСазЊЛЏЙиЯЕЃК
ЁЊCH2ЁЊCHO ЃЉЪЧГЃгУЕФвЛжжЪГгУЯуОЋЃЌвбжЊBжаКЌгавЛИіТШдзгЃЌИїЮяжЪжЎМфДцдкЯТСазЊЛЏЙиЯЕЃК
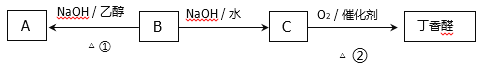
ЃЈ1ЃЉBЕФЗжзгЪНЮЊ________ЃЌCжаКЌбѕЙйФмЭХЕФУћГЦЮЊ________ЁЃ
ЃЈ2ЃЉЗДгІЂкЕФЛЏбЇЗНГЬЪНЮЊ____________________________________ЁЃ
ЃЈ3ЃЉAЗЂЩњМгОлЗДгІЫљЕУВњЮяЕФНсЙЙМђЪНЮЊ________________ЁЃ
ЃЈ4ЃЉгыAКЌгаЯрЭЌЙйФмЭХЕФЗМЯузхЛЏКЯЮяЕФЭЌЗжвьЙЙЬхЛЙга________жжЃЈВЛПМТЧЫГЗДвьЙЙЃЉЃЌЦфжажЛгавЛИіШЁДњЛљЧвВЛКЌМзЛљЕФЮяжЪЕФНсЙЙМђЪНЮЊ____________________ЁЃ
ЁОД№АИЁПC9H11Cl ДМєЧЛљЛђєЧЛљ 2![]() +O2
+O2![]() 2 CH3ЁЊ
2 CH3ЁЊ![]() ЁЊCH2ЁЊCHO+2H2O
ЁЊCH2ЁЊCHO+2H2O 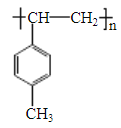 5
5 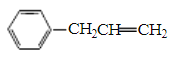
ЁОНтЮіЁП
CДпЛЏбѕЛЏЩњГЩЖЁЯуШЉЃЌдђCжаКЌгаДМєЧЛљЃЌНсЙЙМђЪНЮЊ![]() ЃЛBжаКЌгавЛИіТШдзгЃЌЗЂЩњШЁДњЗДгІЪБЩњГЩ
ЃЛBжаКЌгавЛИіТШдзгЃЌЗЂЩњШЁДњЗДгІЪБЩњГЩ![]() ЃЌдђBЕФНсЙЙМђЪНЮЊ
ЃЌдђBЕФНсЙЙМђЪНЮЊ![]() ЃЛ
ЃЛ![]() дкNaOH/ДМШмвКжаЃЌМгШШЪБЗЂЩњЯћШЅЗДгІЃЌЩњГЩКЌгаЬМЬМЫЋМќЕФгаЛњЮяКЭТШЛЏФЦЃЌдђAЕФНсЙЙМђЪНЮЊ
дкNaOH/ДМШмвКжаЃЌМгШШЪБЗЂЩњЯћШЅЗДгІЃЌЩњГЩКЌгаЬМЬМЫЋМќЕФгаЛњЮяКЭТШЛЏФЦЃЌдђAЕФНсЙЙМђЪНЮЊ![]() ЁЃ
ЁЃ
ЃЈ1ЃЉЗжЮіПЩжЊЃЌBЮЊ![]() ЃЌдђЗжзгЪНЮЊC9H11ClЃЛCЮЊ
ЃЌдђЗжзгЪНЮЊC9H11ClЃЛCЮЊ![]() ЃЌКЌгаЕФКЌбѕЙйФмЭХЮЊДМєЧЛљЃЛ
ЃЌКЌгаЕФКЌбѕЙйФмЭХЮЊДМєЧЛљЃЛ
ЃЈ2ЃЉЗДгІЂкЮЊДМЕФДпЛЏбѕЛЏЃЌЗДгІЬѕМўЮЊAg/CuзїДпЛЏМСЃЌМгШШЕФЬѕМўЯТНјааЃЌЗНГЬЪНЮЊ2![]() +O2
+O2![]() 2 CH3ЁЊ
2 CH3ЁЊ![]() ЁЊCH2ЁЊCHO+2H2OЃЛ
ЁЊCH2ЁЊCHO+2H2OЃЛ
ЃЈ3ЃЉAЮЊ![]() ЃЌКЌгаЬМЬМЫЋМќЃЌФмЗЂЩњМгОлЗДгІЃЌЩњГЩЮяЮЊ
ЃЌКЌгаЬМЬМЫЋМќЃЌФмЗЂЩњМгОлЗДгІЃЌЩњГЩЮяЮЊ![]() ЃЛ
ЃЛ
ЃЈ4ЃЉгыAКЌгаЯрЭЌЙйФмЭХЕФЗМЯузхЛЏКЯЮяжаЃЌМзЛљПЩдкБНЛЗЩЯгыввЯЉЛљСкЮЛЁЂМфЮЛЃЛЛЙПЩвд![]() ЁЂ
ЁЂ![]() ЁЂ
ЁЂ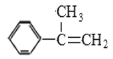 ЃЌЙВМЦ5жжЃЛжЛгавЛИіШЁДњЛљЧвВЛКЌгаМзЛљЕФЮЊ
ЃЌЙВМЦ5жжЃЛжЛгавЛИіШЁДњЛљЧвВЛКЌгаМзЛљЕФЮЊ![]() ЁЃ
ЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЛьКЯЮяMжаПЩФмКЌгаAl2O3ЁЂFe2O3ЁЂAlЁЂCuЃЌЮЊШЗЖЈЦфзщГЩЃЌФГЭЌбЇЩшМЦШчЭМЫљЪОЗжЮіЗНАИЃК

ЯТСаЗжЮіе§ШЗЕФЪЧ
AЃЎШєm1>m2ЪБЃЌдђЛьКЯЮяMжавЛЖЈКЌгаAl2O3
BЃЎЩњГЩРЖЩЋШмвКЕФРызгЗНГЬЪНЮЊЃКCu+Fe3+=Cu2++Fe2+
CЃЎЙЬЬхBМШПЩФмЪЙДПОЛЮяЃЌгжПЩФмЪЧЛьКЯЮя
DЃЎвЊШЗЖЈЛьКЯЮяMжаЪЧЗёКЌгаAlЃЌПЩШЁMМгШыЪЪСПбЮЫс
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЛиД№ЯТСаЬюПеЃК
ЃЈ1ЃЉгаЯТСаЗжзгЛђРызгЃКЂйCS2ЃЌЂкPCl3ЃЌЂлH2SЃЌЂмCH2OЃЌЂнH3OЃЋЃЌЂоNH4+ЃЌЂпBF3ЃЌЂрSO2ЁЃСЃзгЕФСЂЬхЙЙаЭЮЊжБЯпаЮЕФга________(ЬюађКХЃЌЯТЭЌ)ЃЛСЃзгЕФСЂЬхЙЙаЭЮЊVаЮЕФга________ЃЛСЃзгЕФСЂЬхЙЙаЭЮЊЦНУцШ§НЧаЮЕФга________ЃЛСЃзгЕФСЂЬхЙЙаЭЮЊШ§НЧзЖаЮЕФга____ЃЛСЃзгЕФСЂЬхЙЙаЭЮЊе§ЫФУцЬхаЮЕФга____ЁЃ
ЃЈ2ЃЉЫзГЦЙтЦјЕФТШДњМзѕЃТШЗжзг(COCl2)ЮЊЦНУцШ§НЧаЮЃЌЕЋCЁЊClМќгыC=OМќжЎМфЕФМаНЧЮЊ124.3ЁуЃЛCЁЊClМќгыCЁЊClМќжЎМфЕФМаНЧЮЊ111.4ЁуЃЌНтЪЭЦфдвђЃК____ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП25ЁцЪБЃЌНЋ0.0l mol L -1 NaOHШмвКЕЮШы20mL0.01molЁЄL-1CH3COOHШмвКЕФЙ§ГЬжаЃЌШмвКжагЩЫЎЕчРыГіЕФc(H+)гыМгШыNaOHШмвКЬхЛ§ЕФЙиЯЕШчЭМЫљЪОЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ
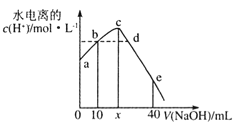
A. x=20ЃЌaЕуЕФзнзјБъЮЊ1.0ЁС10-12
B. bЕуКЭdЕуЫљЪОШмвКЕФpHЯрЕШ
C. ЕЮЖЈЙ§ГЬжаЃЌc(CH3COO-)гыc(OH-)ЕФБШжЕж№НЅдіДѓ
D. eЕуЫљЪОШмвКжаЃЌc(Na+)=2c(CH3COO-)+2c(CH3COOH)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП25CЪБ,0.1mol/LЕФ3жжШмвКЂйбЮЫсЂкАБЫЎЂлCH3COONaШмвКЁЃЯТСаЫЕЗЈжа,ВЛе§ШЗЕФЪЧ
A. 3жжШмвКжаpHзюаЁЕФЪЧЂй
B. 3жжШмвКжаЫЎЕФЕчРыГЬЖШзюДѓЕФЪЧЂл
C. ЂйгыЂкЕШЬхЛ§ЛьКЯКѓШмвКЯдЫсад
D. ЂйгыЂлЕШЬхЛ§ЛьКЯКѓc(Na+)>c(Cl-)>c(H+)>c(CH3COO-)>c(OH-)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгУNAБэЪОАЂЗќМгЕТТоГЃЪ§ЕФжЕЃЌЯТСаЫЕЗЈжаВЛе§ШЗЕФЪЧЃЈ ЃЉ
A.2.8 gввЯЉжаКЌга0.5NAИіІвМќ
B.68 gШлШкЕФKHSO4жаКЌгаNAИібєРызг
C.23.4 g NaClОЇЬхжаКЌга0.1NAИіТШЛЏФЦОЇАћ
D.КЌ1 molЬМдзгЕФН№ИеЪЏжаЃЌCЃCЙВМлМќЪ§ЮЊ2NAИі
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊNaHSO3ЯдЫсадЃЌNaHCO3ШмвКЯдМюадЃЌЯжгаХЈЖШЮЊ0.1mol/LЕФNaHSO3КЭNaHCO3СНжжШмвКЃЌСНжжШмвКжаИїСЃзгЕФЮяжЪЕФСПХЈЖШДцдкЯТСаЙиЯЕ(RБэЪОSЛђC)ЃЌЦфжае§ШЗЕФвЛзщЪЧ( )
A.c(Na+)ЃОc(HRO3Ѓ)ЃОc(H+)ЃОc(RO32-)ЃОc(OHЃ)
B.c(Na+)+c(H+)=c(HRO3Ѓ)+ c(RO32Ѓ)+c(OHЃ)
C.c(H+)+c(H2RO3)=c(RO32-)+c(OHЃ)
D.c(Na+)=c(HRO3Ѓ)+(H2RO3)+2c(RO32-)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдк25ЁцЁЂ101 kPaЯТЃЌ1 gМзДМШМЩеЩњГЩCO2КЭвКЬЌЫЎЪБЗХШШ22.68 kJ,ЯТСаШШЛЏбЇЗНГЬЪНе§ШЗЕФЪЧЃЈ ЃЉ
A. CH3OHЃЈlЃЉ+![]() O2ЃЈgЃЉ===CO2ЃЈgЃЉ+2H2OЃЈlЃЉЃЛІЄH=" +725.8" kJ/mol
O2ЃЈgЃЉ===CO2ЃЈgЃЉ+2H2OЃЈlЃЉЃЛІЄH=" +725.8" kJ/mol
B. 2CH3OHЃЈlЃЉ+3O2ЃЈgЃЉ===2CO2ЃЈgЃЉ+4H2OЃЈlЃЉЃЛІЄH= Ѓ1452 kJ/mol
C. 2CH3OHЃЈlЃЉ+3O2ЃЈgЃЉ===2CO2ЃЈgЃЉ+4H2OЃЈlЃЉЃЛІЄH= Ѓ725.8 kJ/mol
D. 2CH3OHЃЈlЃЉ+3O2ЃЈgЃЉ===2CO2ЃЈgЃЉ+4H2OЃЈlЃЉЃЛІЄH=" +1452" kJ/mol
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈе§ШЗЕФЪЧ( )
A.БъзМзДПіЯТЃЌ22.4LHFжаКЌгаЕФЗњдзгЪ§ФПЮЊNA(NAБэЪОАЂЗќМгЕТТоГЃЪ§)
B.0.1 mol/LЕФNH4HSO4ШмвКжаЕЮМг0.1 mol/LЕФBa(OH)2ШмвКжСГСЕэИеКУЭъШЋЃКc(NH4+)ЃОc(OH-)ЃОc(SO42-)ЃОc(H+)
C.1molШчЭМЫљЪО ЮяжЪгыХЈфхЫЎЗДгІЪБЭЈГЃзюЖрЯћКФBr2ЮЊ4mol
ЮяжЪгыХЈфхЫЎЗДгІЪБЭЈГЃзюЖрЯћКФBr2ЮЊ4mol
D.ГЃЮТЯТЃЌЗДгІC(s)+CO2(g)ЃН2CO(g)ВЛФмздЗЂНјааЃЌдђИУЗДгІЕФЁїHЃО0ЃЌвЛЖЈЬѕМўЯТЃЌЪЙгУДпЛЏМСФмМгПьЗДгІЫйТЪВЂЬсИпЗДгІЮяЕФЦНКтзЊЛЏТЪ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com