
【题目】配位键是一种特殊的共价键,即共用电子对由某原子单方面提供,同时和另一缺电子的粒子结合。如NH4+就是由NH3(氮原子提供电子对)和H+(缺电子)通过配位键形成的。据此,回答下列问题:
(1)下列粒子中可能存在配位键的是 (填字母)。
A.CO2 B.H3O+ C.CH4 D.H2SO4
(2)硼酸(H3BO3)溶液呈酸性,试写出其电离方程式: 。
(3)科学家对H2O2结构的认识经历了较为漫长的过程,最初科学家提出了两种观点:
甲: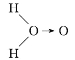 、乙:H—O—O—H,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:
、乙:H—O—O—H,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:
a.将C2H5OH与浓硫酸反应生成(C2H5)2SO4和水;
b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;
c.将生成的A与H2反应(已知该反应中H2作还原剂)。
①如果H2O2的结构如甲所示,实验c中的化学反应方程式为(A写结构简式) 。
②为了进一步确定H2O2的结构,还需要在实验c后添加一步实验d,请设计d的实验方案: 。
【答案】(1)BD
(2)H3BO3+H2O![]() H++[B(OH)4]-
H++[B(OH)4]-
(3)①![]() +H2
+H2![]() C2H5OC2H5+H2O
C2H5OC2H5+H2O
②用无水硫酸铜检验c的反应产物中有没有水(或其他合理答案)
【解析】配位键的形成条件:一方提供电子对,另一方提供空轨道。
(1)由题中信息可导出结论:凡能给出H+的物质中一般都含有配位键。(1)H3O+中O提供孤电子对,H+提供空轨道,NH4+中N提供孤电子对,H+提供空轨道,二者都能形成配位键。
(2)硼原子为缺电子原子,H3BO3的电离是B原子和水电离的OH-形成配位键,水电离的H+表现酸性,反应的离子方程式为H3BO3+H2O=H++[B(OH)4]-,
(3)①如果H2O2的结构如甲所示,实验c中A为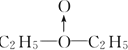 ,与氢气反应生成乙醚,方程式为
,与氢气反应生成乙醚,方程式为 ,②如为H0-OH结构,则A为C2H5-O-O-C2H5,与氢气反应生成乙醇,所以可用用无水硫酸铜检验c的反应产物中有没有水生成,如硫酸铜不变蓝,说明没有水生成,则说明过氧化氢中不含配位键,否则含有配位键,
,②如为H0-OH结构,则A为C2H5-O-O-C2H5,与氢气反应生成乙醇,所以可用用无水硫酸铜检验c的反应产物中有没有水生成,如硫酸铜不变蓝,说明没有水生成,则说明过氧化氢中不含配位键,否则含有配位键,


科目:高中化学 来源: 题型:
【题目】下图表示有关蛋白质分子的简要概念图,分析图示回答下列问题:
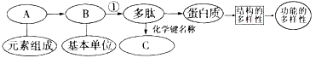
(1)此图中B代表__________,大约有______种,其分子结构通式为__________,C代表_______,其结构式是________。
(2)某蛋白质由104个氨基酸构成的含有四条肽链,在氨基酸形成该蛋白质过程中相对分子质量减少了__________。
(3)若该蛋白质是血红蛋白,说明蛋白质具有__________作用;若该蛋白质是酶,说明蛋白质具有__________作用;造成蛋白质功能多样性的原因(试从氨基酸的角度分析)_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是配制250mL0.2mol·L-1氯化钠溶液的步骤:
①溶解②洗涤③移液④计算⑤定容⑥称量⑦盖好瓶塞,反复上下颠倒,摇匀。请你选出该溶液配制的操作先后顺序是
A. ②③⑤①⑥⑦④ B. ④⑥①③②⑤⑦
C. ④②⑤⑥①③⑦ D. ②⑥⑦④③⑤①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A | B | C | D |
钢闸门容易被腐蚀 | a、b均为惰性电极,b极反应是:O+4OH﹣﹣4e﹣=2H2O | 阴、阳两极生成的气体的物质的量之比是1:1 | 电池工作一段时间 |
|
|
|
|
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于海水资源综合利用的说法中,正确的是
A.可用海水晒盐的方法提取海水中的淡水资源
B.只通过物理变化即可提取海水中的溴单质
C.从海带灰中提取I-,需加入CCl4萃取
D.利用海水、铝、空气发电是将化学能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语表示正确的是( )
A.氢氧化钠的电子式: ![]()
B.质子数为53、中子数为78的碘原子: ![]()
C.水分子比例模型: ![]()
D.对硝基甲苯的结构简式: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)是白色粉末,不溶于水、乙醇及稀硫酸,在空气中迅速被氧化成绿色,常用作有机合成工业中的催化剂.实验室拟以下列方法制取CuCl:在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl.试回答以下问题:
(1)CuCl制备过程中需配制物质的量浓度为2.0mol/L的CuSO4溶液. ①配制950mL 2.0mol/L的CuSO4溶液应称取胆矾的质量为g.
②某学生实际配制CuSO4溶液的浓度为1.8mol/L,原因可能是 .
A.托盘天平的砝码生锈 B.容量瓶中原来存有少量蒸馏水
C.溶解后的烧杯未经多次洗涤 D.胶头滴管加水定容时仰视刻度
(2)写出用上述方法制备CuCl的离子方程式 .
(3)在上述制取过程中,经过滤得到CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却,密封包装即得产品.其中“于70℃真空干燥”的目的是; . (回答两点)
(4)据世界卫生组织统计,最常用的避孕环含金属铜,避孕过程中生成了CuCl.其原因是铜与人体分泌物中的盐酸以及子宫内的空气反应:Cu+HCl+O2=CuCl+HO2 , HO2(超氧酸) 不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列说法或表示正确的是 .
A.氧化产物是HO2
B.HO2在碱中能稳定存在
C.HO2 的电离方程式是HO2H++O2﹣
D.1mol Cu 参加反应有2mol电子发生转移.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组利用荧光素—荧光素酶生物发光法,测定人参愈伤组织中ATP的含量,以研究人参细胞能量代谢的特点。
实验原理:荧光素在荧光素酶、ATP等物质参与下,进行反应发出荧光;用分光光度计可测定发光强度;当荧光素和荧光素酶都足量时,在一定范围内,ATP的含量与发光强度成正相关。
实验步骤:
一、ATP的提取:称取一定量的人参愈伤组织,研磨后沸水浴10min,冷却至室温,离心,取上清液。
二、ATP的测定:吸取一定量的上清液,放入分光光度计反应室内,并注入适量的所需物质,在有氧等适宜条件下进行反应,记录发光强度并计算ATP含量。
请回答:
(1)步骤一中的沸水浴处理,使酶的 被破坏而失活。
(2)步骤二注入的物质中,属于反应物的是 。分光光度计反应室内能量的转换形式是 。
(3)荧光素酶价格昂贵,为能准确测定出ATP的含量,又能节省酶的用量,学习小组探究了“测定ATP时所需荧光素酶溶液的最佳浓度”,实验结果如图。

①学习小组配制了1×10-8mol/LATP标准液、 和70mg/L的荧光素溶液(过量)进行实验。
②结果表明:
图中 点所对应的荧光素酶浓度为最佳浓度。
图中e、f、g点所对应的荧光素酶浓度不同,但发光强度相同,这是因为 。
(4)ATP测定对食品卫生监控有重要意义。食品卫生检验人员利用上述生物发光法测定某熟食品样品中细菌的ATP总含量,测算出了细菌的数量,从而判断食品污染程度。做出上述判断的理由是:每个细菌细胞中ATP的含量 。
(5)下列生理过程中,不消耗ATP的一组是( )
A.蛋白质的合成和加工 B.染色体的复制和运动
C.胰岛素的分泌 D.植物细胞的质壁分离和复原
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com