
【题目】工业合成橡胶可以利用以下途径:


(1)C5H12同分异构体共有_____种,其中核磁共振H谱图只有1种的结构简式为________。
(2)下列有关上述的C5H8说法正确的是_____________。
A.所有的原子可能共平面 B.和溴水、溴的四氯化碳反应的现象不完全相同
C.所有C原子可能共平面 D.和溴的四氯化碳溶液反应生成产物最多有2种
(3)写出分子式C5H8属于炔烃的所有同分异构体的结构简式_____________________。
(4)写出下列反应的化学方程式(注明反应条件):
①C5H12→C5H10Cl2:_______________________________________________________。
②C5H10Cl2→C5H8:_____________________________________________________。
(5)以乙烷为原料可合成聚氯乙烯。请设计合成路线(无机试剂及溶剂任选)。注:合成路线的书写格式参照如下示例流程图: __________
__________
【答案】3 C(CH3)4 BC CH≡CCH2CH2CH3 、CH3C≡CCH2CH3、CH≡CCH(CH3)2 ![]() CH3CCl(CH3)CH2CH2Cl+2NaOH
CH3CCl(CH3)CH2CH2Cl+2NaOH![]() CH2=C(CH3)CH=CH2+2NaCl+2H2O CH3CH3
CH2=C(CH3)CH=CH2+2NaCl+2H2O CH3CH3![]() CH3CH2Cl
CH3CH2Cl![]() CH2=CH2
CH2=CH2![]()
![]() CH2-CH2
CH2-CH2![]()
【解析】
由物质转化过程图并运用逆向思维分析,由![]() CH2C(CH3)=CHCH2
CH2C(CH3)=CHCH2![]() 结构知,C5H8通过加聚反应合成了
结构知,C5H8通过加聚反应合成了![]() CH2C(CH3)=CHCH2
CH2C(CH3)=CHCH2![]() ,即C5H8结构简式为CH2=C(CH3)CH=CH2,根据题给“已知”,C5H10Cl2在NaOH醇溶液中共热反应可生成CH2=C(CH3)CH=CH2,因烃与Cl2的取代反应过程中碳架不变,由C5H12在光照下生成二氯代烃C5H10Cl2可推断C5H12的结构,据此分析解答。
,即C5H8结构简式为CH2=C(CH3)CH=CH2,根据题给“已知”,C5H10Cl2在NaOH醇溶液中共热反应可生成CH2=C(CH3)CH=CH2,因烃与Cl2的取代反应过程中碳架不变,由C5H12在光照下生成二氯代烃C5H10Cl2可推断C5H12的结构,据此分析解答。
(1) C5H12属于烷烃,其同分异构体属于碳链异构,共有3种:CH3(CH2)3CH3、CH3CH(CH3)CH2CH3、(CH3)4C。其中,(CH3)4C分子中只有一种等效氢原子,则该分子的核磁共振H谱图只有1种的结构,其结构简式为:(CH3)4C。
(2)由物质转化过程图并逆向思维分析,由![]() CH2C(CH3)=CHCH2
CH2C(CH3)=CHCH2![]() 结构可知,C5H8通过加聚反应合成了
结构可知,C5H8通过加聚反应合成了![]() CH2C(CH3)=CHCH2
CH2C(CH3)=CHCH2![]() ,所以C5H8结构简式为CH2=C(CH3)CH=CH2,CH2=C(CH3)CH=CH2中2个碳碳双键构成的平面有可能共平面,但-CH3上3个氢原子不可能在双键决定的平面上,所以不可能所有原子共平面,A项错误;B. CH2=C(CH3)CH=CH2中含有碳碳双键可以与溴(Br2)发生加成反应,生成不溶水但能溶于四氯化碳的液态溴代烃,反应后溴水和溴的四氯化碳都褪色,但溴水反应后分层,下层是无色油状液体,溴的四氯化碳溶液反应后不分层,所以现象不完全相同,B项正确;C. 因单键可以旋转,所以CH2=C(CH3)CH=CH2分子中两个碳碳双键决定的平面有可能共平面如
,所以C5H8结构简式为CH2=C(CH3)CH=CH2,CH2=C(CH3)CH=CH2中2个碳碳双键构成的平面有可能共平面,但-CH3上3个氢原子不可能在双键决定的平面上,所以不可能所有原子共平面,A项错误;B. CH2=C(CH3)CH=CH2中含有碳碳双键可以与溴(Br2)发生加成反应,生成不溶水但能溶于四氯化碳的液态溴代烃,反应后溴水和溴的四氯化碳都褪色,但溴水反应后分层,下层是无色油状液体,溴的四氯化碳溶液反应后不分层,所以现象不完全相同,B项正确;C. 因单键可以旋转,所以CH2=C(CH3)CH=CH2分子中两个碳碳双键决定的平面有可能共平面如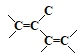 ,故所有C原子可能共平面,C项正确;D. CH2=C(CH3)CH=CH2与Br2发生1,2-加成和1,4-加成,及完全加成,其产物有:CH2BrC(CH3)BrCH=CH2、CH2=C(CH3)CHBrCH2Br、CH2BrC(CH3)=CHCH2Br、CH2BrC(CH3)BrCHBrCH2Br等共4种产物,D项错误;答案选BC。
,故所有C原子可能共平面,C项正确;D. CH2=C(CH3)CH=CH2与Br2发生1,2-加成和1,4-加成,及完全加成,其产物有:CH2BrC(CH3)BrCH=CH2、CH2=C(CH3)CHBrCH2Br、CH2BrC(CH3)=CHCH2Br、CH2BrC(CH3)BrCHBrCH2Br等共4种产物,D项错误;答案选BC。
(3)根据 C5H8不饱和度=2知,所求同分异构体中只有一个-C≡C-,先碳链异构再位置异构分别写出其同分异构体的结构简式:CH≡CCH2CH2CH3、CH3C≡CCH2CH3、CH≡CCH(CH3)2。
(4) 由第(2)题分析知C5H8结构简式为CH2=C(CH3)CH=CH2,根据题给“已知”卤代烃在NaOH醇溶液中共热可生成碳碳双键,且此过程碳架不变,由C5H10Cl2在NaOH醇溶液中可生成CH2=C(CH3)CH=CH2,C5H12在光照下发生取代反应生成二氯代烃C5H10Cl2,取代反应过程中碳架也不变,故C5H12的结构简式为CH3CH(CH3)CH2CH3。发生反应的化学方程式为①CH3CH(CH3)CH2CH3+2Cl2![]() CH3CCl(CH3)CH2CH2Cl+2HCl;②CH3CCl(CH3)CH2CH2Cl+2NaOH
CH3CCl(CH3)CH2CH2Cl+2HCl;②CH3CCl(CH3)CH2CH2Cl+2NaOH![]() CH2=C(CH3)CH=CH2+2NaCl+2H2O。
CH2=C(CH3)CH=CH2+2NaCl+2H2O。
(5)聚氯乙烯可由乙烯加聚得到,乙烯可由氯乙烷在NaOH醇溶液中加热得到,氯乙烷又可由乙烷与Cl2在光照下得到,所以由乙烷合成聚氯乙烯的流程图为:CH3CH3![]() CH3CH2Cl
CH3CH2Cl![]() CH2=CH2
CH2=CH2![]()
![]() CH2-CH2
CH2-CH2![]()


科目:高中化学 来源: 题型:
【题目】一种高寿命可循环的Zn/V2O5水性混合离子电池的结构示意图如下,放电时正极发生反应xLi++xe-+V2O5===LixV2O5。下列说法正确的是

A. 放电时,Li+在正极被还原
B. 充电时,溶液中Li+浓度不断减小
C. 放电时,电极A每减少6.5g,有0.1 mol Li+嵌入电极B
D. 充电时,电极B上的电势比电极A的高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10 mol·L-1的氨水滴定20.00 mL a mol·L-1的盐酸,混合溶液的pH与氨水的体积(V)的关系如图所示。下列说法不正确的是

A. 图上四点对应溶液中离子种类相同
B. 若N点溶液中存在c(H+)=c(OH-)+c(NH3·H2O) ,则N点为滴定反应的恰好反应点
C. 图上四点对应的溶液中水的电离程度由大到小排列为N>P>M>Q
D. 若N点为恰好反应点,则M点溶液中存在c(Cl-)=2c(NH3·H2O)+2c(NH4+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)甲醇(CH3OH,常温下为液态)是一种常用的能源物质。
①甲醇的热值为23 kJ · g-1。写出甲醇燃烧热的热化学方程式:_________________________。
②以甲醇为原料设计成燃料电池:若以熔融Na2CO3作为电解质,一极充入甲醇,另一极充入空气和CO2气体。回答下列问题:
充入空气和CO2气体的电极为__________极,该电池的总反应式:_____________________,充入甲醇电极的反应式:______________________________________。
③若用该燃料电池为电源,用石墨电极电解250 mL CuSO4溶液。则与充入空气和CO2气体的电极相连的是电解池的_______极;与甲醇电极相连的电极反应式为______________________;若燃料电池中消耗0.05 mol甲醇,电解池中共产生标准状况下气体2.24 L, 则原 CuSO4溶液浓度为________mol·L-1(假设电解前后溶液体积不变)。
(2)以四甲基氯化铵[(CH3)4NCl]水溶液为原料,通过电解法可以制备四甲基氢氧化铵[(CH3)4NOH],装置如图所示。写出该电解的总反应_________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl)是一种红褐色液体或黄色气体,其熔点64.5℃,沸点5.5℃,遇水易水解。它是有机合成中的重要试剂,可由NO与Cl2在常温常压下合成。
(1)实验室制备原料气NO和Cl2的装置如下图所示:

实验室制Cl2时,装置A中烧瓶内发生反应的化学方程式为____。装置B中盛放的试剂为____;
(2)将上述收集到的Cl2充入D的集气瓶中,按图示装置制备亚硝酰氯。

①NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为____。
②装置D中发生的反应方程式为___________________。
③如果不用装置E会引起什么后果_______________
④某同学认为装置F不能有效吸收尾气中的某种气体,该气体为_____,为了充分吸收尾气,可将尾气与____同时通入氢氧化钠溶液中。
(3)工业上可用间接电化学法除去NO,其原理如下图所示,吸收塔中发生的反应为:NO+S2O42+H2O→N2+HSO3

①吸收塔内发生反应的氧化剂与还原剂物质的量之比为_________。
②阴极的电极反应式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数,下列说法错误的个数是
①标准状况下,2.24L CH2Cl2含有的分子数为0.1 NA
②1mol苯甲酸中含有双键的数目为NA
③同温同压下,2 NA个C2H4(g)与NA个C4H8(g)的密度相等
④15g甲醛(HCHO)和乙酸的混合物中氧原子数为0.5NA
A. 2个 B. 3个 C. 4个 D. 1个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,将0.200mol·L-1的某一元酸HA与0.200mol·L-1的NaOH溶液等体积混合,充分反应后所得溶液中部分离子浓度如下表。下列说法中正确的是

A. 所得溶液中:c(Na+)>c(A-)>c(HA)>c(OH-)
B. t℃时,水的离子积Kw=1.0×10-13
C. t℃时,一元酸HA的电离常数K=3.10×10-7
D. t℃时,0.100mol·L-1NaA溶液中A-的水解率为0.80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示的一些物质或概念间的从属关系中不正确的是( )
![]()
A. X为含氧酸、Y为酸、Z为化合物
B. X为氧化物、Y为化合物、Z为纯净物
C. X为强碱、Y为碱、Z为化合物
D. X为非金属氧化物、Y为酸性氧化物、Z为氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,向500~600 ℃的铁屑中通入氯气生产无水氯化铁。现用如图所示的装置模拟上述过程进行实验。

(1)写出仪器的名称:a_______,b________。
(2)A中反应的化学方程式为________。C中反应的化学方程式为________。
(3)装置B中加入的试剂是________。
(4)已知:向热铁屑中通入氯化氢气体可以生产无水氯化亚铁。为防止有杂质FeCl2生成,可在装置__和__(填字母)间增加一个盛有________的洗气瓶。
(5)装置D的作用是________。为防止水蒸气影响无水氯化铁的制取,请你提出一个对装置D的改进方案:________。
(6)反应结束后,取少量装置C中的固体于试管中,加入足量盐酸,固体完全溶解,得到溶液X。证明溶液X中含有FeCl3的试剂是________,观察到的现象是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com