
【题目】进行化学实验必须注意安全.下列做法不正确的是( )
A.不慎将浓碱沾到皮肤上,立即用大量水冲洗,再涂上![]() 的硼酸溶液
的硼酸溶液
B.在点燃或加热可燃气体前检验其纯度,防止发生爆炸
C.向正在燃烧的酒精灯里添加酒精
D.钠燃烧着火,应用干燥的沙土盖灭
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
【题目】为了减少 CO 对大气的污染,某研究性学习小组拟研究 CO 和 H2O 反应转化为绿色能源H2。已知:
2CO(g)+O2(g) =2CO2(g); H=-566kJ·moL-1
2H2(g)+O2(g) =2H2O(g); H=-483.6kJ·moL-1
H2O(g) =H2O(l); H=-44.0kJ·moL-1
(1)表示氢气燃烧热的化学方程式中 △H=__________。
(2)写出CO和 H2O(g)作用生成 CO2 和 H2 的热化学方程式____________________________________________。
(3)往 1L 体积不变的容器中加入 0.200mol CO 和 1.00mol H2O(g),在 t℃时反应并达到平衡,若该反应的化学平衡常数 K=1(方程式中各物质前化学计量数为最简比),则 t℃时 CO 的转化率为____;反应达到平衡后,升高温度,此时平衡常数将__________ (填“变大”、 “不变”或“变小”),平衡将向__________ (填“正”或“逆”)方向移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究金属桥墩腐蚀及防护是跨海建桥的重要课题。下列判断中正确的是

A. 用装置①模拟研究时未见a上有气泡产生,说明铁棒没有被腐蚀
B. ②中桥墩与外加电源正极连接能确保桥墩不被腐蚀
C. ③中采用了牺牲阳极的阴极保护法保护桥墩
D. ①②③中海水均是实现化学能转化为电能的电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下有浓度均为0.5 mol/L的四种溶液:
①Na2CO3、②NaHCO3、③HCl、④NH3·H2O
(1)上述溶液中,可发生水解的是______(填序号,下同)。
(2)上述溶液中,既能与氢氧化钠反应,又能和硫酸反应的溶液中离子浓度由大到小的顺序为:_______________。
(3)向④中加入少量氯化铵固体,此时![]() 的值________(填“增大”、“减小”、或“不变”)。
的值________(填“增大”、“减小”、或“不变”)。
(4)若将③和④的溶液混合后溶液恰好呈中性,则混合前③的体积________④的体积(填“大于”、“小于”或“等于”)
(5)取10 mL溶液③,加水稀释到500 mL,则此时溶液中由水电离出的c(H+)=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,量取![]() 的两种二元酸
的两种二元酸![]() 与
与![]() 各
各![]() ,分别加水稀释,测得pH与加水稀释倍数有如图所示关系,则下列有关叙述不正确的是
,分别加水稀释,测得pH与加水稀释倍数有如图所示关系,则下列有关叙述不正确的是

A.![]() 为弱酸
为弱酸
B.NaHA水溶液中:![]()
C.含等物质的量的NaHA、NaHB的混合溶液中:![]()
D.![]() 的NaHB溶液中:
的NaHB溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A. 反应CaCO3(s)===CaO(s)+CO2(g)在常温下不能自发进行,则该反应的ΔH<0
B. 锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除去
C. 不能用玻璃瓶来盛装氟化钠水溶液
D. 常温下Ksp[Mg(OH)2]=5.6×10-12,pH=10的含Mg2+溶液中,c(Mg2+)≤5.6×10-4mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
A.1L1mol/L的氯化铁溶液中,若Cl-的数目为3NA,则Fe3+的数目为NA
B.将1molCl2通入水中,溶液中Cl-、ClO-、HClO的数目之和为2NA
C.常温下,1L0.lmol/L的Na2S溶液中阴离子数目大于0.1NA
D.78gNa2O2与足量的CO2反应转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨对人类的生产生活具有重要影响。
氨的制备与利用。
(1)工业合成氨的化学方程式是_______________。
氨的定量检测。水体中氨气和铵根离子(统称氨氮)总量的检测备受关注。利用氨气传感器检测水体中氨氮含量的示意图如下:

(2)利用平衡原理分析含氨氮水样中加入NaOH溶液的作用:________。
(3)若利用氨气传感器将1L水样中的氨氮完全转化为N2时,转移电子的物质的量为6×10-4mol,则水样中氨氮(以氨气计)含量为_________mg·L-1。
(4)氨的转化与去除。 微生物燃料电池(MFC)是一种现代化氨氮去除技术。如图为MFC碳氮联合同时去除的氮转化系统原理示意图。

已知A、B两极生成CO2和N2的物质的量之比为5:2,写出A极的电极反应式:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Na2CO3溶液中滴加盐酸,反应过程中能量变化如右图所示,下列说法正确的是
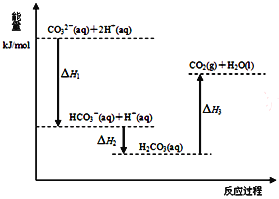
A. 反应HCO3-(aq)+H+(aq)=CO2(g)+H2O(l)为放热反应
B. H1>H2 H2<H3
C. CO32-(aq)+2H+(aq)=CO2(g)+H2O(l) H=(H1+H2+H3)
D. H2CO3(aq)=CO2(g)+H2O(l),若使用催化剂,则H3变小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com