
【题目】下列说法中不正确的是( )
A. 反应CaCO3(s)===CaO(s)+CO2(g)在常温下不能自发进行,则该反应的ΔH<0
B. 锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除去
C. 不能用玻璃瓶来盛装氟化钠水溶液
D. 常温下Ksp[Mg(OH)2]=5.6×10-12,pH=10的含Mg2+溶液中,c(Mg2+)≤5.6×10-4mol·L-1
【答案】A
【解析】由方程式可以知道![]() ,如反应能自发进行,则应满足
,如反应能自发进行,则应满足![]() ,而常温下不能进行,则
,而常温下不能进行,则![]() ,A错误;长期使用的锅炉需要定期除水垢,否则会降低燃料的利用率;水垢中含有的
,A错误;长期使用的锅炉需要定期除水垢,否则会降低燃料的利用率;水垢中含有的![]() ,可先用
,可先用![]() 溶液处理,
溶液处理,![]() 与
与![]() 生产更难溶的
生产更难溶的![]() 沉淀,使
沉淀,使![]() 的沉淀溶解平衡向右移,使之转化为疏松、易溶于酸的
的沉淀溶解平衡向右移,使之转化为疏松、易溶于酸的![]() ,而后用酸除去, B正确;氟化钠水解生成氢氟酸,玻璃成分中有二氧化硅,氢氟酸与二氧化硅反应,所以不能用玻璃瓶来盛装氟化钠水溶液,C正确;Ksp[Mg(OH)2]=c(Mg2+)×c2(OH-)=5.6×10-12, pH=10,c(OH-)=10-4mol/L,带入上式可得:浓度积为c(Mg2+)×(10-4)2≤5.6×10-12,c(Mg2+)≤5.6×10-4mol·L-1;D正确;正确选项A。
,而后用酸除去, B正确;氟化钠水解生成氢氟酸,玻璃成分中有二氧化硅,氢氟酸与二氧化硅反应,所以不能用玻璃瓶来盛装氟化钠水溶液,C正确;Ksp[Mg(OH)2]=c(Mg2+)×c2(OH-)=5.6×10-12, pH=10,c(OH-)=10-4mol/L,带入上式可得:浓度积为c(Mg2+)×(10-4)2≤5.6×10-12,c(Mg2+)≤5.6×10-4mol·L-1;D正确;正确选项A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】实验室需要0.5mol/L的硫酸溶液480mL,根据溶液的配制情况回答下列问题。
(1)在下图所示仪器中,配制上述溶液肯定不需要的是_________(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是 ___________________________。
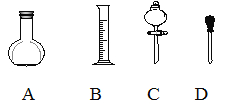
(2)根据计算得知,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为__mL,如果实验室有15mL、20mL、50mL量筒,应选用______ mL量筒最好。
(3)在容量瓶的使用方法中,下列操作不正确的是____________。
A、使用容量瓶前检验是否漏水
B、容量瓶用水洗净后,再用待配溶液洗涤
C、配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1—2cm处,用胶头滴管加蒸馏水至刻度线。
D、配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
E、盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(4)在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度______0.5mol/L(填“大于”“小于”或“等于”)。
(5)该同学在定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度。对所配溶液浓度的影响__________(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】周期表中前四周期的元素A、Z、Q、R、T的原子序数依次增大,且A、Z、Q同周期。A共有两个原子轨道上有电子,且电子数目相同。Z、Q相邻,且Z中的未成对电子数为3个,R元素在地壳中含量位于金属元素的第二位。T是人类最早使用的元素,并以这种元素命名了我国的一个时代。请回答下面的问题:
(1)A、Z、Q第一电离能从小到大的顺序为:_______________(填元素符号),T的价层电子排布图为:__________________________。
(2)Q的基态原子中能量最高的电子,其电子云在空间有___________个方向,原子轨道呈_______形。
(3)Z3-的立体构型为____________,写出与Z3-互为等电子体的一种非极性分子化学式____________。
(4)在不同的温度下,A以ACl2和二聚体A2Cl4两种形式存在,二聚体的结构式如图所示:
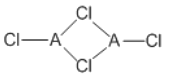
①ACl2中A的杂化方式为______________________。
②1mol A2Cl4中含配位键的数目为____________。
(5)R单质的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。体心立方晶胞和面心立方晶胞的棱边长分别为acm、bcm,则R单质的体心立方晶胞和面心立方晶胞的密度之比为_________,R原子配位数之比为_____________。
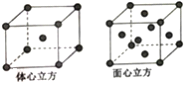
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物乙是一种治疗神经类疾病的药物,可由化合物甲经多步反应得到。下列有关甲、乙的说法正确的是
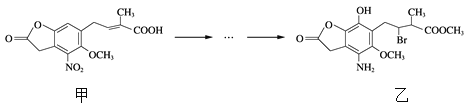
A. 甲的分子式为C14H14NO7
B. 甲、乙中各有1个手性碳原子
C. 可用NaHCO3溶液或FeCl3溶液鉴别化合物甲、乙
D. 乙能与盐酸、NaOH溶液反应,且1 mol乙最多能与5 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂。某种兴奋剂的结构简式如下图所示,有关该物质的说法正确的是

A. 遇FeCl3溶液显紫色,因为该物质与苯酚互为同系物
B. 滴入KMnO4(H+)溶液,观察紫色褪去,能证明结构中存在碳碳双键
C. 1 mol该物质与浓溴水和H2反应最多消耗Br2和H2分别为4 mol、7 mol
D. 该分子中的所有碳原子可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从樟科植物枝叶提取的精油中含有甲、乙两种成分:
![]()
![]()
(1)①用酸性高锰酸钾溶液检验甲和乙中含有碳碳双键,方案是否可行 填“可行”或“不可行”)。
②请写出甲的一种能同时满足下列3个条件的同分异构体的结构简式 。
a.苯环上有两个不同的取代基
b.能与Br2的CCl4溶液发生加成反应
c.遇FeCl3溶液呈现紫色
(2)由甲转化为乙的过程为(已略去无关产物):
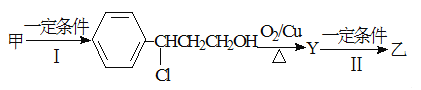
步骤Ⅰ的反应类型为 ,Y的结构简式 ,设计步骤Ⅰ的目的是 。
(3)1 mol乙最多可与 mol H2发生加成反应。
(4)写出乙与新制Cu(OH)2悬浊液反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.氧化反应一定有氧气的参与B.得到电子,发生了还原反应
C.置换反应不一定是氧化还原反应D.所含元素化合价升高的物质被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由A、B两种金属和稀硫酸组成的原电池,A是正极,则下列推断正确的是( )
A.A电极上发生的电极反应是还原反应
B.A的金属性强于B
C.电子不断由A电极经外电路流向B电极
D.溶液中的阳离子移向负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知下列反应:Fe + S == FeS 2Fe + 3Cl2 ==2FeCl3 3Fe + 2O2 ==Fe3O4 则 S,Cl2,O2 的氧化性:______>_____ >______
(2)用双线桥标出下列反应中电子转移的方向和数目:______
MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
该反应中的氧化剂是________,HCl体现的性质是_______________,若有4molHCl参加反应,则被氧化的HCl的物质的量是______mol,如反应中转移了0.4mol电子,则产生的Cl2在标准状况下体积为_________L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com