
【题目】【2015上海卷】实验室回收废水中苯酚的过程如右图所示。下列分析错误的是( )
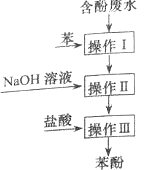
A.操作I中苯作萃取剂
B.苯酚钠在苯中的溶解度比在水中的大
C.通过操作II苯可循环使用
D.三步操作均需要分液漏斗
【答案】B
【解析】A.苯酚容易溶于有机溶剂苯,而难溶于水,水与苯互不相溶,因此 可用苯作萃取剂将含有苯酚的废水中的苯萃取出来,操作I中苯作萃取剂,正确。B.苯酚钠容易溶于水,而难溶于苯,因此在苯中的溶解度比在水中的小,错误。C.向萃取分液后的含有苯酚的溶液中加入NaOH溶液,发生反应:NaOH+C6H5OH=C6H5ONa+H2O,C6H5ONa容易溶于水,而与苯互不相溶,然后分液,得到的苯可再应用于含有苯酚的废水的处理,故通过操作II苯可循环使用,正确。D.再向含有苯酚钠的水层加入盐酸,发生 :C6H5ONa+HCl=C6H5OH+NaCl,苯酚难溶于水,密度比水大,在下层,通过分液与水分离开,通过上述分析可知在三步操作中都要进行分液操作,因此要使用分液漏斗,正确。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】保险粉(Na2S2O4)有极强的还原性,遇热水或潮湿空气会分解发热,但在碱性环境下较稳定。回答下列问题:
(1)二氧化硫的制备

①二氧化硫的发生装置可以选择上图中的_____________(填大写字母),反应的化学方程式为______________________。
②欲收集一瓶干燥的二氧化硫,选择上图中的装置,其接口的连接顺序为发生装置→__________________→→______→______→ ____________。(按气流方向,用小写字母表示)
(2)保险粉的制备
在35-45℃下,将SO2气体通入锌粉一水悬浮液中(如图),使之发生反应生成ZnS2O4;待反应完全后,移走恒温水浴装置并冷却至室温,向三颈烧瓶中加人18%的NaOH溶液,使之发生反应生成Na2S2O4和Zn(OH)2;经一系列操作后得到无水Na2S2O4样品。

①实验开始时,应先关闭止水夹K3、打开K1和K2,通入一段时间SO2,其原因是__________。
②通过观察_________________,调节止水夹K1来控制SO2的流速。
③由ZnS2O4生成Na2S2O4的化学方程式为_____________。
(3)称取2.0gNa2S2O4样品溶于冷水中,配成100mL吐溶液,取出10mL该溶液于试管中,用0 .10 mol/L的KMnO4溶液滴定(滴定至终点时产物为Na2SO4和MnSO4),重复上述操作2次,平均消耗溶液12.00mL。则该样品中Na2S2O4的质量分数为_______(杂质不参与反应)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】异丙苯(![]() ),是一种重要的有机化工原料。根据题意完成下列填空:
),是一种重要的有机化工原料。根据题意完成下列填空:
(1)由苯与2-丙醇反应制备异丙苯属于_____________反应;由异丙苯制备对溴异丙苯的反应试剂和反应条件为_____________________。
(2)异丙苯有多种同分异构体,其中一溴代物最少的芳香烃的名称是___________________________。
(3)α-甲基苯乙烯(![]() )是生产耐热型ABS树脂的一种单体,工业上由异丙苯催化脱氢得到。写出由异丙苯制取该单体的另一种方法__________________________(用化学反应方程式表示)。
)是生产耐热型ABS树脂的一种单体,工业上由异丙苯催化脱氢得到。写出由异丙苯制取该单体的另一种方法__________________________(用化学反应方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是(NA表示阿伏加德罗常数的值)
A.1 mol FeI2与足量氯气反应时转移的电子数为2NA
B.1 mol Al与足量氢氧化钠溶液反应生成33.6L气体
C.1 mol Na2O2固体中含离子总数为3NA
D.1 mol Mg与足量水反应生成2 mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化过程中,需要加入氧化剂的是( )
A. CO2 → CO B. FeCl3 →FeCl2 C. HCl → AgCl D. KI → I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2和I2在一定条件下能发生反应:H2(g) +I2(g) ![]() 2HI(g),已知每生成2mol HI(g),放出的热量为a kJ。
2HI(g),已知每生成2mol HI(g),放出的热量为a kJ。
另: (a、b、c均大于零)
(a、b、c均大于零)
下列说法正确的是
A. H2、I2和HI分子中的化学键都是非极性共价键
B. 断开2 mol HI分子中的化学键所需能量约为(c+b+a) kJ
C. 相同条件下,1 mol H2 (g)和1mol I2 (g)总能量小于2 mol HI (g)的总能量
D. 向密闭容器中加入2 mol H2 (g)和2 mol I2 (g),充分反应后放出的热量为2a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,向2 L恒容密闭容器中充入1 mol NO2与2 mol SO2发生如下反应:
NO2(g)+SO2(g)![]() SO3(g)+NO(g) ΔH=-41.8 kJ·mol-1。
SO3(g)+NO(g) ΔH=-41.8 kJ·mol-1。
(1)下列能说明该反应达到平衡状态的是 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗n mol SO3的同时生成n mol NO2
(2)反应进行到20 s 时,测得反应速率v(NO) = 0.005 mol·L-1·s-1,则消耗的NO2为 mol。
(3)下列措施能使反应加快的是 (仅改变一个条件)
a.降低温度 b.缩小容积 c.使用效率更高的催化剂
(4)若上述容器为绝热容器(与外界无热交换),则到达平衡所需时间将 。
a.延长 b.缩短 c.不变 d.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CPAE是蜂胶的主要活性成分,也可由咖啡酸合成

下列说法不正确的是
A.咖啡酸分子中所有原子可能处在同一个平面上
B.可用金属Na检测上述反应是否残留苯乙醇
C.1 mol 苯乙醇在O2中完全燃烧,需消耗10 mol O2
D.1 mol CPAE与足量的NaOH溶液反应,最多消耗3 mol NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com