
| A. | 油脂 | B. | 淀粉 | C. | 氨基酸 | D. | 葡萄糖 |
科目:高中化学 来源: 题型:选择题
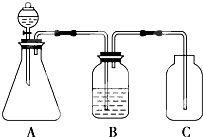
| A. | A中的化学反应可能为:CaCO3+2HCl═CO2↑+CaCl2+H2O | |
| B. | 装置B中盛放的试剂为Na2CO3溶液 | |
| C. | 装置C中盛放的为可溶性硅酸盐 | |
| D. | 由此实验可得到的结构是:酸性HCl>H2CO3>H2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) | |
| B. | 20mL 0.1mol/L CH3COONa溶液与10mL 0.1mol/L HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-) | |
| D. | 0.1mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应H2(g)+I2(g)?2HI(g)的平衡常数K=$\frac{c(HI)}{c({H}_{2})c({I}_{2})}$=49 | |
| B. | 反应2HI(g)?H2(g)+I2(g)的平衡常数K=$\frac{c({H}_{2})c({I}_{2})}{{c}^{2}(HI)}$=49 | |
| C. | 反应HI(g)?$\frac{1}{2}$H2(g)+$\frac{1}{2}$I2(g)的平衡常数K=$\frac{c({H}_{2})c({I}_{2})}{{c}^{2}(HI)}$=7 | |
| D. | 反应2HI(g)?H2(g)+I2(g)的平衡常数K=$\frac{c({H}_{2})c({I}_{2})}{{c}^{2}(HI)}$=$\frac{1}{49}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100g溶液中含有0.9g NaCl | B. | 100g水中含有0.9g NaCl | ||
| C. | 100g溶液中含有0.9mol NaCl | D. | 100g水中含有0.9mol NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 被提纯的物质 | 选用试剂 | 操作方法 |
| A | CaO(CaCO3) | 水 | 溶解、过滤、结晶 |
| B | CuSO4(H2SO4) | NaOH溶液 | 过滤 |
| C | CO2(CO) | 氧气 | 点燃 |
| D | Cu(CuO) | 稀盐酸 | 溶解、过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氮化铝中氮元素的化合价为-3 | |
| B. | 上述反应中每生成2molAlN,N2得到3mol电子 | |
| C. | 在氮化铝的合成反应中,N2是氧化剂,Al2O3是还原剂 | |
| D. | 该反应不属于四种基本反应类型中任一种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com