
| 44.8L |
| 22.4L/mol |
| n |
| V |
| 44.8L |
| 22.4L/mol |
| n |
| V |
| 2mol |
| 0.1L |
| 20mol/L×0.01L |
| 0.1L |
| n |
| V |


科目:高中化学 来源: 题型:
| A、将NaF溶液与浓硫酸混合共热制取氟化氢气体 | ||||
B、工业上:H2+Cl2
| ||||
| C、实验室用浓磷酸与溴化钠共热制溴化氢气体 | ||||
| D、实验室用碘化钠与浓硫酸共热制碘化氢气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、负极,并被氧化 |
| B、正极,并被还原 |
| C、负极,并被还原 |
| D、正极,并被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蛋白质中加Na2SO4后析出蛋白质 |
| B、蛋白质用福尔马林浸泡 |
| C、蛋白质中加Pb(Ac)2后析出蛋白质固体 |
| D、蛋白质中遇X光后 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验次数 | 称取样品 的质量/g | 所加Ba(OH)2溶液 的体积/mL | 测得生成沉 淀的质量/g |
| 1 | 5.28 | 500 | 9.85 |
| 2 | 10.56 | 500 | 19.70 |
| 3 | 15.84 | 500 | |
| 4 | 21.12 | 500 | 39.40 |
| 5 | 26.40 | 500 | 49.25 |
| 6 | 31.68 | 500 | 49.25 |
查看答案和解析>>
科目:高中化学 来源: 题型:
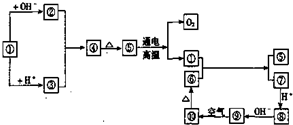
查看答案和解析>>
科目:高中化学 来源: 题型:
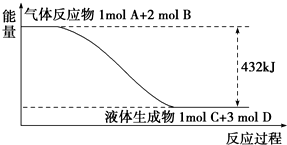 某反应过程中的能量变化如图所示:
某反应过程中的能量变化如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com