
ЁОЬтФПЁПдкКЌгаШѕЕчНтжЪЕФШмвКжаЃЌЭљЭљгаЖрИіЛЏбЇЦНКтЙВДцЃЎ
ЃЈ1ЃЉвЛЖЈЮТЖШЯТЃЌЯђ1L 0.1molLЉ1CH3COOHШмвКжаМгШы0.1mol CH3COONaЙЬЬхЃЌШмвКжа ![]() ЃЈЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБЃЉЃЛаДГіБэЪОИУЛьКЯШмвКжаЫљгаРызгХЈЖШжЎМфЕФвЛИіЕШЪН ЃЎ
ЃЈЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБЃЉЃЛаДГіБэЪОИУЛьКЯШмвКжаЫљгаРызгХЈЖШжЎМфЕФвЛИіЕШЪН ЃЎ
ЃЈ2ЃЉГЃЮТЯТЯђ20mL 0.1molLЉ1Na2CO3ШмвКжаж№ЕЮМгШы0.1molLЉ1HClШмвК40mLЃЌШмвКжаКЌЬМдЊЫиЕФИїжжЮЂСЃЃЈCO2вђвнГіЮДЛГіЃЉЮяжЪЕФСПЗжЪ§ЫцШмвКpHБфЛЏЕФЧщПіШчЯТЃКЛиД№ЯТСаЮЪЬтЃК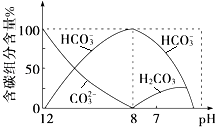
ЂйдкЭЌвЛШмвКжаЃЌH2CO3ЁЂHCO ![]() ЁЂCO
ЁЂCO ![]() ЃЈЬюЁАФмЁБЛђЁАВЛФмЁБЃЉДѓСПЙВДцЃЛ
ЃЈЬюЁАФмЁБЛђЁАВЛФмЁБЃЉДѓСПЙВДцЃЛ
ЂкЕБpH=7ЪБЃЌШмвКжаКЌЬМдЊЫиЕФжївЊЮЂСЃгаЁЂ ЃЌ ШмвКжаКЌСПзюЖрЕФШ§жжЮЂСЃЕФЮяжЪЕФСПХЈЖШЕФДѓаЁЙиЯЕЮЊ ЃЎ
ЁОД№АИЁП
ЃЈ1ЃЉВЛБфЃЛcЃЈCH3COOЉЃЉ+cЃЈOHЉЃЉ=cЃЈNa+ЃЉ+cЃЈH+ЃЉ
ЃЈ2ЃЉВЛФмЃЛHCO ![]() ЃЛH2CO3ЃЛcЃЈNa+ЃЉЃОcЃЈClЉЃЉЃОcЃЈHCO
ЃЛH2CO3ЃЛcЃЈNa+ЃЉЃОcЃЈClЉЃЉЃОcЃЈHCO ![]() ЃЉ
ЃЉ
ЁОНтЮіЁПНтЃКЃЈ1ЃЉвЛЖЈЮТЖШЯТЃЌЯђ1L 0.1molLЉ1CH3COOHШмвКжаМгШы0.1mol CH3COONaЙЬЬхЃЌгЩгкЮТЖШВЛБфЃЌЖјKa= ![]() жЛгыЮТЖШгаЙиЃЌЫљвд
жЛгыЮТЖШгаЙиЃЌЫљвд ![]() ЕФБШжЕВЛБфЃЛШмвКжаДцдкЕчКЩЪиКуЮЊЃКcЃЈCH3COOЉЃЉ+cЃЈOHЉЃЉ=cЃЈNa+ЃЉ+cЃЈH+ЃЉЃЌ ЫљвдД№АИЪЧЃКВЛБфЃЛcЃЈCH3COOЉЃЉ+cЃЈOHЉЃЉ=cЃЈNa+ЃЉ+cЃЈH+ЃЉЃЛЃЈ2ЃЉГЃЮТЯТдк20mL0.1mol/L Na2CO3ШмвКжаж№ЕЮМгШы0.1mol/L HClШмвК40mLЃЌЯШЗДгІЩњГЩЬМЫсЧтФЦЃЌдйгыбЮЫсЗДгІЩњГЩЖўбѕЛЏЬМЁЂЫЎЃЌЂйгЩЗДгІМАЭМЯѓПЩжЊЃЌдкЭЌвЛШмвКжаЃЌH2CO3ЁЂHCO
ЕФБШжЕВЛБфЃЛШмвКжаДцдкЕчКЩЪиКуЮЊЃКcЃЈCH3COOЉЃЉ+cЃЈOHЉЃЉ=cЃЈNa+ЃЉ+cЃЈH+ЃЉЃЌ ЫљвдД№АИЪЧЃКВЛБфЃЛcЃЈCH3COOЉЃЉ+cЃЈOHЉЃЉ=cЃЈNa+ЃЉ+cЃЈH+ЃЉЃЛЃЈ2ЃЉГЃЮТЯТдк20mL0.1mol/L Na2CO3ШмвКжаж№ЕЮМгШы0.1mol/L HClШмвК40mLЃЌЯШЗДгІЩњГЩЬМЫсЧтФЦЃЌдйгыбЮЫсЗДгІЩњГЩЖўбѕЛЏЬМЁЂЫЎЃЌЂйгЩЗДгІМАЭМЯѓПЩжЊЃЌдкЭЌвЛШмвКжаЃЌH2CO3ЁЂHCO ![]() ЁЂCO
ЁЂCO ![]() ВЛФмДѓСПЙВДцЃЌЫљвдД№АИЪЧЃКВЛФмЃЛЂкгЩЭМЯѓПЩжЊЃЌpH=7ЪБЃЌШмвКжаКЌЬМдЊЫиЕФжївЊЮЂСЃЮЊHCO
ВЛФмДѓСПЙВДцЃЌЫљвдД№АИЪЧЃКВЛФмЃЛЂкгЩЭМЯѓПЩжЊЃЌpH=7ЪБЃЌШмвКжаКЌЬМдЊЫиЕФжївЊЮЂСЃЮЊHCO ![]() ЁЂH2CO3 ЃЌ ЕчКЩЪиКуПЩжЊcЃЈNa+ЃЉ+cЃЈH+ЃЉ=cЃЈClЉЃЉ+cЃЈHCO
ЁЂH2CO3 ЃЌ ЕчКЩЪиКуПЩжЊcЃЈNa+ЃЉ+cЃЈH+ЃЉ=cЃЈClЉЃЉ+cЃЈHCO ![]() ЃЉ+cЃЈOHЉЃЉЃЌдђcЃЈNa+ЃЉЃОcЃЈClЉЃЉЃЌвђHCO3ЉЫЎНтЃЌдђШмвКжаКЌСПзюЖрЕФШ§жжЮЂСЃЕФЮяжЪЕФСПХЈЖШЕФДѓаЁЙиЯЕЮЊЃКcЃЈNa+ЃЉЃОcЃЈClЉЃЉЃОcЃЈHCO
ЃЉ+cЃЈOHЉЃЉЃЌдђcЃЈNa+ЃЉЃОcЃЈClЉЃЉЃЌвђHCO3ЉЫЎНтЃЌдђШмвКжаКЌСПзюЖрЕФШ§жжЮЂСЃЕФЮяжЪЕФСПХЈЖШЕФДѓаЁЙиЯЕЮЊЃКcЃЈNa+ЃЉЃОcЃЈClЉЃЉЃОcЃЈHCO ![]() ЃЉЃЌЫљвдД№АИЪЧЃКHCO
ЃЉЃЌЫљвдД№АИЪЧЃКHCO ![]() ЃЛH2CO3ЃЛcЃЈNa+ЃЉЃОcЃЈClЉЃЉЃОcЃЈHCO
ЃЛH2CO3ЃЛcЃЈNa+ЃЉЃОcЃЈClЉЃЉЃОcЃЈHCO ![]() ЃЉЃЎ
ЃЉЃЎ
ЁОПМЕуОЋЮіЁПРћгУШѕЕчНтжЪдкЫЎШмвКжаЕФЕчРыЦНКтЖдЬтФПНјааХаЖЯМДПЩЕУЕНД№АИЃЌашвЊЪьжЊЕБШѕЕчНтжЪЗжзгРыНтГЩРызгЕФЫйТЪЕШгкНсКЯГЩЗжзгЕФЫйТЪЪБЃЌШѕЕчНтжЪЕФЕчРыОЭДІгкЕчРыЦНКтзДЬЌЃЛЕчРыЦНКтЪЧЛЏбЇЦНКтЕФвЛжжЃЌЭЌбљОпгаЛЏбЇЦНКтЕФЬиеїЃЎЬѕМўИФБфЪБЦНКтвЦЖЏЕФЙцТЩЗћКЯРеЩГЬиСадРэЃЎ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЙигкЗЧН№ЪєбѕЛЏЮяЕФа№Ъіе§ШЗЕФЪЧЃК
A. ЖМЪЧЫсадбѕЛЏЮя B. ЖМЪЧЫсєћ
C. ЖМжЛКЌСНжждЊЫи D. ЖМЪЧЦјЬхЃЈГЃЮТГЃбЙЯТЃЉ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПМьбщSO2ЦјЬхжаЪЧЗёЛьгаCO2ЦјЬхЃЌПЩВЩгУЕФЗНЗЈЪЧЃЈ ЃЉ
A.ЭЈЙ§HNO3ЫсЛЏЕФBaЃЈNO3ЃЉ2ШмвК
B.ЯШЭЈЙ§зуСПЦЗКьШмвКЃЌдйЭЈЙ§ГЮЧхЪЏЛвЫЎ
C.ЯШЭЈЙ§зуСПNaOHШмвКЃЌдйЭЈЙ§ГЮЧхЪЏЛвЫЎ
D.ЯШЭЈЙ§зуСПЫсадKMnO4ШмвКЃЌдйЭЈЙ§ГЮЧхЪЏЛвЫЎ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПСкБНЖўМзЫсЖўЖЁѕЅDBPЪЧвЛжжГЃМћЕФЫмЛЏМСЃЌПЩвдввЯЉКЭСкЖўМзБНЮЊдСЯКЯГЩЃЌКЯГЩЙ§ГЬШчЭМЫљЪОЃК
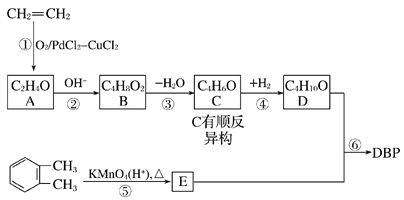
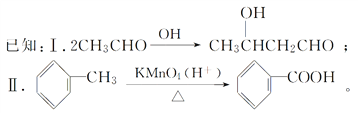
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉDBPЕФЗжзгЪНЮЊ________________ЃЌCЕФЫГЪННсЙЙЮЊ________________ЁЃ
ЃЈ2ЃЉBжаКЌгаЕФЙйФмЭХУћГЦЮЊ________________ЃЌЗДгІЂлЕФРраЭЮЊ________ЗДгІЁЃ
ЃЈ3ЃЉаДГіЯТСаЗДгІЕФЛЏбЇЗНГЬЪН
ЗДгІЂл______________________________________________________________
ЗДгІЂо_______________________________________________________________
ЃЈ4ЃЉEЕФвЛжжЭЌЗжвьЙЙЬхFЃЌЃЌБНЛЗЩЯКЌгаСНИіШЁДњЛљЃЌФмгыNaOHШмвКЗДгІЃЌЧв1 mol FЭъШЋЗДгІЯћКФ3 mol NaOHЃЌаДГіFЫљгаПЩФмЕФНсЙЙМђЪНЃК_______________________________________________________________ЁЃ
ЃЈ5ЃЉМьбщCжаЬМЬМЫЋМќЕФЗНЗЈ_______________________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПМзДММШЪЧживЊЕФЛЏЙЄдСЯЃЌгжПЩзїЮЊШМСЯЃЎРћгУКЯГЩЦјЃЈжївЊГЩЗжЮЊCOЁЂCO2КЭH2ЃЉдкДпЛЏМСЕФзїгУЯТКЯГЩМзДМЃЌЗЂЩњЕФжївЊЗДгІШчЯТЃК
ЂйCOЃЈgЃЉ+2H2ЃЈgЃЉ![]() CH3OHЃЈgЃЉ ІЄH1
CH3OHЃЈgЃЉ ІЄH1
ЂкCO2ЃЈgЃЉ+3H2ЃЈgЃЉ![]() CH3OHЃЈgЃЉ+H2OЃЈgЃЉ ІЄH2
CH3OHЃЈgЃЉ+H2OЃЈgЃЉ ІЄH2
ЂлCO2ЃЈgЃЉ+H2ЃЈgЃЉ![]() COЃЈgЃЉ+H2OЃЈgЃЉ ІЄH3
COЃЈgЃЉ+H2OЃЈgЃЉ ІЄH3
ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉвбжЊЗДгІЂйжаЕФЯрЙиЕФЛЏбЇМќМќФмЪ§ОнШчЯТЃК
ЛЏбЇМќ | HЉH | CЉO | CЁдO | HЉO | CЉH |
E/( kJmol-1) | 436 | 343 | 1076 | 465 | 413 |
гЩДЫМЦЫуІЄH1=______ЁЃвбжЊІЄH2=Љ58 kJmol-1ЃЌдђІЄH3=______ЁЃ
ЃЈ2ЃЉКЯГЩЦјжаЕФЧтЦјЪЧЗЂеЙжаЕФаТФмдДЃЌЫќЕФРћгУАќРЈжЦБИЁЂДЂДцКЭгІгУШ§ИіЛЗНкЁЃгыЦћгЭЯрБШЃЌЧтЦјзїЮЊШМСЯЕФгХЕуЪЧ__________________________________________________________ЃЈаДГіСНЕуЃЉЃЌШБЕуЪЧ______________________________________________________________________ЃЈаДГіСНЕуЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПбЮЫсОпгааджЪЪЧЃК
A. ШѕЫсад B. ЦЏАзад C. ЛгЗЂад D. ВЛЮШЖЈад
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПбЬЦј(жївЊЮлШОЮяSO2ЁЂNOx)ОO3дЄДІРэКѓгУCaSO3ЫЎаќИЁвКЮќЪеЃЌПЩМѕЩйбЬЦјжаSO2ЁЂNOxЕФКЌСПЁЃO3бѕЛЏбЬЦјжаSO2ЁЂNOxЕФжївЊЗДгІЕФШШЛЏбЇЗНГЬЪНЮЊЃКNO(g)ЃЋO3(g)=NO2(g)ЃЋO2(g) ЁїH=Ѓ200ЃЎ9kJЁЄmolЃ1 NO(g)ЃЋ1/2O2(g)=NO2(g) ЁїH=Ѓ58ЃЎ2kJЁЄmolЃ1 SO2(g)ЃЋO3(g)=SO3(g)ЃЋO2(g) ЁїH=Ѓ241ЃЎ6kJЁЄmolЃ1
ЃЈ1ЃЉЗДгІ3NO(g)ЃЋO3(g)=3NO2(g)ЕФЁїH=_______molЁЄLЃ1ЁЃ
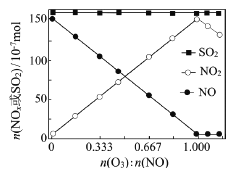
ЃЈ2ЃЉЪвЮТЯТЃЌЙЬЖЈНјШыЗДгІЦїЕФNOЁЂSO2ЕФЮяжЪЕФСПЃЌИФБфМгШыO3ЕФЮяжЪЕФСПЃЌЗДгІвЛЖЮЪБМфКѓЬхЯЕжаn(NO)ЁЂn(NO2)КЭn(SO2)ЫцЗДгІЧАn(O3)ЃКn(NO)ЕФБфЛЏМћгвЭМЁЃ
ЂйЕБn(O3)ЃКn(NO)>1ЪБЃЌЗДгІКѓNO2ЕФЮяжЪЕФСПМѕЩйЃЌЦфдвђЪЧ_________________
ЂкдіМгn(O3)ЃЌO3бѕЛЏSO2ЕФЗДгІМИКѕВЛЪмгАЯьЃЌЦфПЩФмдвђЪЧ___________________ЁЃ
ЃЈ3ЃЉЕБгУCaSO3ЫЎаќИЁвКЮќЪеОO3дЄДІРэЕФбЬЦјЪБЃЌШмвК(pHдМЮЊ 8)жаSO32ЃНЋNO2зЊЛЏЮЊNO2ЃЃЌЦфРызгЗНГЬЪНЮЊЃК_________________________________________________________________________________
ЃЈ4ЃЉCaSO3ЫЎаќИЁвКжаМгШыNa2SO4ШмвКЃЌДяЕНЦНКтКѓШмвКжаc(SO32Ѓ)=_____________________________[гУc(SO42Ѓ)ЁЂKsp(CaSO3)КЭKsp(CaSO4)БэЪО]ЃЛCaSO3ЫЎаќИЁвКжаМгШыNa2SO4ШмвКФмЬсИпNO2ЕФЮќЪеЫйТЪЃЌЦфжївЊдвђЪЧ__________________________________________________________________
ЃЈ5ЃЉМзДМШМСЯЕчГидкМюадШмвКжаЕФЕчМЋЗДгІЪНЁЃе§МЋ_________________________________ЃЛИКМЋ____________________________________________________________________________
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЫцзХЩњЛюЫЎЦНЕФЬсИпЃЌШЫУЧдНРДдНжиЪгЁАТЬЩЋЪГЦЗЁБЃЌТЬЩЋЪГЦЗЪЧжИ(ЁЁЁЁ)
A.ЬэМгСЫТЬЩЋЩЋЫиЕФЪГЦЗ
B.КЌгавЖТЬЫиЕФЪГЦЗ
C.дСЯЩњВњЙ§ГЬжаУЛгаЪЙгУЛЏЗЪЁЂХЉвЉЕФЪГЦЗ
D.дСЯЩњВњМАМгЙЄЙ§ГЬжаУЛгаЪмЕНЮлШОЕФЪГЦЗ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгУШчЭМЫљЪОзАжУНјааЯТСаЪЕбщЃЌНЋЗжвКТЉЖЗжаШмвКXМгШыдВЕзЩеЦПжагыYЗДгІЃЌЖдЪдЙмBжаЯжЯѓУшЪіВЛе§ШЗЕФЪЧ
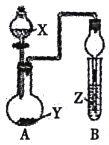
бЁЯю | XШмвК | ЙЬЬхY | ZШмвК | ЯжЯѓ |
A | 70%H2SO4 | Na2SO3ШмвК | H2SШмвК | ВњЩњЛызЧ |
B | ХЈАБЫЎ | CaO | ЗгЬЊЪдМС | ШмвКБфКь |
C | бЮЫс | ДѓРэЪЏ | Na2SiO3ШмвК | ГіЯжАзЩЋГСЕэ |
D | ХЈбЮЫс | MnO2 | NaOHШмвК | ЛЦТЬЩЋЦјЬхБЛЮќЪе |
A. A B. B C. C D. D
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com