
下列溶液一定呈中性的是
A.pH = 7的溶液
B.Kw = c(H+)·c(OH-) = 1.0×10-14的溶液
C.c(H+) = c(OH-)
D.pH = 3的酸与pH = 11的碱等体积混合后的溶液
科目:高中化学 来源:2014-2015广东省肇庆市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列关于中和滴定的操作错误的是
A.滴定前需要检查滴定管是否漏水
B.用对应加入的溶液润洗的仪器有:酸式滴定管、锥形瓶
C.用标准盐酸测定氨水的浓度,最适宜使用的指示剂是甲基橙
D.已知浓度滴定未知溶液,终点读数时俯视滴定管的刻度,会造成计算值偏低
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省广州市五校高二上学期期末联考化学试卷(解析版) 题型:选择题
对于可逆反应A(g)+2B(g) 2C(g) △H>0,下列图象中正确的是
2C(g) △H>0,下列图象中正确的是

查看答案和解析>>
科目:高中化学 来源:2014-2015广东省广雅等四校高二上学期期末联考化学试卷(解析版) 题型:选择题
下列各溶液中,微粒的物质的量浓度关系正确的是
A.0.1 mol/L Na2CO3溶液:c(OH-) = c(HCO3-) + c(H+) + 2c(H2CO3)
B.0.1 mol/L NH4Cl溶液:c(NH4+ ) = c(Cl-)
C.向醋酸钠溶液中加适量醋酸,得到的酸性混合溶液:c(Na+) > c(CH3COO-) > c(H+) > c(OH-)
D.向硝酸钠溶液中滴加稀盐酸得到pH = 5的混合溶液:c(Na+) = c(NO3-)
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省广雅等四校高二上学期期末联考化学试卷(解析版) 题型:选择题
25℃时,水的电离达到平衡:H2O H+ + OH-,下列叙述正确的是
H+ + OH-,下列叙述正确的是
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D.将水加热,Kw增大,pH不变
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省高三上学期期中考试化学试卷(解析版) 题型:填空题
(8分)无色透明溶液中可能含有下列离子:K+、Al3+、Fe3+、Ba2+、NO3-、SO42-、HCO3-、Cl-,取该溶液进行如下实验:①用蓝色石蕊试纸检测该溶液,试纸显红色;
②取原溶液少许,加铜片和稀硫酸共热,产生无色气体,该气体遇空气立即变为红棕色;
③取原溶液少许,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失;
④取原溶液少许,滴入氯化钡溶液产生白色沉淀;
⑤取实验④后的澄清溶液,滴入硝酸银溶液产生白色沉淀,再加入过量的稀硝酸,沉淀不消失。请回答下列问题:
(1)根据上述实验判断原溶液中上述离子肯定存在的是 ,
肯定不存在的是 。
(2)写出与②③两个实验有关的离子方程式:
② ,
③ 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省高三上学期期中考试化学试卷(解析版) 题型:选择题
下列关于化学用语的表示正确的是
A.过氧化钠的电子式: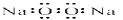
B.质子数为35、中子数为45的溴原子: Br
Br
C.氯化铵、次氯酸都属于强电解质
D.只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省益阳市高一上学期期中考试化学卷(解析版) 题型:选择题
(4*2分)写出下列反应的离子方程式:
(1)氢氧化钠与硫酸反应 ;
(2)实验室制取CO2气体 ;
(3)少量CO2气体通入澄清石灰水 ;
(4)硫酸铜溶液与氢氧化钠反应 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省新密市高三第三次月考化学试卷(解析版) 题型:选择题
一定条件下,用甲烷可以消除氮的氧化物(NOx)的污染,已知:
①CH4(g)+4NO2(g) =4NO(g)+CO2(g)+2H2O(g) ΔH1=-574kJ·mol-1
②CH4(g)+4NO(g) =2N2(g)+CO2(g)+2H2O(g) ΔH2=-1160kJ·mol-1;下列选项正确的是
A.CH4(g)+2NO2(g) =N2(g)+CO2(g)+2H2O(g) ΔH=-867kJ·mol-1
B.CH4(g)+4NO2(g) =4NO(g)+CO2(g)+2H2O(l) ΔH3>ΔH1
C.若用0.2mol CH4还原NO2至N2,则反应中放出的热量一定为173.4kJ
D.若用标准状况下2.24L CH4还原NO2至N2,整个过程中转移的电子为1.6mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com