
【题目】下列书写正确的是
A. NaHCO3=Na+ + H+ + CO32-B. NaHSO4=Na+ + HSO4-
C. CH3COOH=CH3COO- +H+ D. Na2SO4=2Na+ + SO42-
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.国庆70周年大典放飞的气球由可降解材料制成,主要成分是聚乙烯
B.歼- 20上用到的氮化镓材料是一种金属合金材料
C.我国发射的“嫦娥三号”卫星所使用的碳纤维,是一种无机非金属材料
D.“绿水青山就是金山银山”。推广聚氯乙烯代替木材,生产快餐盒等,以减少术材的使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氧化还原反应的叙述正确的是( )
A.在反应中不一定所有元素的化合价都发生变化
B.肯定有一种元素被氧化,另一种元素被还原
C.非金属单质在反应中只作氧化剂
D.金属原子失电子越多,其还原性越强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为实现“绿色奥运”,下列建议不合理的是( )
A.推广使用无磷洗涤剂
B.推广垃圾分类存放、回收和处理
C.提倡使用手帕,减少餐巾纸的使用
D.提倡使用一次性塑料餐具和塑料袋
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼和氮元素在化学中有很重要的地位,回答下列问题:
(1)基态硼原子核外电子有种不同的运动状态,基态氮原子的价层电子排布图为 . 预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2].(CH3)2NNH2中N原子的杂化方式为 .
(2)化合物H3BNH3是一种潜在的储氢材料,可利用化合物B3N3H6通过如下反应制得:3CH4+2B3N3H6+6H2O═3CO2+6H3BNH3①H3BNH3分子中是否存在配位键(填“是”或“否”),B、C、N、O的第一电离能由小到大的顺序为 .
②与B3N3H6互为等电子体的分子是(填一个即可),B3N3H6为非极性分子,根据等电子原理写出B3N3H6的结构式 .
(3)“嫦娥五号”探测器采用太阳能电池板提供能量,在太阳能电池板材料中除单晶硅外,还有铜,铟,镓,硒等化学物质,回答下列问题:①SeO3分子的立体构型为 .
②金属铜投入氨水或H2O2溶液中均无明显现象,但投入氨水与H2O2的混合溶液中,则铜片溶解,溶液呈深蓝色,写出该反应的离子反应方程式为 .
③某种铜合金的晶胞结构如图所示,该晶胞中距离最近的铜原子和氮原子间的距离为 ![]() apm,则该晶体的密度为(用含a的代数式表示,设NA为阿伏伽德罗常数的值).
apm,则该晶体的密度为(用含a的代数式表示,设NA为阿伏伽德罗常数的值).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】成环反应在有机合成中具有重要应用,某环状化合物G的合成过程如下: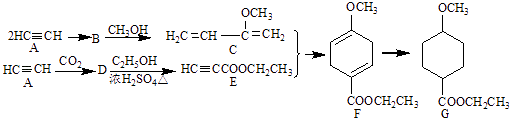
(1)A→B为加成反应,则B的结构简式是;B→C的反应类型是 .
(2)G中含有的官能团名称是;F的化学式为 .
(3)D→E的化学方程式是 .
(4)H是F的同分异构体,具有下列结构特征:①核磁共振氢谱除苯环吸收峰外仅有1个吸收峰;②存在甲氧基(CH3O﹣).H的结构简式是 .
(5)由C通过加聚反应合成的顺式高分子化合物M的化学方程式为 .
(6)下列说法正确的是 . a.A能和HCl反应得到聚氯乙烯的单体 b.D和F中均含有2个π键
c.1molG完全燃烧生成8mol H2O d.F能发生加成反应、取代反应、氧化反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
主族周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(1)在③~⑦元素中,原子半径最大的是______,其离子的原子结构示意图为______________。
(2)元素的最高价氧化物对应的水化物中酸性最强的是____________,碱性最强的是____________,呈两性的氢氧化物是________________。
(3)按要求写出下列两种物质的电子式:①的氢化物__________________;⑨的最高价氧化物对应的水化物_______________________;
(4)在⑦与⑩的单质中,化学性质较活泼的是______,可用什么化学反应说明该事实(写出反应的化学方程式) :__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质发生变化时,所克服的粒子间相互作用属于同种类型的是( )
A.液溴和苯分别受热变为气体
B.干冰和氯化铵分别受热变为气体
C.二氧化硅和铁分别受热熔化
D.食盐和葡萄糖分别溶解在水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水在25℃和95℃时,其电离平衡曲线如图所示: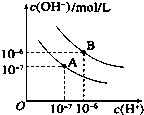
(1)则25℃时水的电离平衡曲线应为(填“A”或“B”),请说明理由
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com