
【题目】氢氧化铝可作为治疗某种胃病的内服药,这是利用了氢氧化铝的哪个性质( )
A.酸性
B.碱性
C.两性
D.氧化性
 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】20℃时,饱和NaCl溶液密度为1.1g.cm-3,物质的量浓度为5.0mol·L-1,下列说法不正确的是
A. 25℃时,饱和NaCl溶波的物质的量浓度大于5.0mol/L
B. 20℃时,饱和NaCl溶液的质量分数约为26.6%
C. 20℃时,密度小于1.1g/cm3的NaCl溶液是不饱和溶液
D. 将此饱和NaCl溶液蒸发部分水,再恢复到20℃时,溶液密度一定大于1.1g/cm3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸橙花酯是一种食用香料,其结构简式如图,关于该有机物的叙述中正确的是( )
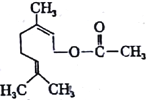
①1mol该有机物可消耗3molH2;②不能发生银镜反应;③分子式为C12H20O2;④它的同分异构体中可能有酚类;⑤1mol该有机物水解时只能消耗1molNaOH
A. ②③⑤ B. ①④⑤ C. ①②③ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=l.1×10-12以及Ksp[Cu(OH)2] =2×10-20。下列说法错误的是
A. 常温下AgCl饱和溶液和Ag2CrO4饱和溶液的物质的量浓度比较:c(AgCl)<c(Ag2CrO4)
B. 常温下,在0.010molL-1的AgNO3溶液中,AgCl与Ag2CrO4分别能达到的最大物质的量浓度比较:c(AgCl)<c(Ag2CrO4)
C. 某CuSO4溶液里c(Cu2+)=0.02 molL-1,如要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于5
D. 要使0.2molL-1 CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液PH为6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从樟科植物枝叶提取的精油中含有一种有机物 ![]() ,则对该有机物的说法正确的是( )
,则对该有机物的说法正确的是( )
A.能使溴水、酸性高锰酸钾溶液褪色
B.分子中所有原子在同一平面内
C.分子式为C9H12O
D.能发生加成反应、酯化反应、水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用金属钠和空气制备纯度较高的Na2O2,可利用的装置如下:
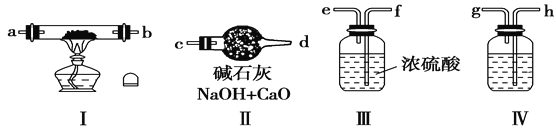
请回答下列问题:
(1)若规定气体的流动方向为从左到右,则组合实验装置时各仪器的连接顺序是:空气→Ⅳ→________→________→________(填“Ⅰ、Ⅱ、Ⅲ”,仪器不能重复使用)。
(2)装置Ⅳ中盛放的药品是___________,其作用是____________________。
(3)装置Ⅱ的作用是_________________________________________。
(4)加热装置Ⅰ时发生反应的化学方程式为___________________________。
(5)下列对于过氧化钠的叙述中,正确的是___________。
A.过氧化钠能与酸反应生成盐和水,所以过氧化钠是碱性氧化物
B.将过量Na2O2投入紫色石蕊试液中,溶液变蓝
C.过氧化钠与水反应时,过氧化钠是氧化剂,水是还原剂
D.过氧化钠与二氧化碳反应时,过氧化钠既是氧化剂又是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在常温常压下: ①2CH3OH(l)+2O2(g)═2CO(g)+4H2O(g)△H=﹣a kJmol﹣1
②2CO(g)+O2(g)═2CO2(g)△H=﹣b kJmol﹣1
③H2O(g)═H2O(l)△H=﹣c kJmol﹣1
则表示CH3OH(l)燃烧热的热化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,在浓度为1mol/L的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2的溶液中,测其c(NH4+)分别为a、b、c(单位为mol/L),下列判断正确的是
A. a=b=c B. a>b>c C. a>c>b D. c>a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(11分)为了探究Cl2、SO2同时通入H2O发生的反应,某校化学兴趣小组同学设计了如下图所示的实验装置。
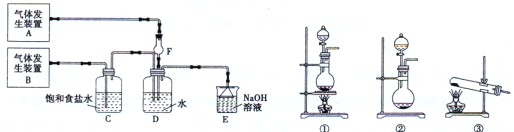
试填空:
(1)该化学兴趣小组的同学为制取Cl2、SO2气体,现采用Na2SO3与70%的浓硫酸为原料制取SO2,采用MnO2和浓盐酸(12 mol·L-1)为原料制取Cl2。在此实验中,F仪器的作用是 ;气体发生装置B应选择①、②、③三种装置中的 (选填序号)。
(2)D装置中主要反应的离子方程式为: 。
(3)为验证通入D装置中气体是Cl2过量还是SO2过量,兴趣小组的同!学准备了以下试剂:氯化铁溶液;氯化亚铁溶液;硫氰化钾溶液;苯酚溶液;品红溶液;酸性高锰酸钾溶液。
若Cl2量:取适量D中溶液滴加至盛有 (试剂名称,下同)的试管中,再加入产生的现象是 ,说明Cl2过量;
若SO2过量:取适量D中溶液滴加至盛有 的试管内,产生的现象是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com