
【题目】【化学一选修3:物质结构与性质】
磷及其化合物在工农业生产上应用非常广泛。
(1)磷元素位于周期表的_______区,基态磷原子价层电子排布图________,最高能层符号________。
(2)磷的三种同素异形体的结构如下图所示。

①三种同素异形体中能导电的是_______(填名称)。
②白磷易溶于CS2,其原因是___________。
(3)磷酸与Fe3+可形成H3[Fe(PO4)2],Fe、P、O电负性由大到小的顺序是________。与PO43-空间构型相同的分子和阴离子分别是________(各举1例)。
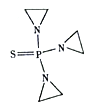
(4)噻替哌的结构简式如右图所示,其中氮原子的杂化轨道类型为_______,1mol噻替哌中含有的σ键数目为______。
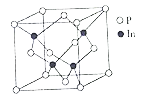
(5)磷化铟(InP)是一种半导体材料,可用于光纤通信技术,其晶胞结构如图所示。
①结构化学上常用原子坐标参数表示晶胞内部各原子的相对位置,晶胞中P原子的坐标参数分别有:P(0,0,0),P(![]() ,0,
,0, ![]() );P(0,
);P(0, ![]() ,
, ![]() )等,则距离上述三个P原子最近且等离的In原子的坐标参数为_____。
)等,则距离上述三个P原子最近且等离的In原子的坐标参数为_____。
②已知晶胞参数a=0.587m,则InP晶体的密度为______g/cm3。
【答案】 p 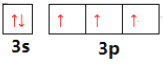 M 黑磷 P4和 CS2是非极性分子,根据相似相溶的原理,P4易溶于 CS2 O>P>Fe CCl4(或SiCl4等)和SO42- (或ClO4-等) sp3 25NA (1/4, 1/4, 1/4) 4.8
M 黑磷 P4和 CS2是非极性分子,根据相似相溶的原理,P4易溶于 CS2 O>P>Fe CCl4(或SiCl4等)和SO42- (或ClO4-等) sp3 25NA (1/4, 1/4, 1/4) 4.8
【解析】(1)P原子核外有15个电子,核外电子排布为1s22s22p63s23p3, 最外层为3s23p3,则磷元素位于周期表的p区;分三层排布,即有三个能层,所以电子占据的最高能层符号为M;基态磷原子价层电子排布图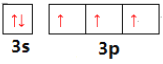 ;正确答案: p ;
;正确答案: p ;  ; M 。
; M 。
(2) ①磷结构与石墨相似,黑磷能导电,正确答案:黑磷。
②相似相溶原理是指因为极性分子间的电性作用,使得极性分子组成的溶质易溶于极性分子组成的溶剂,难溶于非极性分子组成的溶剂,非极性分子组成的溶质易溶于非极性分子组成的溶剂,难溶于极性分子组成的溶剂;![]() 和
和![]() 是非极性分子,根据相似相溶的原理,
是非极性分子,根据相似相溶的原理,![]() 易溶于
易溶于![]() ;正确答案: P4和 CS2是非极性分子,根据相似相溶的原理,P4易溶于 CS2。
;正确答案: P4和 CS2是非极性分子,根据相似相溶的原理,P4易溶于 CS2。
(3) 同周期元素,从左到右电负性逐渐增大,同主族元素从下到上,电负性逐渐增大,所以Fe、P、O电负性由大到小的顺序O>P>Fe;P原子的价层电子对![]() ,且不含孤电子对,所以其空间构型正四面体,与
,且不含孤电子对,所以其空间构型正四面体,与![]() 空间构型相同的分子和阴离子分别是
空间构型相同的分子和阴离子分别是![]() (或
(或![]() 等)和
等)和![]() (或
(或![]() 、
、![]() );正确答案:O>P>Fe ;CCl4(或SiCl4等)和SO42- (或ClO4-等)。
);正确答案:O>P>Fe ;CCl4(或SiCl4等)和SO42- (或ClO4-等)。
(4)噻替哌分子中,N原子含有3个![]() 键和一个孤电子对,所以采取
键和一个孤电子对,所以采取![]() 杂化,环上的C原子含有4个
杂化,环上的C原子含有4个![]() 键,一个噻替哌分子中含有25个
键,一个噻替哌分子中含有25个![]() 键,所以
键,所以![]() 噻替哌分子中
噻替哌分子中![]() 键为数目为25NA ,正确答案: sp3 ;25NA。
键为数目为25NA ,正确答案: sp3 ;25NA。
(5) ①将左下角的P原子理解为(0,0,0),由图可知距离上述三个P原子最近且等离的In原子的坐标参数为(1/4,1/4,1/4) ;正确答案:(1/4, 1/4, 1/4)。
②磷化铟InP中P原子数目为![]() ,In原子数目为4,晶胞质量
,In原子数目为4,晶胞质量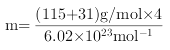 ,晶胞体积
,晶胞体积![]() =(0.587×10-7)3cm3;晶体的密度密度ρ=m/V=
=(0.587×10-7)3cm3;晶体的密度密度ρ=m/V=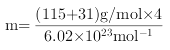 /(0.587×10-7)3=4.8 g/cm3;正确答案:4.8。
/(0.587×10-7)3=4.8 g/cm3;正确答案:4.8。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】如图1是细胞中化合物含量的扇形图,图2是有活性的细胞中元素含量的柱形图,下列说法不正确的是( )

A. 若图1表示细胞鲜重,则A、B化合物依次是H2O、蛋白质
B. 若图2表示组成人体细胞的元素含量,则a、b、c依次是O、C、H
C. 地壳与活细胞中含量最多的元素都是a,因此说明生物界与非生物界具有统一性
D. 若图1表示细胞完全脱水后化合物的含量,则A化合物具有多样性,其中含的元素为C、H、O、N
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某学习小组做Na2O2与H2O反应的实验,发现一些有趣的现象:
①取适量Na2O2固体用脱脂棉包好放在石棉网上,然后向脱脂棉上滴加3-4滴水,结果脱脂棉剧烈燃烧。
②取适量Na2O2固体置于试管中,加水使其充分反应至不再产生气体为止,滴入几滴酚酞试液,溶液先变红后褪色。回答有关问题。
(1)写出Na2O2的电子式_______________________。
(2)已知Na2O2可看作二元弱酸H2O2对应的盐,其第一步水解完全进行。写出其第一步水解的离子方程式为___________________________________。
(3)由①实验现象所得出的有关结论是:a.有氧气生成;b.___________________。
(4)Na2O2与H2O反应的离子方程式____________________________________。
II.为探究Na2O2与H2O反应的机理,他们在老师的指导下设计了下图所示装置。连接好装置,打开K1、K2,通过注射器注入适量蒸馏水,充分反应后用气球鼓气,Na2S溶液变浑浊,酸性KMnO4溶液褪色。分别取A、C中溶液滴入几滴酚酞,开始都变红,以后A中溶液很快褪色,C中溶液缓慢褪色。另取A、C中溶液分别加入少量二氧化锰,充分振荡,发现均反应剧烈、产生大量气泡,把带火星的木条伸入试管,木条复燃,向反应后的溶液中滴入几滴酚酞试液,溶液变红不褪色。
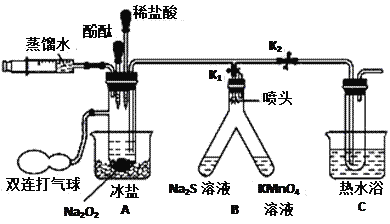
(5)A中冰盐和C中热水的作用分别是__________________,___________________。
(6)用化学方程式表示Na2S变浑浊的原因___________________________________。
(7)用离子方程式表示KMnO4溶液褪色的原因(MnO4-在酸性条件下被还原成Mn2+)__________________________________________。
(8)Na2O2与H2O反应的机理是(用化学方程式表示)第一步_____________________,第二步_______________________________。
(9)若向Na2O2中滴加适量的稀盐酸,也能产生同样的气体,请写出该反应的化学方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成气的主要成分是 一氧化碳和氢气,是重要的化工原料。
I.已知下列反应:
①CH4(g) + H2O(g)![]() CO(g) + 3H2(g) ΔH = +206 kJ/mol
CO(g) + 3H2(g) ΔH = +206 kJ/mol
②C(s) + H2O(g) = CO(g) + H2(g) ΔH = +131 kJ/mol
(1)工业制取炭黑的方法之一是将甲烷隔绝空气加热到1300℃进行裂解。填写空白。
CH4(g)= C(s)+ 2H2(g) ΔH =______________kJ/mol。
(2)若800℃时,反应①的平衡常数K1=1.0,某时刻测得该温度下,密闭容器中各物质的物质的量浓度分别为:c(CH4)=4.0 mol·L-1;c(H2O)=5.0 mol·L-1;c(CO)=1.5 mol·L-1;c(H2)=2 mol·L-1,则此时该可逆反应的状态是_____________________(填“达到平衡”、“向正反应方向移动”或“向逆反应方向移动”)。
Ⅱ.甲醇是一种可再生能源,工业上用合成气来合成甲醇:CO(g)+2H2(g)![]() CH3OH(g),分析该反应并回答下列问题:
CH3OH(g),分析该反应并回答下列问题:
(3)一定条件下,将CO与H2以物质的量之比1:1置于恒容密闭容器中发生以上反应,能说明该反应已达到平衡的是_____________________________。
A.体系的压强不发生变化 B.混合气的密度保持不变
C.体系中碳元素的质量分数不变 D.CO与H2的物质的量之比保持不变
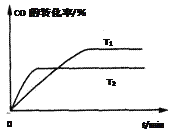
(4)如图是该反应在不同温度下CO的转化率随时间变化的曲线。T1和T2温度下的平衡常数大小关系是K1______K2 (填“>”、“<”或“=”)。理由是__________________________________________________。
(5)已知甲醇燃料电池的工作原理如图所示。该电池工作时,电池左边的电极发生的电极反应式为______________________________。
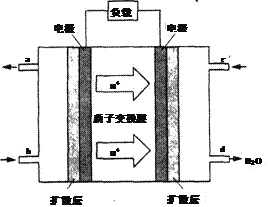
(6)用甲醇燃料电池作为直流电源,设计如图装置制取Cu2O,电解总反应为:2Cu+H2O=Cu2O+H2↑。写出铜电极的电极反应式_______________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃、101 kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是( )
A. 2H2(g)+O2(g) == 2H2O(1) △H= ―285.8kJ/mol![]()
B. 2H2(g)+ O2(g) == 2H2O(1) △H= +571.6 kJ/mol
C. 2H2(g)+O2(g) == 2H2O(g) △H= ―571.6 kJ/mol
D. H2(g)+1/2O2(g) == H2O(1) △H= ―285.8kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一) A、B、C、D为中学常见物质且均含有同一种元素,相互转化关系如图(反应条件及其他物质已经略去):
![]()
(1)若A、B、C、D均为化合物,而且它们的水溶液均能使湿润的蓝色石蕊试纸变红,则D的化学式为________,写出B→C的化学反应方程式:____________。
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使湿润的蓝色石蕊试纸变红。则D的化学式为__________________。写出A→B的化学反应方程式:_______。
(3)若A为单质,组成元素的原子所含质子的数目小于18,D为强碱,则B的化学式:________________。
(二)(1)肼(N2H4)和NO2是一种双组分火箭推进剂。两种物质混合发生反应生成N2和H2O(g),已知8g气体肼在上述反应中放出142kJ热量,其热化学方程式为______________ 。
(2)0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,其热化学反应方程式为__________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新旧动能转换工程之一是新能源新材料的挖掘和应用。乙二醇是重要的化工原料, 煤基合成气(CO、 H2)间接制乙二醇具有转化率高、回收率高等优点,是我国一项拥有自主知识产权的世界首创技术,制备过程如下:
反应 I: 4NO(g)+4CH3OH(g)+O2(g) ![]() 4CH3ONO(g)+2H2O(g) △H1 = a kJ·mol-1
4CH3ONO(g)+2H2O(g) △H1 = a kJ·mol-1
反应 II: 2CO(g)+2CH3ONO(g) ![]() CH3OOCCOOCH3(l) + 2NO(g) △H2= b kJ·mol-1
CH3OOCCOOCH3(l) + 2NO(g) △H2= b kJ·mol-1
反应 III: CH3OOCCOOCH3(1)+4H2(g) ![]() HOCH2CH2OH(1)+2CH3OH(g) △H3= c kJ·mol-1
HOCH2CH2OH(1)+2CH3OH(g) △H3= c kJ·mol-1
(1)请写出煤基合成气[n(CO): n(H2)= 1:2]与氧气间接合成乙二醇的总热化学方程式________,已知该反应在较低温条件下能自发进行,则该反应的△H ____0(填“>”“<”或“=”)。
(2)一定温度下,在 2 L 的密闭容器中投入物质的量均为 0.4mol的CO 和 CH3ONO发生反应 II,10min 达到平衡时CO的体积分数与NO的体积分数相等。
①下列选项能判断反应已达到化学平衡状态的是________。
a. CO 的质量不再变化 b. 混合气体的密度不再变化
c.单位时间内生成 CO 和 NO 的物质的量相等 d. CO 和 CH3ONO 的浓度比不再变化
②10min 内该反应的速率 ν(NO)=____________;该温度下化学平衡常数 K=_________。若此时向容器中再通入0.4 mol NO,一段时间后,达到新平衡时 NO的体积分数与原平衡时相比______(填“增大”“相等”“减小”或“不能确定”)。
③若该反应△H<0,在恒容的密闭容器中,反应达平衡后,改变某一条件,下列示意图正确的是____________(填字母)。
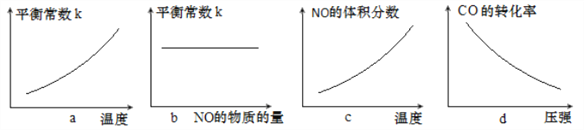
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素 W、X、Y、Z的原子序数依次增大,WX2 为红棕色气体,Y的单质既能与强酸又能与强碱反应,W、Z 最外层电子数之和是X最外层电子数的2 倍。下列说法中错误的是
A. Y 与X、Y与Z均形成离子化合物
B. 对应简单离子的半径:W>X>Y
C. Z 对应的最高价含氧酸是一元强酸
D. ZX2 是一种消毒能力强于氯气且更加安全的自来水消毒剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com