
【题目】在智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘,其化学方程式是2NaIO3+5NaHSO3===3NaHSO4+2Na2SO4+I2+H2O
(1)反应中______元素被氧化,_______是氧化剂。
(2)用“双线桥”标出电子转移的方向和数目。_________。
(3)反应产物中,氧化产物与还原产物的物质的量之比为__________。
【答案】S NaIO3 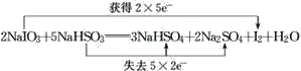 5∶1
5∶1
【解析】
(1)根据氧化剂:化合价降低,得电子,被还原;还原剂:化合价升高,失电子,被氧化判断;
(2)双线桥法注意箭头方向由氧化剂指向还原产物,还原剂指向氧化产物,在箭头上方标出得失电子数;
(3)根据还原剂生成氧化产物,氧化剂生成还原产物,确定氧化产物和还原产物,再根据方程式判断物质的量之比。
(1)结合方程式中元素化合价发生的变化可知,NaIO3中碘元素化合价降低,作氧化剂,被还原为I2;硫元素化合价升高,被氧化为NaHSO4和Na2SO4;
答案:S ;NaIO3
(2)结合各物质的化学计量数计算转移的电子数目,标注电子转移,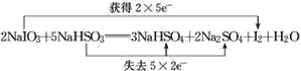 ;
;
答案:
(3)氧化产物为NaHSO4和Na2SO4共5 mol,还原产物为1 mol I2,氧化产物与还原产物的物质的量之比为5∶1;
答案:5∶1


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】在一定温度和压强的密闭容器中,将平均分子质量为8.5的N2和H2混合,随后在一定条件下合成氨,当反应达到平衡时测得混合气体的平均分子质量为10。
(1)反应前N2和H2的体积比为_____;
(2)氮气的平衡转化率;_____________
(3)平衡混合气中氨气的体积分数。_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O,以下叙述正确的是( )
5NaCl+NaClO3+3H2O,以下叙述正确的是( )
A.Cl2是氧化剂,NaOH是还原剂
B.被氧化的氯原子和被还原的氯原子的物质的量之比为5∶1
C.Cl2既做氧化剂又做还原剂
D.氧化剂得电子数与还原剂失电子数之比为5∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学平衡原理在工农业生产中发挥着重要的指导作用。
(1)反应C(s)+CO2(g)![]() 2CO(g)平衡常数K的表达式:K=___;
2CO(g)平衡常数K的表达式:K=___;
(2)已知某温度下,反应2SO2(g)+O2(g)![]() 2SO3(g),的平衡常数K=19。在该温度下的体积固定的密闭容器中充入c(SO2)=1mol·L-1,c(O2)=1 mol·L-1,当反应在该温度下SO2转化率为80%时,该反应___(填“是”或“否”)达到化学平衡状态,若未达到,向___(填“正反应”或“逆反应”) 方向进行。
2SO3(g),的平衡常数K=19。在该温度下的体积固定的密闭容器中充入c(SO2)=1mol·L-1,c(O2)=1 mol·L-1,当反应在该温度下SO2转化率为80%时,该反应___(填“是”或“否”)达到化学平衡状态,若未达到,向___(填“正反应”或“逆反应”) 方向进行。
(3)对于可逆反应:aA(g) +bB(g)![]() cC(g)+dD(g) △H = m kJ·mol-1;若a+b>c+d,增大压强平衡向___(填“正反应”或“逆反应”)方向移动;若升高温度,平衡向逆反应方向移动,则m___0(填“>”或“<”)
cC(g)+dD(g) △H = m kJ·mol-1;若a+b>c+d,增大压强平衡向___(填“正反应”或“逆反应”)方向移动;若升高温度,平衡向逆反应方向移动,则m___0(填“>”或“<”)
(4)在一定条件下,A气体与B气体反应生成C气体。反应过程中,反应物与生成物的浓度随时间变化的曲线如图,则
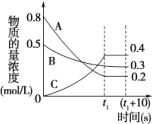
①该反应的化学方程式为:___;
②t1s时反应物A的转化率为:___;
③0~t1s内A的反应速率为v(A)=___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中,ΔH的绝对值表示可燃物的燃烧热的是( ).
A.H2(g)+F2(g)=2HF(g) ΔH=-270 kJ/mol
B.CH4(g)+2O2(g)= CO2(g)+2H2O(g) ΔH=-802.3 kJ/mol
C.2H2(g)+O2(g)= 2H2O(l) ΔH=-571.6 kJ/mol
D.CO(g)+![]() O2(g)= CO2(g) ΔH=-283 kJ/mol
O2(g)= CO2(g) ΔH=-283 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】S2O82-具有强氧化性,其还原产物为SO42-,硫酸锰(MnSO4)和过硫酸钾(K2S2O8)两种盐溶液在银离子催化下可发生反应,得到紫红色溶液。请写出此反应的化学方程式:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法中正确的是( )
A.0.2 mol氧原子中含1.6NA个电子
B.1 mol 氯化镁中含有离子数为NA
C.12.4 g白磷中含有磷原子数为0.1NA
D.28 g一氧化碳气体所含的电子数为20NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用KMnO4氧化盐酸溶液,反应方程式如2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O,若产生的Cl2在标准状况下体积为56 L,计算:
(1)参加反应的HCl的物质的量________________
(2)反应中被氧化的HCl的物质的量__________________
(3)并用双线桥标出电子转移的方向和数目___________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向25ml氢氧化钠标准溶液中逐滴加入0.2mol·L1的一元酸HA溶液,PH变化曲线如下图所示:
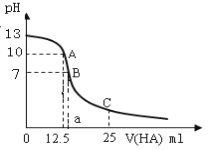
(1)该氢氧化钠溶液的物质的量浓度为__________mol·L1。
(2)A点对应酸的体积为12.5ml,则所得混合溶液中由水电离出的c(OH)= _______mol·L1。
(3)HA是____酸(选填“强”、“弱”)。
(4) 在B点所得混合溶液中,c(Na+)、c(A)、c(H+)、c(OH) 的大小的顺序是_____________。
(5)在C点所得混合溶液中,下列说正确的是________。
A.HA的电离程度小于NaA的水解程度
B.离子浓度由大到小的顺序是c(Na+)>c(A)>c(H+)>c(OH)
C.c(Na+) + c(H+) = c(A-) + c(OH)
D.c(HA) + c(A) = 0.2mol·L1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com