
【题目】除去Na2CO3 固体中少量NaHCO3的最佳方法是
A.加入适量盐酸 B.加热 C.加入NaOH溶液 D.配成溶液后通入CO2
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】硫是一种生命元素,组成某些蛋白质时离不开它。SO2是硫的一种重要氧化物,为探究SO2的性质,某化学兴趣小组的同学进行如下系列实验:
(1)将SO2通入紫色石蕊试液,现象是_________________。
(2)将SO2通入FeCl3溶液中,使其充分反应。写出SO2与FeCl3反应的离子方程式___________________;为了验证SO2与FeCl3发生了氧化还原反应,将反应后的溶液分成两份,并设计如下实验:
方案1:往第一份试液中加入少量酸性KMnO4溶液,紫红色褪去;
方案2:往第二份试液中加入KSCN溶液,不变红,再加入新制氯水,溶液变红。
上述方案合理的是__________。(填“方案1”或“方案2”或“均合理”)
(3)将SO2通入到BaCl2溶液中,出现了异常现象,看到了明显的白色沉淀。为探究该白色沉淀的成分,他们设计了如下实验流程:

操作①的名称为_____,试剂A为_______:加入试剂A后,白色沉淀未见溶解,则该白色沉淀的成分是_______(填化学式)。
(4)为探究SO2的漂白是SO2直接作用于有色物质还是SO2与水反应的产物的作用。设计如图装置进行探究。
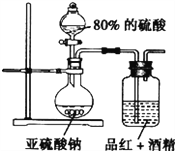
(信息提示:品红能溶解在酒精中形成红色溶液;H2SO3是二元弱酸)
①亚硫酸钠和浓硫酸反应的化学方程式为__________。
②请指出设计的装置中两个明显的不足:
___________________;________________________。
③按照修改后的装置,实验中控制SO2以较缓慢的速率通过品红的酒精溶液,60分钟后溶液仍不褪色,由此可推断,引起品红褪色的微粒可能是______________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合金贮氢材料具有优异的吸放氢性能,在配合氢能的开发中起到重要作用。
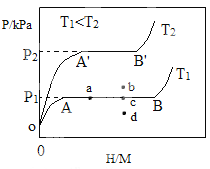
(1)一定温度下,某贮氢合金(M)的贮氢过程如图所示,纵轴为平衡时氢气的压强(p),横轴表示固相中氢原子与金属原子的个数比(H/M)。在OA段,氢溶解于M中形成固溶体MHx,随着氢气压强的增大,H/M逐惭增大;在AB段,MH与氢气发生氢化反应生成氢化物MHy,氢化反应方程式为:zMHx(s)+H2(g)![]() zMHy(s) △H1(I);B点,氢化反应结束,进一步增大氢气压强,H/M几乎不变。
zMHy(s) △H1(I);B点,氢化反应结束,进一步增大氢气压强,H/M几乎不变。
反应(I)的焓变△HⅠ_______0(填“>”“<”或“=”)。
反应(I)中z=___________(用含x和y的代数式表示)。
温度为T1时,2g某合金4min内吸收氢气240mL,吸氢速率v=________mLg1min1。
(2)当反应(I)处于图中a点时,保持温度不变,向恒容体系中通入少量氢气,达到平衡后反应(I)可能处于图中的_______点(填“b”“c”或“d”),该贮氢合金可通过______或_______的方式释放氢气。η表示单位质量贮氢合金在氢化反应阶段的最大吸氢量占其总吸氢量的比例,则温度为T1、T2时,η(T1)___ _______η(T2)(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最大。
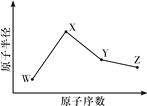
(1)X位于元素周期表中的位置是____________________。
(2)Z的气态氢化物和溴化氢相比,较稳定的是____________(写化学式)。
(3)W与X形成的一种化合物和水反应能生成W的单质,请写出该反应的化学方程式:________________________________________________________________________。
(4)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质。以下叙述正确的是
A.植物油不能使溴的四氯化碳溶液褪色
B.葡萄糖能发生氧化反应和水解反应
C.麦芽糖水解的最终产物是葡萄糖
D.蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对制取水泥和玻璃的共同特点的叙述中,错误的是
A. 生产设备相同 B. 原料中均有石灰石
C. 反应都在高温下进行 D. 发生的都是复杂的物理化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里用二氧化锰和浓盐酸加热制取氯气;
(1)该反应的离子方程式为____________________________。
根据反应原理,图乙中合适的气体发生装置为 ______ 。
(2)也可以利用反应2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O制取并收集纯净、干燥的氯气,部分装置如图甲所示。
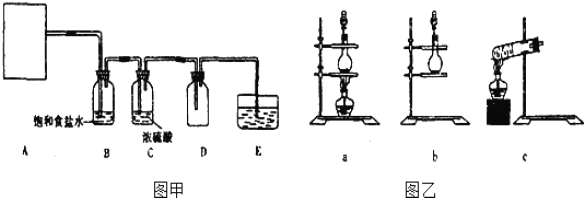
根据反应原理,图乙中合适的制气装置为 ______ 。
(3)装置B的作用是 ______ 。
(4)装置E的作用是 ______,E中的试剂可选 ______ 。
A.NaOH溶液 B.NaCl溶液 C.澄清石灰水 D.水
(5)某同学通过下列两种方式制取氯气:
①用8.7g MnO2与足量浓盐酸反应;
②用含14.6g HCl的浓盐酸与足量MnO2反应这两种方式产生Cl2的量的关系是 ______。
A.①多 B.②多 C.一样多 D.不确定.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学实验能够获得成功的是( )
A. 只用溴水为试剂, 可以将苯、乙醇、己烯、四氯化碳四种液体区分开来。
B. 将无水乙醇加热到 170℃时, 可以制得乙烯
C. 苯酚和福尔马林在沸水浴中加热可以制取酚醛树脂
D. 乙醇、冰醋酸和 2 mol/L 的硫酸混合物, 加热可以制备乙酸乙酯。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的叙述符合事实的是
A. 乙烯使溴水和酸性高锰酸钾溶液褪色的反应都属于氧化反应
B. 乙酸和乙醇均能与NaOH溶液发生反应
C. 苯与溴水混合后加入FeBr3做催化剂,可发生取代反应生成溴苯
D. C5H11Br有8种同分异构体,它们的熔点、沸点各不相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com