
海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
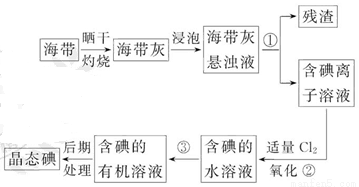
(1)步骤①的实验操作名称是_________;
(2)现有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品。完成该实验尚缺少的玻璃仪器是_________;
(3)步骤③中能选用CCl4从碘水中萃取碘的原因是_________;
A.CCl4与水不互溶
B.CCl4可与I2发生取代反应
C.CCl4的密度比水大
D.CCl4不易燃烧,可作灭火剂
E.碘在CCl4中的溶解度比在水中大很多
(4)步骤③中还可选择_________作萃取剂;
(5)步骤②中反应的离子方程式是__________________________________;
(6)请设计一种简单的实验方法,检验提取碘后的水溶液中是否还含有单质碘:_________。
(1)过滤 (2)漏斗、分液漏斗
(3)A、E (4)苯 (5)Cl2+2I-=2Cl-+I2
(6)取少量待测液注入试管中,滴加淀粉溶液,若溶液变蓝色,说明水溶液中存在I2,否则水溶液中无I2
【解析】(1)分离难溶性物质与溶液的方法是过滤。
(2)根据实验流程图可以看出,完成实验需要经过灼烧、浸泡、过滤、氧化、萃取、分液、蒸发等步骤,由此可以判断出实验尚缺少的玻璃仪器是漏斗和分液漏斗。
(3)萃取剂需要满足的条件是:①与原溶剂互不相溶;
②溶质在萃取剂中的溶解度大于在原溶剂中的溶解度且不与萃取剂反应,CCl4符合萃取剂的选择条件。
(4)检验水溶液中是否含有单质碘的试剂是淀粉溶液,看两种溶液相遇是否变蓝来确定是否含有单质碘。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2014年化学高考总复习单元检测 第五章物质结构、元素周期律练习卷(解析版) 题型:选择题
同一主族的两种元素的原子序数之差不可能是( )
A.16 B.26 C.36 D.46
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习单元检测 第九章电化学基础练习卷(解析版) 题型:选择题
能够使反应Cu+2H2O=Cu(OH)2+H2↑发生的是( )
A.铜片作原电池的负极,碳棒作原电池的正极,氯化钠作电解质溶液
B.铜锌合金在潮湿的空气中发生电化学腐蚀
C.用铜片作阴、阳电极,电解硫酸钠水溶液
D.用铜片作阴、阳电极,电解硫酸铜水溶液
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习单元检测 第三章金属及其化合物练习卷(解析版) 题型:选择题
.化学反应经常伴随着颜色变化,下列有关反应显示的颜色正确的有( )
①氢氧化亚铁在空气中最终变为灰绿色;
②淀粉溶液遇单质碘变为蓝色;
③向硫酸铁溶液中加入KSCN溶液变为红色;
④新制氯水久置后变为无色;
⑤无水硫酸铜吸收水蒸气变成浅绿色;
⑥品红溶液通入过量二氧化硫后褪色。
A.2个 B.3个 C.4个 D.5个
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习单元检测 第三章金属及其化合物练习卷(解析版) 题型:选择题
下列有关金属的说法中正确的是( )
①在人类对金属材料的使用过程中,性质活泼的金属单质最早被人们冶炼和使用
②纯铁比生铁抗腐蚀性更强
③单质铝在空气中比较耐腐蚀,所以铝是不活泼金属
④正常人体缺钙会引起骨质疏松症,缺铁会引起贫血等疾病
⑤青铜、不锈钢、硬铝都是合金
⑥可通过焰色反应区分钾元素和钠元素
A.②④⑤⑥ B.②③④⑤ C.①③④⑤ D.①②⑤⑥
查看答案和解析>>
科目:高中化学 来源:2014年化学高考复习演练4-5海水资源利用环境保护绿色化学练习卷(解析版) 题型:选择题
化学在人类生活中扮演着重要角色,以下应用正确的是( )
A.用浸泡过高锰酸钾溶液的硅土吸收水果释放的乙烯,可达到水果保鲜的目的
B.为改善食物的色、香、味并防止变质,可在其中加入大量食品添加剂
C.使用无磷洗衣粉,可彻底解决水体富营养化问题
D.天然药物无任何毒副作用,可长期服用
查看答案和解析>>
科目:高中化学 来源:2014学年高二鲁科选修3化学训练1.2.1基态原子核外电子排布练习卷(解析版) 题型:选择题
某元素有6个电子处于n=3、l=2的能级上,根据洪特规则推测它在d轨道上未成对电子数为( )。
A.3 B.4 C.5 D.2
查看答案和解析>>
科目:高中化学 来源:2014学年高二鲁科选修3化学规范训练1.1.2原子核外电子运动练习卷(解析版) 题型:选择题
下列符号表示的轨道中具有球对称性的是( )。
A.7s B.4f C.5d D.3p
查看答案和解析>>
科目:高中化学 来源:2014学年高一化学人教版必修2 2.3.2反应限度条件的控制练习卷(解析版) 题型:填空题
在2 L密闭容器内,800 ℃时反应2NO(g)+O2(g)  2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)下图表示NO2的变化的曲线是________。用O2表示从0~2 s内该反应的平均速率v=________。
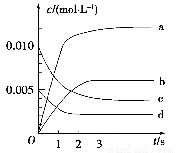
(2)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(3)为使该反应的反应速率增大,下列措施正确的是________。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com