
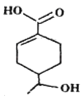
【题目】某有机物的结构简式如图所示,下列有关该有机物的说法正确的是
A.分子中含有四种官能团
B.1mol该有机物完全燃烧消耗O2的物质的量为10mol
C.能发生加成、取代、水解等反应
D.相同条件下,等量的该有机物分别与足量的Na和NaHCO3溶液反应产生的气体的量相同
【答案】D
【解析】
分析该有机物结构可知,该有机物含碳碳双键、羟基和羧基,有3个不饱和度,分子式为C9H14O3,可在此认识基础上对各选项作出判断。
A. 根据分析可知,该有机物含碳碳双键、羟基和羧基三种官能团,A选项错误;
B. 该有机物分子式为C9H14O3,完全燃烧消耗O2的物质的量为:(9+![]() -
-![]() )mol=11mol,B选项错误;
)mol=11mol,B选项错误;
C. 碳碳双键能发生加成反应,羟基和羧基等能发生取代反应,但没有能发生水解反应的结构,C选项错误;
D. -COOH和-OH能和Na反应产生H2,每摩尔有机物和Na反应产生1mol H2;-COOH能和NaHCO3反应生成CO2,每摩尔有机物和NaHCO3反应产生1molCO2;所以相同条件下,等量的该有机物分别与足量的Na和NaHCO3溶液反应产生的气体的量相同,D选项正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】一定温度下,某恒容容器内的可逆反应A(气)+3B(气)![]() 2C(气)。下列说法正确的是
2C(气)。下列说法正确的是
A.当反应进行到混合气体密度不变时,达化学平衡状态
B.当B的生成速率是A的消耗速率的3倍时,反应达化学平衡状态
C.向容器内充入氦气致使压强增大,化学反应速率加快
D.当反应达平衡后,若改变某一外界条件引起速率发生变化,平衡一定会发生移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,有关物质的电离平衡常数如下:

(1)电解质由强至弱顺序为___(用化学式表示,下同)。
(2)常温下,0.02mol·L-1的CH3COOH溶液的电离度约为___,体积为10 mL pH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者___后者(填“>”、“<”或“=”)。
(3)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的顺序为_____。
(4)NaHSO3溶液显酸性的原因_____(离子方程式配适当文字叙述),其溶液中离子浓度由大到小的关系是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸铝(AlPO4)是一种用途广泛的材料,可在玻璃生产过程中充当助熔剂,作陶瓷或牙齿的黏合剂等。以磷硅渣[主要成分为Ca3(PO4)2、Al2O3、SiO2和V2O5等]为原料制备磷酸铝的工艺流程如图所示:

请回答下列问题:
(1)浸渣中含有SiO2,试写出SiO2的一种重要用途__;酸浸中磷元素主要转化为H3PO4,该反应的化学方程式为__。
(2)生石灰除了调节pH外,另一作用是__。
(3)滤液中钒元素以V3O93-形式存在,V3O93-易水解为[VO3(OH)]2-,该水解反应的离子方程式为__。
(4)碱浸时,粗磷酸铝转化为可溶性溶质,则可溶性溶质分别是__(填化学式)。
(5)实验测得pH、反应温度与时间对碱浸时固相中P、Al含量w%的影响如图所示:

则最优反应条件是__。
(6)在物质的量浓度分别为0.01mol·L-1的CaCl2和AlCl3的混合溶液中加入等体积的Na3PO4溶液,若A13+恰好沉淀完全,即溶液中c(A13+)=1.0×10-5mol·L-1,此时AlPO4沉淀中__(填“是”或“否”)混有Ca3(PO4)2。[已知AlPO4、Ca3(PO4)2的Ksp分别为6.3×10-19、2.0×10-29]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.常温常压下,30g乙烷气体中所含有的共价键数目为7NA
B.1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去2NA个电子
C.0.5mol雄黄(As4S4,结构为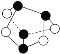 )中含有NA个S—S键
)中含有NA个S—S键
D.6.0gSiO2晶体中含有的分子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫氰化钾可用于农药、医药、电镀、化学试剂、检定铁离子、铜和银等。某兴趣小组同学在实验室模拟工业制备硫氰化钾(KSCN),实验装置如图所示。
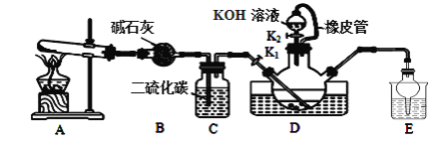
实验步骤如下:
(1)制备NH4SCN溶液:CS2+2NH3![]() NH4SCN+H2S,该反应进行的比较缓慢,NH3不溶于CS2。
NH4SCN+H2S,该反应进行的比较缓慢,NH3不溶于CS2。
①实验前,应进行的操作是__;三颈烧瓶内盛放有一定量的CS2、水和催化剂。三颈烧瓶的下层CS2液体必须浸没导气管口,目的是__。
②实验开始时打开K1,加热装置A、D,缓慢地向装置D中充入气体。装置A中发生反应的化学方程式是__,装置C的作用可能是__。
(2)制备KSCN溶液:移去装置A处的酒精灯,关闭K1,打开K2,利用耐碱分液漏斗边加液边加热,则此时装置D中发生反应的化学方程式是__。
(3)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,再减压蒸发浓缩,冷却结晶,___,得到硫氰化钾晶体。
(4)测定KSCN的含量:称取10.00g样品配成1000mL溶液,量取25.00mL溶液于锥形瓶中,并加入几滴Fe(NO3)3溶液,用0.1000mol·L-1AgNO3标准溶液滴定。经过3次平行试验,达到滴定终点时,消耗AgNO3标准溶液的体积平均为20.00mL。滴定反应的离子方程式为SCN-+Ag+=AgSCN↓。
①判断达到滴定终点的方法是__。
②样品中KSCN的质量分数为__(KSCN的摩尔质量为97g·mol-1,保留4位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】周期表中的五种元素A、B、D、E、F,原子序数依次增大,A的基态原子价层电子排布为nsnnpn;B的基态原子2p能级有3个单电子;D是一种富集在海水中的元素,含量位于海水中各元素的第三位;E2+的3d轨道中有10个电子;F位于第六周期,与Cu同族,其单质在金属活动性顺序表中排在末位。
(1)写出E的基态原子的价层电子排布式___________。
(2)A、B形成的AB﹣常作为配位化合物中的配体,其A原子的杂化方式为________,AB﹣中含有的σ键与π键的数目之比为________。
(3)FD3是一种褐红色晶体,吸湿性极强,易溶于水和乙醇,无论是固态、还是气态,它都是以二聚体F2D6的形式存在,依据以上信息判断FD3,晶体的结构属于____晶体,写出F2D6的结构式________。
(4)E、F均能与AB﹣形成配离子,已知E与AB﹣形成的配离子为正四面体形。F(+1价)与AB形成的配离子为直线形,工业上常用F和AB﹣形成的配离子与E反应来提取F单质,写出E置换F的离子方程式_________________。
(5)F单质的晶体为面心立方最密堆积,若F的原子半径为a nm,F单质的摩尔的的质量为Mg/mol,阿伏加德罗常数为NA,求F单质的密度为______g/cm3。(用a、NA、M的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列各组物质:①![]() 和
和![]() ;②石墨和金刚石;③漂白粉和漂白液主要成分;④正丁烷和异庚烷;⑤乙烯和甲烷;⑥
;②石墨和金刚石;③漂白粉和漂白液主要成分;④正丁烷和异庚烷;⑤乙烯和甲烷;⑥![]() 和
和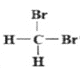 ;⑦丙烷和环丙烷; ⑧CH3-CH2-CH2-CH3 和CH3-CH(CH3)CH3。用序号填空:
;⑦丙烷和环丙烷; ⑧CH3-CH2-CH2-CH3 和CH3-CH(CH3)CH3。用序号填空:
(1)____________组两者互为同位素。
(2)____________组两者互为同素异形体。
(3)____________组两者属于同系物。
(4)____________组两者互为同分异构体。
(5)____________组两者是同一物质。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近科学家获得了一种稳定性好、抗氧化能力强的活性化合物A;其结构如下:

为了研究X的结构,将化合物A在一定条件下水解只得到 和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
请回答下列问题:
(1)化合物B能发生下列哪些类型的反应________。
A.取代反应 B.加成反应
C.缩聚反应 D.氧化反应
(2)写出化合物C所有可能的结构简式______________________________。
(3)C可通过下图所示途径合成,并制取冬青油和阿司匹林。

(ⅰ)写出有机物的结构简式:D:______________,C:________________,E:______________。
(ⅱ)写出变化过程中①、⑥的化学方程式(注明反应条件)
反应①__________________________________;反应⑥_____________________________。
(ⅲ)变化过程中的②属于____________反应,⑦属于________反应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com