
【题目】TiCl4是制备钛及其化合物的重要中间体,可利用下列装置在实验室制备TiCl4(夹持装置略去): TiO2+2C+2Cl2![]() TiCl4+2CO
TiCl4+2CO
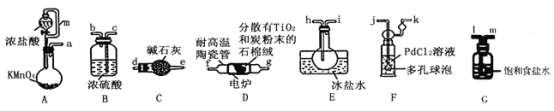
已知:①PdCl2溶液捕获CO时生成Pd单质;②相关数据如下表:
化合物 | 熔点/℃ | 沸点/℃ | 密度/gcm-3 | 溶解性 |
TiCl4 | -25 | 136 | 1.5 | 能溶于有机溶剂:遇水分解生成难溶于水的物质 |
CCl4 | -23 | 76.8 | 1.6 | 难溶于水 |
回答下列问题:
(1)装置A中连通管的作用是______;装置E中使用冰盐水浴的目的是_____________________。
(2)按照气流由左到右的方向,上述装置合理的连接顺序为____________________ (填仪器接口字母);根据完整的实验装置进行实验,实验步骤如下:_____________; 装入药品;向装置A烧瓶中滴加适量浓盐酸,当观察到_________时,加热装置D中陶瓷管;装置E烧瓶中的液体量不再增加时,停止加热,充分冷却。
(3)装置C的作用为___________________。
(4)装置F中发生反应的化学方程式为________________________。
(5)制得的TiCl4中常含有少量CCl4, 从混合液体中分离出TiCl4的操作名称为_______________。
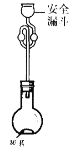
(6)利用如图所示装置测定产品纯度:称取w g TiCl4产品进行实验,向安全漏斗中加入适量蒸馏水,待四氯化钛充分反应后,将烧瓶和安全漏斗中的液体一并转入锥形瓶中,用氢氧化钠溶液调节至中性,滴加几滴0.1 molL-1的K2CrO4溶液作指示剂,用cmol L-1 AgNO3标准溶液滴定至终点( Ag2CrO4为红棕色沉淀,可指示滴定终点),重复滴定两次,平均消耗标准溶液V mL。
已知:TiCl4 +(2+x)H2O=TiO2xH2O↓+4HCl
①安全漏斗在本实验中的作用除加水外,还有___________。
②根据上述数据计算该产品的纯度为__________。(用含w、c和V的代数式表示)
【答案】平衡压强,使浓盐酸更易滴落 降温、冷凝,收集产品TiCl4 almcbfghidej 检查装置的气密性 装置充满氯气 防止水蒸气进入E装置,同时吸收未参加反应的氯气,防止氯气污染空气 PdCl2+CO+H2O=Pd+CO2+2HCl 蒸馏 形成液封,吸收多余的HCl,避免HCl损失 ![]() %
%
【解析】
A中有KMnO4与浓盐酸制备Cl2,通过G装置净化除去HCl,再经B装置的浓硫酸干燥,进入D装置与TiO2和C反应制备TiCl4,在E中冷凝收集产品TiCl4,为防止产品有水进入E装置,连接C装置,最后在F装置收集生成的不溶于水的CO。
(1)A中有气体生成,容易造成A中气压增大,分液漏斗液体不易顺利滴下,E装置收集产品TiCl4,据此分析;
(2)根据A装置制备Cl2,G装置除去HCl,B装置干燥,D装置制备TiCl4,C装置防止水蒸气进入收集装置,E收集产品TiCl4,F装置收集CO分析有气体参加的反应首先要检查装置的气密性,然后加入药品,制取气体,待装置充满氯气时,进行氯气与TiO2的反应TiCl4;
(3)根据防止产品水解和保持产品干燥及氯气的性质的角度分析;
(4)装置F中进行PdCl2溶液捕获CO时生成Pd单质和两种酸性气体;
(5)根据TiCl4、CCl4的沸点差异分析。
(6)根据安全漏斗的气密性分析仪器的作用,结合Ag++Cl-=AgCl↓即Cl元素守恒计算。
(1)装置A中导管m的作用是:平衡压强,使浓盐酸更易滴落;冰水混合物可起到降温、冷凝,收集产品TiCl4的作用;
(2)A装置制备Cl2,G装置除去Cl2中混有的杂质HCl,B装置干燥,为干燥彻底,导气管长进短出,D装置制备TiCl4,E装置收集,C装置防止水蒸气进入收集装置,除去氯气,F装置收集CO,故按照气流由左到右的方向,上述装置仪器接口字母的连接顺序为almcbfghidej;根据完整的实验装置进行实验,实验步骤如下:检查装置的气密性; 装入药品;向装置A烧瓶中滴加适量浓盐酸,当观察到装置充满氯气时,加热装置D中陶瓷管;装置E烧瓶中的液体量不再增加时,停止加热,充分冷却。
(3)E中装置C的作用是防止水蒸气进入E装置,同时吸收未参加反应的氯气,防止氯气污染空气;
(4)装置F中CO与PdCl2、H2O发生反应产生Pd、CO2、HCl,发生反应的化学方程式为PdCl2+CO+H2O=Pd+CO2+2HCl;
(5)已知:TiCl4的沸点为136℃,CCl4的沸点为76.8℃,可采用蒸馏方法分离出TiCl4;
(6)①安全漏斗在本实验中的作用除加水外,还可以形成液封,吸收多余的HCl,避免HCl损失;
②产品与水充分反应得到HCl的水溶液,加入K2CrO4溶液作指示剂,用cmol/LAgNO3溶液滴定,当观察到白色沉淀刚刚出现砖红色沉淀时达到滴定终点,则有:
TiCl4~4HCl~4AgCl~4AgNO3,故n(TiCl4)=![]() n(AgNO3),所以产品纯度为
n(AgNO3),所以产品纯度为 ×100%=
×100%=![]() %。
%。


科目:高中化学 来源: 题型:
【题目】(1)观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题。
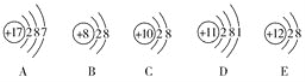
①与离子相对应的元素符号是______________,与原子相对应的离子的结构示意图是______________。
②电子层结构相同的是__________(填写代号,下同),性质最稳定的是__________,最容易失去电子的是__________,最容易得到电子的是__________。
③可直接相互结合形成的化合物的化学式是____________。可经过得失电子后再相互结合形成的化合物的化学式是______________。
④在核电荷数1~10的元素内,列举两个与B电子层结构相同的离子,写出离子的符号______________。
(2)已知元素X和Y的核电荷数均小于18,最外层电子数分别为n和(m-5),次外层有(n+2)个和m个电子,据此推断元素X和Y,其名称为X__________,Y__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒(Se)是人体健康必需的一种微量元素,已知Se的原子结构示意图如图:下列说法不正确的是

A. 该原子的质量数为34
B. 该元素处于第四周期第ⅥA族
C. SeO2既有氧化性又有还原性
D. 酸性:H2SO4>H2SeO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有固体单质A和淡黄色固体B都能与C反应生成D,同时A与C反应放出单质气体E,B与C反应放出F,E与F在点燃的条件下可以生成C,请回答下列问题:
⑴写出各物质的化学式:
A: ______ B: ______ C: ______D: ______ E: ______ F: ______
⑵写出下列反应方程式:
A与C反应: ______ B与C反应: ______ E与F反应: ______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示:向饱和![]() 溶液中逐滴加入稀硫酸,不断搅拌至过量。
溶液中逐滴加入稀硫酸,不断搅拌至过量。
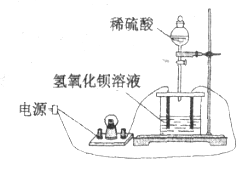
(1)主要的实验现象:烧杯中____________, 灯泡__________________。
(2)烧杯中反应的离子方程式:________________。
(3)下列图示能正确表示实验过程的是___________(填序号)。
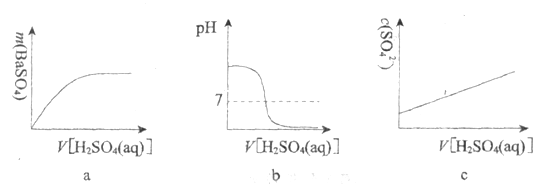
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组为了探究木炭与浓硝酸反应后的气态生成物,设计如下实验。
(1)甲同学设计实验如图甲。
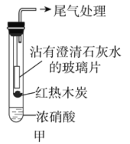
红热木炭未进入试管前,浓硝酸上方并无明显变化。当如图甲连接实验后,浓硝酸液面上方有明显的红棕色气体产生,且沾有澄清石灰水的玻璃片出现浑浊,后浑浊消失。
①液面上方出现红棕色气体,说明浓硝酸具有________(填选项字母)。
a.酸性 b.挥发性 c.不稳定性
②沾有澄清石灰水的玻璃片出现浑浊,________(填“能”或“不能”)说明木炭与浓硝酸发生了反应,是因为________。
(2)乙同学设计实验如图乙。
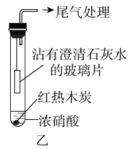
如图乙连接实验后,浓硝酸液面上方有明显的红棕色气体产生,且沾有澄清石灰水的玻璃片无明显变化。沾有澄清石灰水的玻璃片无明显变化,________(填“能”或“不能”)说明木炭与浓硝酸未反应,是因为________。
(3)丙同学克服了甲、乙同学设计上的缺点,设计实验如图丙。已知酸性高锰酸钾能将NO、NO2 氧化成 NO3-,MnO4- 被还原为 Mn2+。
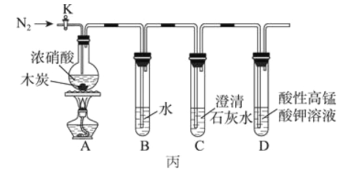
①如图连接装置后,需进行的实验操作为________;加热木炭与浓硝酸前需先通一段时间N2,目的为________________。
②装置A中木炭与浓硝酸反应的化学方程式为_________________________。
③能证明木炭被氧化的实验现象为________________________________________。
④D 装置中发生反应的离子方程式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲同学利用下图所示装置进行硝酸、氮氧化物的相关实验:
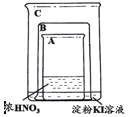
实验1:将铜片放入烧杯A后,立即用烧杯B盖住
(1)烧杯A液体上方出现大量红棕色气体,该反应的化学方程式为_________________
(2)一段时间后,红棕色气体消失,烧杯C中的液体变成蓝色,甲同学分析出现蓝色的原因,认为其中涉及到两个反应:
①红棕色气体消失,该化学方程式为_____________________________________________
②配平溶液出现蓝色的离子方程式,并用单线桥法标出电子转移方向和数目:
________I-+________![]() +________H+=________I2+________NO↑+________H2O
+________H+=________I2+________NO↑+________H2O
(3)打开烧杯B,A液体上方又出现淡棕色,该反应的化学方程式为__________________
实验Ⅱ:因为有其他同学对淀粉KI溶液变蓝的原因提出异议,甲同学将铜片换成铁片放入烧杯A后,立即用烧杯B盖住。
(4)实验前甲同学认为换为铁片后不应出现红棕色气体,淀粉KI溶液不会变为蓝色,其理由是____________________________________________________________________
(5)实验开始后,发现确实无红棕色气体生成,但过一段时间后,淀粉KI溶液仍然变为蓝色,请你帮忙分析其中的原因_________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于实验室制氯气的说法中错误的是( )
A.该反应是一个氧化还原反应,其中二氧化锰是氧化剂
B.每生成1mol氯气,就要转移2mol电子
C.该反应的离子方程式为MnO2+4H++4Cl-![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
D.该方法是瑞典化学家舍勒最先发现的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】菠萝酯F是一种具有菠萝香味的赋香剂,其合成路线如图:
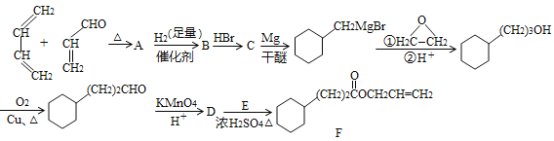
已知:①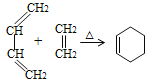
②RMgBr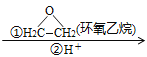 RCH2CH2OH+
RCH2CH2OH+![]()
(1)A中所含官能团![]() 名称是__,B的结构简式为__。
名称是__,B的结构简式为__。
(2)由A生成B的反应类型是__。
(3)写出D和E反应生成F的化学方程式__。
(4)D中含有环己基(只有一个侧键)能发生银镜反应的同分异构体的结构简式为__。
(5)结合题给信息,以乙烯为原料制备1-丁醇,设计合成路线(其他试剂任选)__。
合成路线流程图示例:CH3CHO![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com