
【题目】锂—磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备:2Na3PO4+4CuSO4+2NH3H2O═Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)写出基态Cu2+的电子排布式:____________;与Cu同周期的元素中,与铜原子最外层电子数相等的元素还有____________(填元素符号)。
(2)PO43-的空间构型是____________。
(3)与SO42-互为等电子体的2种分子是______。
(4)氨水溶液中各元素原子的电负性从大到小排列顺序为_______________.
(5)氨基乙酸铜(结构简式:H2NCH2COO-Cu-OOC-CH2NH2)分子中碳原子的杂化方式为____________,基态碳原子核外电子占有_________个轨道。
(6)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则1mol该配合物中含有的π键的物质的量为__________mol。
(7)铜晶体为面心立方最密堆积,配位数为___________,铜的原子半径为127.8pm,NA表示阿伏加德罗常数的值,列出晶体铜的密度计算式(不必化简)__________g/cm-3
【答案】 [Ar]3d9 K、Cr 正四面体 SiF4 、CCl4 、CF4、SiCl4等 O>N>H sp3、sp2 4 8 12 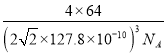
【解析】(1)考查电子排布式的书写、核外电子排布规律,Cu的价电子排布式为3d104s1,即Cu2+电子排布式为[Ar]3d9;与铜原子最外层电子数相等的元素是K、Cr;(2)考查空间构型,PO43-中中心原子有4个σ键,孤电子对数为(5+3-4×2)/2=0,价层电子对数为4,即PO43-的空间构型为正四面体;(3)考查等电子体,与SO42-等电子体的分子有SiF4 、CCl4 、CF4、SiCl4等;(4)考查电负性的规律,氨水中含有的元素是N、H、O,电负性的顺序是O>N>H;(5)考查杂化类型的判断,电子排布式,氨基乙酸铜中-CH2-,该碳原子的杂化类型为sp3,氨基乙酸铜中“C=O”中C原子的杂化类型为sp2;基态C原子的电子排布式为1s22s22p2,一个p能级有3个原子轨道,1个s能级有1个原子轨道,即基态碳原子核外电子占有4个原子轨道;(6)考查化学键的数目,CN-中C和N共有三个电子对,其中有2个π键,即1mol该配合物中含有π键的物质的量为8mol;(7)考查晶胞的计算,铜晶体为面心立方最密堆积,配位数为12,两个最近的铜原子距离是面对角线的一半,即面对角线距离为4×127.8×10-10cm,根据勾股定理,求出边长为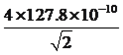 cm,晶胞的体积为(
cm,晶胞的体积为(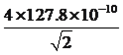 )3cm3,铜原子位于顶点和面心,个数为8×1/8+6×1/2=4,即晶胞的质量为
)3cm3,铜原子位于顶点和面心,个数为8×1/8+6×1/2=4,即晶胞的质量为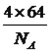 g,根据密度的定义,晶胞的密度为
g,根据密度的定义,晶胞的密度为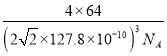 g/cm3。
g/cm3。


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:
【题目】电解质溶液导电能力越强,电导率越大。常温下用0.1000 mol/L 盐酸分别滴定10.00 mL浓度均为0.1000 mol/L的NaOH溶液和二甲胺[ (CH3)2NH]溶液( 二甲胺在水中电离与氨相似,已知在常温下Kb[(CH3)2NH·H2O] =1.6×10-4),利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是
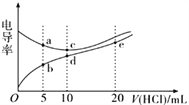
A. 盐酸滴定二甲胺实验中选择酚酞做指示剂比选甲基橙误差更小
B. d点溶液中:c(H+)<c(OH-)+c[(CH3)2NH2+]
C. a 点溶液与d点的溶液混合后的溶液中:c[(CH3)2NH2+]<c[(CH3)2NH·H2O]
D. b、c、e.三点的溶液中,水的电离程度最大的是e点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:①101kPa时,C(s)+ ![]() O2(g)=CO(g)△H1=﹣110.5kJmol﹣1②稀溶液中,H+(aq)+OH﹣(aq)=H2O(l)△H2=﹣57.3kJmol﹣1下列结论正确的是( )
O2(g)=CO(g)△H1=﹣110.5kJmol﹣1②稀溶液中,H+(aq)+OH﹣(aq)=H2O(l)△H2=﹣57.3kJmol﹣1下列结论正确的是( )
A.若碳的燃烧热用△H3来表示,则△H3<△H1
B.若碳的燃烧热用△H3来表示,则△H3>△H1
C.浓硫酸与稀NaOH溶液反应的中和热为﹣57.3 kJmol﹣1
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程.反应过程的示意图如下: 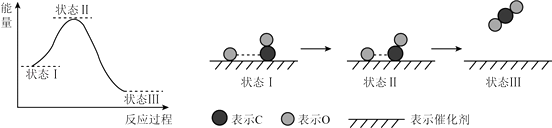
下列说法正确的是( )
A.CO和O生成CO2是吸热反应
B.在该过程中,CO断键形成C和O
C.CO和O生成了具有极性共价键的CO2
D.状态Ⅰ→状态Ⅲ表示CO与O2反应的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有如下两个反应: (A)NaOH+HCl═NaCl+H2O
(B)2FeCl3+Fe═3FeCl2
①根据两反应本质,分别判断能否用于设计原电池 .
②如果不能,说明其原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.10mol/L的盐酸分别滴定体积相同且浓度均为0.10mol/L的三种一元碱XOH、YOH及ZOH,滴定曲线如图所示。

下列说法正确的是
A. 滴定XOH时可用酚酞作指示剂
B. YOH是强碱
C. X++H2O![]() XOH+H+的平衡常数K=10-4
XOH+H+的平衡常数K=10-4
D. [V(盐酸)/V(碱)]=0.5时,c(Z+)>c(Y+)>c(X+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com