
【题目】三氯氧磷(POCl3)常用作半导体掺杂剂及光导纤维原料,实验室制备POCl3并测定产品含量的实验过程如下:
Ⅰ.制备POCl3。
采用氧气氧化液态PCl3法制取POCl3,实验装置(加热及夹持仪器略)如图所示:
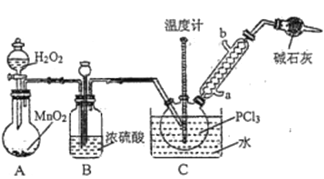
已知:①Ag++SCN-=AgSCN↓;Ksp(AgCl)>Ksp(AgSCN);磷酸银溶于硝酸。
②PCl3和POCl3的相关信息如下表:
物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
PCl3 | -112.0 | 76.0 | 137.5 | 两者互溶,均为无色液体,遇水均剧烈反应生成含氧酸和氯化氢 |
POCl3 | 2.0 | 106.0 | 153.5 |
(1)POCl3遇水反应的化学方程式为_________________________________________。
(2)装置B的作用除干燥O2外,还有_________________________________________。干燥管的作用是_______________。
(3)反应温度要控制在60~65℃,原因是_____________________________________________。
Ⅱ.测定POCl3产品的含量。
实验步骤:
①制备POCl3实验结束后,待三颈烧瓶中的液体冷却至室温,准确称取30.7gPOCl3产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解,将水解液配成100.00mL溶液。
②取10.00mL溶液于锥形瓶中,加入10.00mL3.2mol/LAgNO3标准溶液。
③加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖。
④以X为指示剂,用0.2mol/LKSCN溶液漓定过量的AgNO3溶液,达到滴定终点时共用去10.00mLKSCN溶液。
(4)步骤③中加入硝基苯的作用是___________________________________________。若无此操作,所测产品中氯元素的质量分数将会__________(填“偏大”、“偏小”或“不变”)。
(5)步骤④中X为__________,产品中POCl3的质量分数为____________。
【答案】 POCl3+3H2O=H3PO4+3HCl 平衡压强、观察O2的流速 防止空中的水蒸气进入三颈烧瓶 温度过低,反应速率太慢;温度过高,PCl3易挥发,利用率低 防止在滴加KSCN溶液时,将AgCl沉淀转化为AgSCN沉淀 偏小 Fe(NO3)3 50%
【解析】Ⅰ.(1)POCl3遇水会发生反应,根据原子守恒可知反应的方程式为: POCl3+3H2O=H3PO4+3HCl,答案为:POCl3+3H2O=H3PO4+3HCl
(2)B装置导管和大气相连,则B还有平衡压强、观察O2的流速的作用;POCl3遇水会发生反应,干燥管可以防止空中的水蒸气进入三颈烧瓶与POCl3发生反应。答案为:平衡压强、观察O2的流速;防止空中的水蒸气进入三颈烧瓶
(3)PCl3的沸点为76.0℃,若温度过低,反应速率太慢;温度过高,PCl3易挥发,导致PCl3的利用率低,所以反应温度要控制在60~65℃;答案为:温度过低,反应速率太慢;温度过高,PCl3易挥发,利用率低
Ⅱ.(4) 实验过程中加入硝基苯的目的是覆盖氯化银,防止沉淀转化生成AgSCN沉淀而导致数据不准确。如无此操作,部分AgCl沉淀会转化为Ag+,使所测Cl元素含量将会偏小;答案为:防止在滴加KSCN溶液时,将AgCl沉淀转化为AgSCN沉淀、偏小
(5)由于是用KSCN溶液滴定溶液中过量的Ag+,而Fe(SCN)3 溶液是血红色溶液,所以可用含有Fe3+的Fe(NO3)3溶液作指示剂,当溶液中Ag+反应完全后,再滴加的KSCN溶液就会与溶液中的Fe3+作用,使溶液变为血红色;根据物质的元素组成及关系式可知POCl3~3HCl~3Ag+,n(Ag+)=0.032mol-0.002mol=0.03mol,n(POCl3)=0.01mol,所以三氯氧磷的含量为![]() 答案为:Fe(NO3)3 、50%
答案为:Fe(NO3)3 、50%


 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案科目:高中化学 来源: 题型:
【题目】烃类有机物在生活和生产中发挥着重要作用,研究它们意义重大。请回答下列问题:
(1)写出乙烷制氯乙烷的方程式______________________________,其反应类型为____________。
(2)写出以乙醇为原料经过两步反应制备乙烯的方程式,并指出第二步反应的反应类型。
第一步:__________________________________;
第二步:______________________,其反应类型为___________________。
(3)0.2mol某烃A在氧气中宋个燃烧后,生成CO2利H2O各1.2mol。若烃A不能使溴水褪色,但在一定条化下能与氯气发生取代反应,其一氯取代物有两种,则烃A的结构简式为___________________。
(4)在一定条件下,某些不饱和烃分子可以进行自身加成反应。例如:
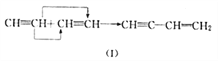
①参照(I)则有机物A![]() ,可由____________(填结构简式)相互加成制取。
,可由____________(填结构简式)相互加成制取。
②参照(I)当两分子丙烯发生自身加成时生成主链为4个碳原子的烃B,则B的结构简式为______,用系统命名法命名B_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】O2、O3、N2、N4是氧和氮元素的几种单质。回答下列问题:
(1)O原子中价电子占据的轨道数目为__________________。
(2)第一电离能I1:N____O(填“>”或“<”),第二电离能I2:O大于N的原因是__________________。
(3)O3的空间构型为_________________;是_____________(填“极性”或“非极性”)分子;分子中存在的大π键,可用符号![]() 表示,其中m表示形成的大π键的原子数,n表示形成的大π键的电子数,则O3中大π键应表示为_______________________。
表示,其中m表示形成的大π键的原子数,n表示形成的大π键的电子数,则O3中大π键应表示为_______________________。
(4)N元素的简单气态氢化物NH3在H2O中溶解度很大,其原因之一是NH3和H2O可以形成分子间氢键,则在氨水中氢键可以表示为H3N…H-N、___________、____________ (任写两种即可)。
(5)已知:如下键能和键长数目。
化学键 | 键长/pm | 键能/ |
N-N | 145 | 193 |
N=N | 125 | 418 |
N | 110 | 946 |
N2和N4都是N元素的单质,其中N4是正面体构型,N原子占据四面体的四个顶点,从键参数角度分析N4分子稳定性远小于N2原因是________________________________________。
(6)Na2O的晶胞结构如下图所示,X表示O2-,Y表示Na+,则O2-的配位数为_______________,该晶胞的原子空间利用率为_______________;(已知该晶胞的棱长为apm,r(Na+)=xpm,r(O2-)=ypm)。
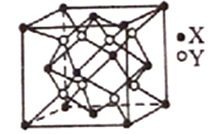
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸乙酯(C9H10O2)是无色透明有水果香气的液体,俗称安息香酸乙酯,常用做溶剂和香料。下列说法正确的是( )
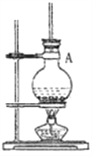
A. 按如图装置制备苯甲酸乙酯,应在烧瓶A中先加入3mL浓H2SO4和4g苯甲酸,然后边振荡烧瓶边慢慢加入10mL乙醇
B. 如图是制备苯甲酸乙酯的简易装置,A中玻璃导管改用球形玲凝管效果更好
C. 制得的苯甲酸乙酯粗产品,可通过水洗、NaOH溶液洗涤、水洗,除去苯甲酸乙酯中的部分杂质
D. 分子式为C9H10O2,含有苯环且能与饱和NaHCO3溶液反应放出气体的有机物共有15种(不含立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下,Ka1(H2CO3)=4.3×10-7,Ka2(H2CO3)=5.6×10-11。某二元酸H2R及其钠盐的溶液中,H2R、HR-、R2-三者的物质的量分数随溶液pH变化关系如图所示,下列叙述错误的是( )

A. 在pH=4.3的溶液中:3c(R2-)=c(Na+)+c(H+)-c(OH-)
B. 等体积、等浓度的NaOH溶液与H2R溶液混合后,此溶液中水的电离程度比纯水小
C. 等浓度的NaOH溶液与H2R溶液按体积比1∶2混合,溶液的pH=1.3
D. 向Na2CO3溶液中加入少量H2R溶液,发生反应:2CO32-+H2R=2HCO3-+R2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铋(Bi)与氮同族,氯氧化铋(BiOCl)广泛用于彩釉调料、塑料助剂、油漆调色、生产金属铋等。一种以用火法炼铜过程产生的铜转炉烟尘(除含铋的化合物之外,还有CuSO4、ZnSO4、CuS、Fe2O3、PbSO4及As2O3)制备高纯氯氧化铋的工艺流程如下:

请回答:
(1)BiOCl中Bi元素的化合价为__________。
(2)向“酸浸”所得“浸液1”中加入Zn粉,主要目的是__________________________。
(3)“浸铜”时,有单质硫生成,其反应的离子方程式为____________________________。
(4)“浸铋”时,温度升高,铋的浸出率降低,其原因为____________________________。
(5)“沉铋”时需控制溶液的pH=3.0,此时BiCl3发生反应的化学方程式为__________。
(6)“除铅、砷”时,可以采用以下两种方法:
①加入改性羟基磷灰石固体(HAP):浸液2与HAP的液固比(L/S)与铅、砷去除率以及后续沉铋量的关系如下表:
L/S | 125∶1 | 50∶1 | 25∶1 | 15∶1 |
Pb2+去除率/% | 84.86 | 94.15 | 95.40 | 96.83 |
As3+去除率/% | 98.79 | 98.92 | 98.34 | 99.05 |
m(沉铋)/g | 2.34 | 2.33 | 2.05 | 1.98 |
实验中应采用的L/S=__________。
②铁盐氧化法:向浸液2中加入Fe2(SO4)3,并调节pH,生成FeAsO4沉淀。当溶液中c(AsO43-)=1×10-9mol/L,且不产生Fe(OH)3沉淀,此时溶液的pH为__________。(已知:1g2=0.3;FeAsO4、Fe(OH)3的Ksp分别为5×10-21、4×10-38。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体重50 kg的健康人含Fe元素约2 g。主要以Fe2+、Fe3+形式存在于人体内。Fe2+易被吸收,给贫血者补充铁,应补充含Fe2+的亚铁盐(如FeSO4)。服用Vc,可使食物中的Fe3+转化为Fe2+。
①人体中经常进行Fe2+![]() Fe3+的转化,在过程A中,Fe2+做_______剂,过程B中Fe3+做______剂。
Fe3+的转化,在过程A中,Fe2+做_______剂,过程B中Fe3+做______剂。
②Vc使Fe3+转化为Fe2+,VC在这一过程中做___________,具有____________性。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.100mol/L 的AgNO3溶液滴定50.0mL,0.0500mol/L KCl溶液,以K2CrO4为指示剂,测得溶液中pCl=-lgc(Cl-) 、pAg=-lgc(Ag+)随加入AgNO3的体积变化如图所示,已知溶液中离子浓度小于等于1.0×10-5mol/L则沉淀完全,Ksp(Ag2CrO4)=2.0×10-12,Ksp(Ag2SO4)=1.4×10-5,下列说法错误的是( )
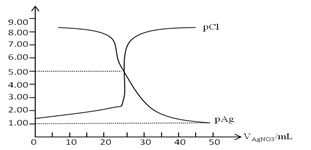
A. AgCl的沉淀溶解平衡常数Ksp数量级为10-10
B. 为防止指示剂失效,溶液应维持中性或弱碱性
C. 滴定中指示剂的有效浓度应维持在2.0×10-2 mol/L
D. 滴定完后加入1mL 0.01mol/L H2SO4会产生新的沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com