
【题目】O2、O3、N2、N4是氧和氮元素的几种单质。回答下列问题:
(1)O原子中价电子占据的轨道数目为__________________。
(2)第一电离能I1:N____O(填“>”或“<”),第二电离能I2:O大于N的原因是__________________。
(3)O3的空间构型为_________________;是_____________(填“极性”或“非极性”)分子;分子中存在的大π键,可用符号![]() 表示,其中m表示形成的大π键的原子数,n表示形成的大π键的电子数,则O3中大π键应表示为_______________________。
表示,其中m表示形成的大π键的原子数,n表示形成的大π键的电子数,则O3中大π键应表示为_______________________。
(4)N元素的简单气态氢化物NH3在H2O中溶解度很大,其原因之一是NH3和H2O可以形成分子间氢键,则在氨水中氢键可以表示为H3N…H-N、___________、____________ (任写两种即可)。
(5)已知:如下键能和键长数目。
化学键 | 键长/pm | 键能/ |
N-N | 145 | 193 |
N=N | 125 | 418 |
N | 110 | 946 |
N2和N4都是N元素的单质,其中N4是正面体构型,N原子占据四面体的四个顶点,从键参数角度分析N4分子稳定性远小于N2原因是________________________________________。
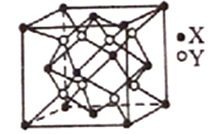
(6)Na2O的晶胞结构如下图所示,X表示O2-,Y表示Na+,则O2-的配位数为_______________,该晶胞的原子空间利用率为_______________;(已知该晶胞的棱长为apm,r(Na+)=xpm,r(O2-)=ypm)。
【答案】 4 > 失去一个电子后O+的2p处于半充满状态,更加稳定,再失去一个电子消耗能量更高 V形 极性 ![]() H3N…H-O、H2O…H-N H2O…H-O N4中N-N键能小于N2中的N
H3N…H-O、H2O…H-N H2O…H-O N4中N-N键能小于N2中的N![]() N,键长大于N
N,键长大于N![]() N 8
N 8 ![]() ×100%
×100%
【解析】分析:(1)根据原子核外电子排布式及一个原子轨道最多容纳2个电子解答。
(2)电离能是基态的气态原子失去电子变为气态阳离子,必须克服核电荷对电子的引力而所需要的能量;第一电离能是原子失去一个电子,而第二电离能则是失去外层第二个电子;可根据元素性质(活泼性)判断。
(3)臭氧中O原子以sp2杂化轨道形成σ键,分子形状为V形,形成三中心四电子大π键。
(4)N原子与其他分子的H原子之间可形成分子间氢键,O原子与其他分子的H原子之间也可形成分子间氢键。
(5)键长越小,说明原子核之间的距离小,键能越大,拆开化学键需要的能量高,稳定性越高,由此入手分析。
(6)结合晶胞结构,以处于面心上的O2-周围Na+数为例分析O2-的配位数比较容易理解;先计算晶胞中的微粒的体积,再计算晶胞体积,二者的体积百分比即是空间利用率。
详解:(1)O原子的价电子排布式为2s22p4,其价电子占据的4原子轨道。
(2)同周期从左到右第一电离能呈增大趋势,但N的电子排布最外层p能级三个轨道各有一电子,处于半充满状态,比较稳定,所以第一电离能I1:N>O;O失去一个电子后O+的2p处于半充满状态,更加稳定,再失去一个电子消耗能量更高,所以第二电离能I2:O>N。
(3)O3看成一个O原子是中心原子,其他两个O原子为配原子的三原子分子,价电子对数=2+1/2(6-2×2)=3,有一个孤电子对,属于sp2杂化,空间构型为V形;因为V形空间构型正负电荷重心不重合,所以是极性分子;O原子的轨道表示式为:![]() ,O3中心氧原子采取sp2杂化,其中两个单电子轨道与另外两个原子形成两个σ键,第三个轨道有一对孤电子对,与另两个氧原子的各1个电子形成三中心四电子大π键,可用符号
,O3中心氧原子采取sp2杂化,其中两个单电子轨道与另外两个原子形成两个σ键,第三个轨道有一对孤电子对,与另两个氧原子的各1个电子形成三中心四电子大π键,可用符号![]() 表示。
表示。
(4)因为O、N原子有比较强的吸电子能力,所以NH3和H2O既会吸引同种分子的H,又会吸引对方分子的H,从而形成氢键,所以在氨水中存在4种分子间氢键,可以表示为:H3N…H-N、H3N…H-O、H2O…H-N、H2O…H-O。
(5)因为N4是正面体构型,N原子占据四面体的四个顶点,所以N4中只存在N-N,而N2中只存在N![]() N,由表中数据可知,N-N键长大于N
N,由表中数据可知,N-N键长大于N![]() N键长,N-N键能小于N
N键长,N-N键能小于N![]() N键能,且二者键能差距较大,所以N4分子稳定性远小于N2。
N键能,且二者键能差距较大,所以N4分子稳定性远小于N2。
(6)分析Na2O的晶胞结构图可得,处于面心上的O2-被2个晶胞共用,以图中上面的面心O2-为例,在其上方还有一个同样的晶胞与其紧邻,所以每个O2-周围有8个Na+与之最近距离,则O2-的配位数为8;Na2O晶胞中Na+数为8,O2-数为:8×![]() +6×
+6×![]() =4,根据r(Na+)=xpm、r(O2-)=ypm及球体的体积公式可得:这12个原子总体积V1=8×
=4,根据r(Na+)=xpm、r(O2-)=ypm及球体的体积公式可得:这12个原子总体积V1=8×![]() ×πx+4×
×πx+4×![]() ×πy,根据该晶胞的棱长为apm,则晶胞体积为:V2=a3,所以该晶胞的原子空间利用率为:V1÷V2×100%=(8×
×πy,根据该晶胞的棱长为apm,则晶胞体积为:V2=a3,所以该晶胞的原子空间利用率为:V1÷V2×100%=(8×![]() ×πx+4×
×πx+4×![]() ×πy)÷a3×100%=
×πy)÷a3×100%=![]() ×100%。
×100%。


科目:高中化学 来源: 题型:
【题目】聚氯乙烯(PVC)保鲜膜的安全问题引起广泛关注。PVC的安全隐患主要来自于塑料中残留的PVC单体以及不符合国家标准的增塑剂DEHA。工业上用乙烯和氯气为原料经下列各步合成PVC:
![]()
(1)乙是PVC的单体,其结构简式为_____________________;
(2)反应①的化学方程式为______________________________________________________;
(3)写出以下反应类型:反应②_________________;反应③_________________。
(4)邻苯二甲酸辛酯(DOP)是国家标准中允许使用的增塑剂之一,邻苯二甲酸( )是制造DOP的原料,它跟过量的甲醇反应能得到另一种增塑剂DMP(分子式为C10H10O4),DMP属于芳香酯,请写出DMP的结构简式为________________。
)是制造DOP的原料,它跟过量的甲醇反应能得到另一种增塑剂DMP(分子式为C10H10O4),DMP属于芳香酯,请写出DMP的结构简式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某离子反应涉及H2O、Cr2O72-、NO2-、H+、NO3-、Cr3+六种微粒,已知反应过程中NO3-浓度变化如图所示,且氧化剂和还原剂的物质的量之比为1∶3,下列判断错误的是( )
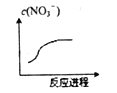
A. Cr2O72-中Cr化合价是+6 价 B. 反应的氧化产物是NO3-
C. 消耗1mol氧化剂,转移电子6mol D. 反应中Cr3+被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原电池的叙述中,正确的是( )
A.原电池的负极上发生还原反应
B.原电池工作时,电子总是由负极经导线流入正极
C.原电池中,正、负极的电极材料一定都是金属单质
D.酸碱中和反应也可以设计成原电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】南海是一个巨大的资源宝库,开发利用这些资源是科学研究的重要课题。下图为海水资源利用的部分过程,有关说法正确的是( )

A. 海水淡化的方法主要有蒸馏法、电渗析法、冰冻法
B. 氯碱工业中采用阴离子交换膜可提高产品的纯度
C. 由MgCl2·6H2O得到无水MgCl2的关键是要低温小火烘干
D. 溴工业中③、④的目的是为了富集溴元素,溴元素在反应③、⑤中均被氧化,在反应④中被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离。但事实是,硫酸在水中的第一步电离是完全的,第二步电离并不完全,其电离情况为H2SO4==H++HSO4-,HSO4-![]() H++SO42-。请回答下列有关问题:
H++SO42-。请回答下列有关问题:
(1)Na2SO4溶液呈_______(填“弱酸性”“中性”或“弱碱性”),其理由是(用离子方程式表示)_____________。
(2)H2SO4溶液与BaCl2溶液反应的离子方程式为____________________________________。
(3)在:0.10mol/L的Na2SO4溶液中,下列离子浓度关系确的是____(填字母)
A.c(Na+)=c(SO42-)+c(HSO4-)+c(H2SO4)
B.c(OH-)=c(HSO4-)+c(H+)
C.c(Na+)+c(H+)=c(OH-)+c(HSO4-)+2c(SO42-)
D.c(Na+)=2c(SO42-)+2c(HSO4-)
(4)若25℃时,0.10mol/L的NaHSO4溶液中c(SO42-)=0.029mol/L,则0.10mol/L的H2SO4溶液中c(SO42-)___(填“<”“>”或“=”)0.029mol/L
(5)若25℃时,0.10mol/LH2SO4溶液的pH=-lg0.11,则0.10mol/LH2SO4溶液中c(SO42-)=____mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氧磷(POCl3)常用作半导体掺杂剂及光导纤维原料,实验室制备POCl3并测定产品含量的实验过程如下:
Ⅰ.制备POCl3。
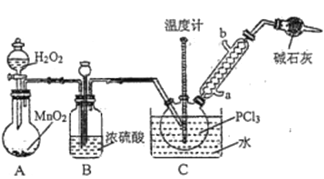
采用氧气氧化液态PCl3法制取POCl3,实验装置(加热及夹持仪器略)如图所示:
已知:①Ag++SCN-=AgSCN↓;Ksp(AgCl)>Ksp(AgSCN);磷酸银溶于硝酸。
②PCl3和POCl3的相关信息如下表:
物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
PCl3 | -112.0 | 76.0 | 137.5 | 两者互溶,均为无色液体,遇水均剧烈反应生成含氧酸和氯化氢 |
POCl3 | 2.0 | 106.0 | 153.5 |
(1)POCl3遇水反应的化学方程式为_________________________________________。
(2)装置B的作用除干燥O2外,还有_________________________________________。干燥管的作用是_______________。
(3)反应温度要控制在60~65℃,原因是_____________________________________________。
Ⅱ.测定POCl3产品的含量。
实验步骤:
①制备POCl3实验结束后,待三颈烧瓶中的液体冷却至室温,准确称取30.7gPOCl3产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解,将水解液配成100.00mL溶液。
②取10.00mL溶液于锥形瓶中,加入10.00mL3.2mol/LAgNO3标准溶液。
③加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖。
④以X为指示剂,用0.2mol/LKSCN溶液漓定过量的AgNO3溶液,达到滴定终点时共用去10.00mLKSCN溶液。
(4)步骤③中加入硝基苯的作用是___________________________________________。若无此操作,所测产品中氯元素的质量分数将会__________(填“偏大”、“偏小”或“不变”)。
(5)步骤④中X为__________,产品中POCl3的质量分数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设pC为溶液中粒子物质的量浓度的负对数,即:pC=-lgC。25℃时,某浓度H2R水溶液中,pC(H2R)、pC(HR-)、pC(R2-)随溶液pH的变化曲线如图所示。下列说法正确的是
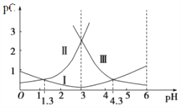
A. 曲线I表明,c(R2-)随着pH增大而逐渐增大
B. pH=1.3时,3c(R2-)+c(OH-)=10-1.3mol/L
C. 常温下,该体系中c2(HR-)/ c(R2-)·c(H2R)=1000
D. NaHR水溶液中:c(Na+)>c(HR-)>c(OH-)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com