
【题目】硫酸铝铵![]() 是一种重要的分析试剂,下列有关说法正确的是( )
是一种重要的分析试剂,下列有关说法正确的是( )
A.硫酸铝铵中![]() 的水解程度比明矾中
的水解程度比明矾中![]() 的水解程度大
的水解程度大
B.该物质的水溶液中![]() 、
、![]() 、
、![]() 、
、![]() 都可大量共存
都可大量共存
C.向该物质的溶液中滴加同浓度的NaOH溶液的体积与生成沉淀的关系如图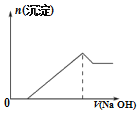
D.向该物质的溶液中滴加![]() 溶液,使
溶液,使![]() 恰好完全沉淀的离子方程式为:
恰好完全沉淀的离子方程式为:![]()
【答案】D
【解析】
A.硫酸铝铵溶液中铵根离子水解显酸性抑制铝离子的水解,明矾溶液中铝离子水解显酸性,硫酸铝铵中Al3+的水解程度比明矾中Al3+的水解程度小,故A错误;
B.该物质的水溶液中S2-和铝离子能够发生双水解反应,生成氢氧化铝和硫化氢,不能大量共存,故B错误;
C.向该物质的溶液中滴加同浓度的NaOH溶液,先生成氢氧化铝沉淀,再和铵根离子结合生成一水合氨,沉淀量不变,继续滴加氢氧化钠,氢氧化铝沉淀溶解,曲线变化为先沉淀,再出现平台,最后沉淀溶解,故C错误;
D.向该物质的溶液中滴加Ba(OH)2溶液,使SO42-恰好完全沉淀二者恰好按照NH4Al(SO4)2和Ba(OH)2,物质的量之比为1∶2,离子方程式为:NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3H2O,故D正确;
故选D。


科目:高中化学 来源: 题型:
【题目】某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线以下某一刻度,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数
请回答:
(1)以上步骤有错误的是___(填编号),该错误操作会导致测定结果___(填“偏大”、“偏小”或“无影响”)。
(2)实验中用左手控制___,眼睛注视___,直至滴定终点。判断滴定终点的现象是:锥形瓶中溶液___。
(3)如图是某次滴定时的滴定管中的液面,其读数为___mL。
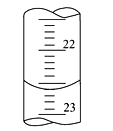
(4)根据下列数据:请计算待测盐酸溶液的浓度为___mol/L。
滴定次数 | 待测液体积(mL) | 标准液读数记录(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 20.00 | 0.42 | 20.40 |
第二次 | 20.00 | 2.28 | 22.30 |
第三次 | 20.00 | 0.20 | 22.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y的价电子数相同,且原子序数之比等于1∶2;元素Z是人体必需的微量元素,位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。
(1)与X同周期且第一电离能比X大的元素有_____种。
(2)基态Y原子中,能量最高的核外电子占据的能级的电子云轮廓图形状为____。
(3)X与Y可形成多种微粒,其中微粒的立体构型为正四面体形的是____(写化学式),写出两种与它互为等电子体的粒子的化学式_____(写一种分子和一种离子)
(4)Y与Z形成的某种晶体的晶胞如图所示,该晶胞中Z微粒的配位数为_____,该化合物的化学式为_____。
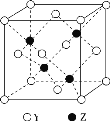
(5)已知ZY晶体的熔点约为1700℃,ZX与ZY结构相似,其熔点为1975℃,构成ZY晶体的作用力是_____,ZX熔点较高的原因是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同元素的原子在分子内吸引电子的能力大小可用一数值X来表示,若X越大,则原子吸引电子的能力越强,在所形成的分子中成为负电荷一方。下面是某些短周期元素的X值。
元素 | Li | Be | B | C | O | F |
X值 | 0.98 | 1.57 | 2.04 | 2.53 | 3.44 | 3.98 |
元素 | Na | Al | Si | P | S | Cl |
X值 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)通过分析X值的变化规律,确定N、Mg的X值范围:___<X(Mg)<___;___<X(N)<___。
(2)推测X值与原子半径的关系是___。
(3)某有机物结构简式为![]() ,在SN中,你认为共用电子对偏向谁?___(写原子名称)。
,在SN中,你认为共用电子对偏向谁?___(写原子名称)。
(4)经验规律告诉我们当成键的两原子相应元素电负性的差值△X>1.7时,一般为离子键,当△X<1.7时,一般为共价键,试推断AlBr3中化学键的类型是_______。
(5)预测元素周期表中,X值最小的元素位置_______(放射性元素除外)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(1)在这些元素中,金属性最强的元素是_____,最活泼的非金属元素是_______________
(2)化学性质最不活泼的元素是______________,其原子的原子结构示意图为___________;
(3)元素的最高价氧化物对应的水化物中酸性最强的是______________,碱性最强的是____________,
(4)在③~⑦元素中,原子半径最大的是________,原子半径最小的是_______;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾(![]() )是治疗缺铁性贫血的特效药。某化学兴趣小组对绿矾进行了如下的探究:
)是治疗缺铁性贫血的特效药。某化学兴趣小组对绿矾进行了如下的探究:
I .【制备产品】
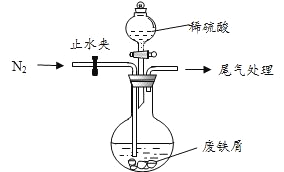
该小组由废铁屑(含少量氧化铜、氧化铁等杂质),用上图所示装置制备![]() 晶体,步骤如下:
晶体,步骤如下:
(1)预处理:先将废铁屑加入到饱和![]() 溶液中洗涤,目的是_____,然后将废铁屑用水洗涤2~3 遍。
溶液中洗涤,目的是_____,然后将废铁屑用水洗涤2~3 遍。
(2)将洗涤后的废铁屑加入到圆底烧瓶中,并持续通入![]() ,
,![]() 的作用是________。
的作用是________。
(3)再加入足量稀硫酸,控制温度 50℃~80℃之间,充分反应后,圆底烧瓶中剩余的固体为_____________。
(4)获取产品:先向步骤(3)中反应后的混合物中加入少许蒸馏水,趁热过滤, ____________。
滤出晶体,用少量冰水洗涤 2~3 次,再用滤纸将晶体吸干,密闭保存。
II.【测定![]() 含量】
含量】
(1)称取上述样品 10.0g,溶于适量的稀硫酸中,配成 100mL 溶液,需要的仪器除天平、胶头滴管、 烧杯、量筒外,还需要的仪器有(填仪器名称)____________________、_______________________。
(2)准确量取 25mL 该液体于锥形瓶中,用 0.1000mol/L ![]() 标准溶液滴定,则滴定终点的判断方法是________________________。
标准溶液滴定,则滴定终点的判断方法是________________________。
(3)用同样的方法滴定 3 次,平均消耗 10.00mL 标准液,该样品中![]() 的质量分数为____________。(已知 Mr(
的质量分数为____________。(已知 Mr(![]() )=278)
)=278)
(4)若测量结果偏小,则可能是在定容时_________________(填“俯视”或“仰视”)读数。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一透明溶液,可能含有较大量的Mg2+、Fe3+、Al3+、Cu2+、Na+、H+、SO42-、CO32-中的一种或几种,取此溶液做下列实验:
①取少量溶液加入用盐酸酸化的BaCl2溶液,有白色沉淀生成;
②取少量溶液加入过氧化钠粉末,溶液中有白色沉淀产生并逸出无色无味的气体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示。
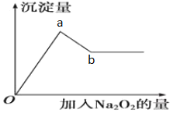
试推断并完成作答:
(1)溶液中一定含有的离子是___________;
(2)溶液中肯定不含有的离子是_________;
(3)检验可能含有的离子的方法是____________。
(4)图示中a点沉淀的成分是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com