
【题目】有一透明溶液,可能含有较大量的Mg2+、Fe3+、Al3+、Cu2+、Na+、H+、SO42-、CO32-中的一种或几种,取此溶液做下列实验:
①取少量溶液加入用盐酸酸化的BaCl2溶液,有白色沉淀生成;
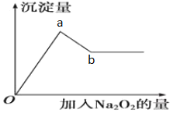
②取少量溶液加入过氧化钠粉末,溶液中有白色沉淀产生并逸出无色无味的气体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示。
试推断并完成作答:
(1)溶液中一定含有的离子是___________;
(2)溶液中肯定不含有的离子是_________;
(3)检验可能含有的离子的方法是____________。
(4)图示中a点沉淀的成分是______________。
【答案】Mg2+、Al3+、SO42- CO32-、H+、Cu2+、Fe3+ 焰色反应检验 Al(OH)3和Mg(OH)2
【解析】
取少量溶液加入用盐酸酸化的BaCl2溶液,有白色沉淀生成,则溶液中一定含有SO42-,取少量溶液加入过氧化钠粉末,溶液中有白色沉淀产生并逸出无色无味的气体,从图上看一开始就产生了沉淀,故溶液中无H+,Fe3+,Cu2+,因为沉淀质量随着过氧化钠的增加有溶解,说明溶液中同时含有Mg2+和Al3+,那么溶液中一定没有CO32-,Na+无法确认,综上所述,一定还有的离子为:Mg2+、Al3+、SO42-,一定不含的离子为:CO32-、H+、Cu2+、Fe3+,可能含有Na+,据此解答。
(1)由分析可知,溶液中一定含有的离子是Mg2+、Al3+、SO42-,故答案为:Mg2+、Al3+、SO42-;
(2)溶液中肯定不含有的离子是CO32-、H+、Cu2+、Fe3+,故答案为:CO32-、H+、Cu2+、Fe3+;
(3)可能含有的为Na+,可用焰色反应来检验,故答案为:焰色反应检验;
(4)图示中a点沉淀达到最大值,是Mg2+、Al3+恰好完全转换为沉淀的点,所以a点沉淀的成分为:Al(OH)3和Mg(OH)2,故答案为:Al(OH)3和Mg(OH)2。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】硫酸铝铵![]() 是一种重要的分析试剂,下列有关说法正确的是( )
是一种重要的分析试剂,下列有关说法正确的是( )
A.硫酸铝铵中![]() 的水解程度比明矾中
的水解程度比明矾中![]() 的水解程度大
的水解程度大
B.该物质的水溶液中![]() 、
、![]() 、
、![]() 、
、![]() 都可大量共存
都可大量共存
C.向该物质的溶液中滴加同浓度的NaOH溶液的体积与生成沉淀的关系如图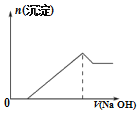
D.向该物质的溶液中滴加![]() 溶液,使
溶液,使![]() 恰好完全沉淀的离子方程式为:
恰好完全沉淀的离子方程式为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有2.8 g Fe全部溶于一定浓度、200 mL的HNO3溶液中,得到标准状况下的气体1.12 L,测得反应后溶液的pH为1。若反应前后溶液体积变化忽略不计,则下列有关判断正确的是
A. 反应后溶液中铁元素可能以Fe2+形式存在
B. 反应后的溶液最多还能溶解1.4 g Fe
C. 反应后溶液中c(NO3)=0.85 mol·L1
D. 1.12 L气体可能是NO、NO2的混合气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求填空做答。
(1)NaHCO3能用于治疗胃酸过多,反应的离子方程式为_______。
(2)铁和水蒸气反应的化学方程式为3Fe+4H2O(g)![]() Fe3O4+4H2,该反应中84g Fe参加反应,转移电子的物质的量为__________。
Fe3O4+4H2,该反应中84g Fe参加反应,转移电子的物质的量为__________。
(3)制备Fe(OH)3的实验操作:向煮沸的蒸馏水中加入几滴FeCl3溶液,______。
(4)密度为1.84g/cm3,质量分数为98%的浓硫酸的物质的量浓度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NaOH溶液滴入某一元酸(HA)溶液中,测得混合溶液的pH与离子浓度变化关系如图所示[已知:![]() ]。下列叙述不正确的是
]。下列叙述不正确的是

A. Ka(HA)的数量级为10-5
B. 滴加NaOH溶液的过程中,![]() 保持不变
保持不变
C. m点所示溶液中:c(H+)+c(Na+)=c(HA)+c(OH-)
D. n点所示溶液中:c(Na+)=c(A-)+c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下述实验方案能达到实验目的的是( )
编号 | A | B | C | D |
实验方案 |
|
|
|
|
实验目的 | 实验室制备乙酸乙酯 | 分离乙酸和水 | 验证溴乙烷在氢氧化钠乙醇溶液中发生消去反应产生的乙烯 | 收集乙烯并验证它与溴水发生加成反应 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定![]() 假设盐酸与NaOH溶液混合后体积变化忽略不计
假设盐酸与NaOH溶液混合后体积变化忽略不计![]() ,滴定过程中溶液的pH变化如图所示。下列叙述正确的是
,滴定过程中溶液的pH变化如图所示。下列叙述正确的是![]()
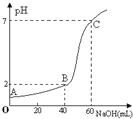
A.所用HCl的浓度是![]() ,NaOH溶液浓度为
,NaOH溶液浓度为![]()
B.在B点,溶液中离子浓度关系为:![]()
C.A.![]() 三点水的电离程度大小依次为:
三点水的电离程度大小依次为:![]()
D.滴定前,锥形瓶用待测液润洗,导致HCl浓度偏低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对SCN-的性质进行探究,设计了以下实验
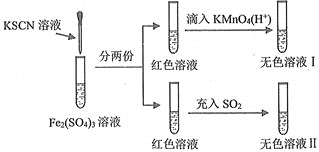
已知:(CN)2、(SCN)2、(OCN)2等称之为拟卤素,它们的化学性质均与卤素单质相似。下列说法正确的是( )
A.溶液颜色变红时发生反应的离子方程式是:Fe3++3SCN-=Fe(SCN)3↓
B.红色溶液褪色表现了SO2的漂白性
C.氧化性:KMnO4>Fe3+>(SCN)2
D.无色溶液Ⅱ中滴入适量的KMnO4(H+)溶液,溶液又变成红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中,一定条件下发生反应:2A![]() B(g)+2C(g),且达到平衡。当升高温度时气体的密度增大,则下列叙述中正确的是 ( )
B(g)+2C(g),且达到平衡。当升高温度时气体的密度增大,则下列叙述中正确的是 ( )
A. 升高温度,正反应速率增大,逆反应速率减小
B. 若正反应是放热反应,则A为气态
C. 物质A一定为非气态,且正反应是吸热反应
D. 若向容器中充入惰性气体,则平衡向右移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com