
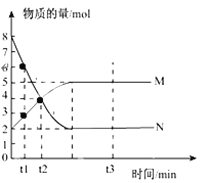
【题目】一定温度下,在容积为V L的密闭容器中进行反应:aN(g)![]() bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
(1)此反应化学方程式中![]() =_________。
=_________。
(2)t1到t2时刻,以N的浓度变化表示的平均反应速率为:___________________。
(3)为提高反应速率,可以采取________、_______等可行的措施(已知该反应无需催化剂)。
【答案】2![]() mol·L-1·min-1升温加压或增大浓度
mol·L-1·min-1升温加压或增大浓度
【解析】
(1)根据化学反应方程式的计量数之比等于物质的量变化之比。(2)由图可知,t1到t2时刻N的物质的量变化,根据v=△n/V△t计算v(N)(3)根据影响化学反应的速率的因素为温度、浓度、压强和催化剂等进行选择。
(1)因为方程式aN(g)![]() bM(g),由图可知,t1到t2时刻N的物质的量变化为6mol-4mol=2mol,M的物质的量变化为4mol-3mol=1mol由此知反应化学方程式中
bM(g),由图可知,t1到t2时刻N的物质的量变化为6mol-4mol=2mol,M的物质的量变化为4mol-3mol=1mol由此知反应化学方程式中![]() =2mol /1mo =2。答案为:2。
=2mol /1mo =2。答案为:2。
(2)由图可知,t1到t2时刻N的物质的量变化为6mol-4mol=2mol,根据v=△n/V△t,故v(N)=2mol/VL(t2- t1)min=2/V(t2- t1)mol/(L.min),故答案为:![]() mol·L-1·min-1
mol·L-1·min-1
(3)已知影响化学反应的速率的因素为温度、浓度、压强和催化剂等,为提高反应速率,可以采取升高温度或者增大气体的压强或者增大反应物的浓度都可以加快化学反应速率。所以答案为:升温 加压或增大浓度。


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】实验:①0.1molL﹣1AgNO3溶液和0.1molL﹣1NaCl溶液等体积混合得到浊液a,过滤得到滤液b和白色沉淀c;
②向滤液b中滴加0.1molL﹣1KI溶液,出现浑浊;
③向沉淀c中滴加0.1molL﹣1KI溶液,沉淀变为黄色.
下列分析不正确的是( )
A. 浊液a中存在沉淀溶解平衡:AgCl(s)![]() Ag+(aq)+Cl﹣(aq)
Ag+(aq)+Cl﹣(aq)
B. 滤液b中不含有Ag+
C. ③中颜色变化说明AgCl转化为AgI
D. 实验可以证明AgI比AgCl更难溶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生 产MnO2和Zn的工艺简化流程如图所示(中间产物的固体部分已经略去):
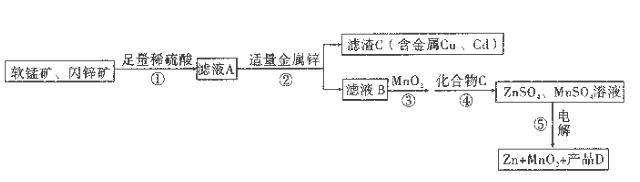
软锰矿: MnO2含量≥65%;Al2O3含量为4%。闪锌矿: ZnS含量≥80%; FeS、CuS、CdS含量各为2%。 滤液B中含金属离子: Zn2+、Mn2+、 Fe2+、Al3+。
试回答下列问题:
(1)步骤①中软锰矿、闪锌矿与硫酸溶液共热时可析出硫,且金属元素转化为相应的硫酸盐(铁元素以+3价存在)。 其中MnO2和FeS发生的离子方程式为___________________________。
(2)步骤③ 中的MnO2也可用下列___________________物质代替(不考虑Mn2+的反应)
A.KMnO4 固体 B.H2O2 C.浓硝酸 D.新制氯水
(3) 步骤⑤电解过程中阳极的电极反应式为___________________________。
(4)加入化合物C后可得纯净的ZnSO4 、MnSO4溶液,C可以是ZnO或Zn(OH)2,Mn (OH)2 或MnCO3,
则产品D为___________________________(填化学式)。
(5)I .将制得的MnO2(s)与KOH(s)、KClO3(s)(按比例混合,加热熔融(不断搅拌)可得KCl和K2MnO4的固体混合物;
II.再用5%的KOH溶液溶解得绿色(MnO42-)溶液;
III.向绿色溶液中通入适量的CO2后,将溶液加热,并趁热滤去残渣( 含MnO2(s)];
IV.将滤液蒸发浓缩、冷却结品、过滤、洗涤、干燥得紫色KMnO4晶体。
①第III步操作中“趁热过滤”的目的是___________________________。
② 写出III中生成KMnO4的化学程式__________________________________。
③III中需控制CO2的用量,若CO2过量,会使所得产品的纯度降低,原因可能是___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语的表示正确的是( )
A. 甲烷的球棍模型:![]() B. 氯离子的结构示意图:
B. 氯离子的结构示意图:![]()
C. 氮气的结构式:∶N≡N∶ D. 氯化氢的电子式:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 白磷和红磷互为同素异形体 B. CH3-CH2OH和 CH3-O-CH3 互为同分异构体
C. ![]() 和
和![]() 互为同位素 D. 分子间作用力越大,分子越稳定。
互为同位素 D. 分子间作用力越大,分子越稳定。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸的下列性质中,可以证明它是弱电解质的是
A. 0.1mol/L醋酸溶液的c(H+)约为1×10-3mol/L
B. 醋酸能与水以任何比例互溶
C. 10mL 1mol/L醋酸恰好与10mL 1mol/L NaOH溶液完全反应
D. 醋酸溶液的导电性比盐酸溶液的弱
【答案】A
【解析】0.1mol/L醋酸溶液的c(H+)约为1×10-3mol/L,说明醋酸只电离了一部分,所以是弱电解质,选项A正确。醋酸能与水以任何比例互溶是醋酸的物理性质,这个与电解质的强弱无关,选项B错误。10mL 1mol/L的一元酸(无论强弱)都会恰好与10mL 1mol/L NaOH溶液完全反应,所以选项C错误。因为没有说明浓度的关系,所以醋酸溶液的导电性比盐酸溶液的弱,并不能说明醋酸是弱电解质,选项D错误。
点睛:证明一个一元酸HA是弱电解质的方法主要有:
配成0.1mol/L的溶液,测得氢离子浓度小于0.1mol/L,或者测得pH>1。
测NaA的溶液的酸碱性,得到该溶液显碱性。
配成相同浓度的HA和HCl溶液,测得HA的导电性较差。
【题型】单选题
【结束】
16
【题目】下列表示化学过程的化学用语书写正确的是
A. BaSO4投入水中后建立的沉淀溶解平衡:BaSO4![]() Ba2++SO42-
Ba2++SO42-
B. AlCl3溶液与NaAlO2溶液混合:A13++A1O2-+3H2O![]() 2Al(OH)3↓
2Al(OH)3↓
C. HCO3-的电离:HCO3-+H2O![]() CO32-+H3O+
CO32-+H3O+
D. Na2SO3的水解:SO32-+2H2O![]() H2SO3+2OH-
H2SO3+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是



甲 乙 丙
A. 图甲中纯水仅升高温度,就可以从a点变到c点
B. 图甲中在b点对应温度下,将pH=2的H2SO4溶液与pH=10的NaOH溶液等体积混合后,溶液显中性
C. 图乙表相同温度下pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强
D. 用0.0100mol/L硝酸银标准溶液,滴定浓度均为0.1000mol/L,C1-、Br-及I-的混合溶液,由图丙曲线,可确定首先沉淀的是Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是

A. X→Y反应类型为酯化反应
B. X、Y、Z均能使溴的四氯化碳溶液褪色
C. Y和Z互为同分异构体
D. 等物质的量的X、Z分别与足量Na反应,消耗Na的物质的量之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.CH3COOH和CH3COOCH3互为同系物B.氧气和臭氧互为同位素
C.C5H12有四种同分异构体D.金刚石和石墨互为同素异形体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com