
����Ŀ��[��ѧ�D�Dѡ��2����ѧ�뼼��]�������Ҷ�����������ԭ���ͳ����������ڽ������⡢֯��Ư��ϡ��������һ���Ʊ��������������ᾧˮ���Ĺ����������£�

�ش��������⣺
��1��CO��NaOH��һ�������ºϳɼ����ơ������Ƽ�������Ļ�ѧ��Ӧ����ʽ�ֱ�Ϊ �� ��
��2�����Ʊ������������ι��˲���,���˲����ٵ���Һ�� �������� _____�����˲����ڵ���Һ�� __�� ��������________ ��
��3�����չ����Тۺܵ͢�Ŀ���� ��
��4�����˽�������������ֱ���������ữ�Ʊ����ᡣ�÷�����ȱ���Dz�Ʒ���������к��е�������Ҫ�� ��
��5���ᾧˮ�ϲ����Ʒ�Ĵ����ø�����ط��ⶨ�����������Ʒ0.250g����ˮ����0.0500mol/L������KMnO4��Һ�ζ�����dz�ۺ�ɫ�����ʣ�����KMnO4��Һ15.00mL����Ӧ�����ӷ���ʽΪ ����ʽ����ó�Ʒ�Ĵ��� ��
���𰸡���1��CO��NaOH![]() HCOONa��2HCOONa
HCOONa��2HCOONa![]() Na2C2O4 + H2��
Na2C2O4 + H2��
��2��NaOH��Һ��CaC2O4��H2C2O4��Һ��H2SO4��Һ��CaSO4 ��5����
��3���ֱ�ѭ����������������Һ�����������ͳɱ�������С��Ⱦ����1���� ��4��Na2SO4 ��1����
��5��5C2O42��+2MnO4��+16H+��2Mn2++8H2O+10CO2����2���� 94.5% ��2����
��������
�����������1��������������ͼ��֪��CO��NaOH��һ�������ºϳɼ����Ʒ���ʽΪCO��NaOH![]() HCOONa�������Ƽ���������ͬʱ���в��������ɣ���˷�Ӧ�Ļ�ѧ��Ӧ����ʽΪ2HCOONa
HCOONa�������Ƽ���������ͬʱ���в��������ɣ���˷�Ӧ�Ļ�ѧ��Ӧ����ʽΪ2HCOONa![]() Na2C2O4 + H2����
Na2C2O4 + H2����
��2�����ݷ�Ӧԭ�����ܽ����Լ�ʾ��ͼ��֪�����˲���������Һ��NaOH��Һ��������CaC2O4�����˲���������Һ��H2C2O4��Һ��H2SO4��Һ��������CaSO4��
��3�����ݹ��չ��̿�֪�����բۿ���ѭ�������������ƣ����բܿ���ѭ���������ᣬ�������ԭ�ϵ������ʣ��ֽ����˳ɱ�����С��Ⱦ��
��4�������������IJ���Ϊ�����ƣ�ֱ���������ữ�����ɲ���������ƣ����к��е�������Ҫ��Na2SO4��
��5���ڲⶨ�����У��������Ϊ������������Ϊ��ԭ������Ӧ�����ӷ���ʽ5C2O2- 4 + 2MnO- 4 + 16H+ = 2Mn2+ + 8H2O + 10CO2�������ݷ���ʽ�ɵù�ϵʽ��
5H2C2O4��2H2O ~ 2KMnO4
5 2
n 0.05mol/L��15.0��10-3L
���n��H2C2O4��2H2O��=1.875��10-3mol
��m��H2C2O4��2H2O��=1.875��10-3mol��126g/mol=0.236g
���Գ�Ʒ�Ĵ��Ȧ�=![]() ��100%=94.5%��
��100%=94.5%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѧ��ѡ��5�л���ѧ������
�����ؾ��п�ͻ���Ԥ�����������ã���ϳ�·�����£�

��֪��
i��1 mol G���������Na��NaOH��NaHCO3�����ʵ����ֱ�Ϊ3 mol��2 mol��1 mol��
ii��![]()
iii�� ��R1��R2��R3Ϊ��������ԭ�ӣ� ��ش�
��R1��R2��R3Ϊ��������ԭ�ӣ� ��ش�
��1��B��C����Ӧ������ ��
��2��C��D��Ӧ�Ļ�ѧ����ʽ�� ��
��3��E�ĺ˴Ź����������������壬E�к��еĹ����������� ��
E��G��Ӧ�Ļ�ѧ����ʽ�� ��
��4�������й�����ȩ����������ȷ���� ��
a������ȩ����NaHCO3��Һ��Ӧ
b������ȩ����Ũ��ˮ����ȡ����Ӧ
c��1 mol����ȩ�������3 molH2�����ӳɷ�Ӧ
��5��д��һ�ַ�����������������ȩ��ͬ���칹��Ľṹ��ʽ ��
�������ϵ�һ����ȡ������2��
��1 mol������ˮ�⣬�������3 molNaOH
��6�������صķ�������2���������ṹ��ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ٷɻ���ƽ�������ʱ��β���е�NO���ƻ������㡣��ѧ�������о����ô�������β���е�NO��COת���CO2��N2����ѧ����ʽ���£�2NO + 2CO![]() 2CO2 + N2��Ϊ�˲ⶨ��ij�ִ��������µķ�Ӧ���ʣ���ij�¶��������崫������ò�ͬʱ���NO��COŨ�������
2CO2 + N2��Ϊ�˲ⶨ��ij�ִ��������µķ�Ӧ���ʣ���ij�¶��������崫������ò�ͬʱ���NO��COŨ�������
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/mol��L-1 | 1.00��10-3 | 4.50��10-4 | 2.50��10-4 | 1.50��10-4 | 1.00��10-4 | 1.00��10-4 |
c(CO)/mol��L-1 | 3.60��10-3 | 3.05��10-3 | 2.85��10-3 | 2.75��10-3 | 2.70��10-3 | 2.70��10-3 |
��ش���������(���������¶ȱ仯�Դ�����Ч�ʵ�Ӱ��):
��1�� ǰ3s��ƽ����Ӧ����v(N2)��_____________��(�𰸱���2λС��)
��2�� ����4sʱCO��ת���ʦ� �� ��
��3�� ���д�ʩ�����NO��COת���CO2��N2�ķ�Ӧ���ʵ���( )
A.ѡ�ø���Ч�Ĵ��� B.���߷�Ӧ��ϵ���¶�
C�����ͷ�Ӧ��ϵ���¶� D.��С���������
��4�� �о���������ʹ�õ���������ʱ����������ȱ���������ѧ��Ӧ���ʡ�Ϊ�˷ֱ���֤�¶ȡ������ȱ�����Ի�ѧ��Ӧ���ʵ�Ӱ����ɣ�ijͬѧ���������ʵ�飬����ʵ�������Ѿ���������ʵ����Ʊ��С�
ʵ���� | T/�� | NO��ʼŨ��/mol��L-1 | CO��ʼŨ��/ mol��L-1 | �����ıȱ����/m2��g-1 |
�� | 280 | 1.20��10-3 | 5.80��10-3 | 82 |
�� | 124 | |||
�� | 350 | 124 |
�������ϱ���������ʣ���ʵ���������ݡ�
�����ڸ���������ͼ�У������ϱ��еĢ�����ʵ�������»��������NOŨ����ʱ��仯����������ͼ������������������ʵ���š�
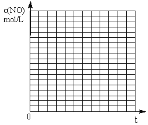
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���༰�仯���ﱻ�㷺Ӧ���ڰ뵼�塢������������Ǧп�����̳�Ϊԭ�Ͽ��Ʊ�GeO2���乤������ͼ���¡�

��֪��GeO2�����������GeCl4��ˮ�⣬�е�86.6��
��1��������������Ҫ�ɷ���_____________���ѧʽ����ʵ������ȡ�����õ��IJ���������__________________��
��2����������ȡʱ�������ȡ����Vˮ��/V�л�����ˮ����л������ �������Ĺ�ϵ����ͼ��ʾ���������ɱ��Ƕȿ��ǣ������˵�Vˮ��/V�л�����ֵΪ ��

��3����������������������__________________________________�������㼴������Ӧ�����¶ȵķ�������Χ____________________________��
��4����������Ӧ�Ļ�ѧ����ʽ_______________________________��
��5��������������ô��������ƻ�ԭΪGe2+���õ�����Һ��ָʾ������c mol/L����ر���Һ�ζ����������VmL,�г��̳���������������ļ���ʽ________�����йط�ӦʽΪ��3Ge2++IO3-+6H+��3Ge4++I-+3H2O��IO3-+5I-+6H+��3I2+3H2O����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧ ѡ��2����ѧ�뼼��]
�������Ҫ�Ļ���ԭ�ϣ���N2��H2Ϊԭ����ȡ����淋�����ͼ���£���ش��������⣺

��1������������ͼ�У�B�豸�������� �����з�����Ӧ�Ļ�ѧ����ʽΪ ��
��2����������ҵ�����У�N2��H2�ϳ�NH3�Ĵ����� ��1909�껯ѧ�ҹ�����ʵ�����״κϳ��˰���2007�껯ѧ�Ҹ���¡����ض��ڹ����о���֤ʵ�������뵪���ڹ����������ϳɰ��ķ�Ӧ���̣�ʾ��ͼ���£�

![]() �ֱ��ʾN2��H2��NH3 ��ͼ����ʾ���ɵ�NH3�뿪�������棬ͼ����ͼ���ĺ���ֱ��� �� ��
�ֱ��ʾN2��H2��NH3 ��ͼ����ʾ���ɵ�NH3�뿪�������棬ͼ����ͼ���ĺ���ֱ��� �� ��

��3��NH3��CO2��һ�������¿ɺϳ����أ��䷴ӦΪ��2NH3(g)+CO2(g) ![]() CO( NH2)2(s)+H2O(g)
CO( NH2)2(s)+H2O(g)
��ͼ��ʾ�ϳ����а�̼��a��CO2ת���ʦصĹ�ϵ��aΪ[n(NH3)/n(CO2)]��bΪˮ̼��[n(H2O)/n(CO2)]����
��bӦ������ �� A��1.5��1.6 B��1��1.1 C��0.6��0.7
��aӦ������4.0�������� ��
��4���ںϳɰ����豸���ϳ������У������Ƚ�������Ŀ���� ���ںϳ��������������ͨ�������Ŀ���� ��
��5����������Ĺ����г������һЩ��������������������ַ���������
��Һ���շ���NO+NO2+2NaOH��2NaNO2+H2O
NH3��ԭ����8NH3+6NO2![]() 7N2+12H2O��NOҲ�����Ƶķ�Ӧ��
7N2+12H2O��NOҲ�����Ƶķ�Ӧ��
�������ַ����У�������ɫ��ѧ���� ��
��6��ij���ʳ���NH3�Ʊ�NH4NO3����֪����NH3��NO�IJ�����96%��NO��HNO3�IJ�����92%������HNO3����ȥ��NH3������ռ�ܺ�NH3������������������ģ��� %��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����Ӧ3A(g)��B(g) ===2C(g)�����ֲ�ͬ�������½��з�Ӧ����ͬһʱ��������õķ�Ӧ�����ò�ͬ�����ʱ�ʾΪ��vA��1 mol/(L��min)����vC��0.5 mol/(L��min)����vB��0.5 mol/(L��min)����������¸÷�Ӧ����������С�Ĺ�ϵ�� ��������ű�ʾ��
��2��ij�¶�ʱ����һ��5L�ĺ��������У�X��Y��Z��Ϊ���壬�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ��������գ�

���÷�Ӧ�Ļ�ѧ����ʽΪ____________________________��
����Ӧ��ʼ��2min��������Z��ʾ��ƽ����Ӧ����Ϊ ��
��2min��Ӧ��ƽ�������ڻ�������ƽ����Է����������� ʼʱ �������С������ȡ���ͬ������������ܶȱ���ʼʱ ��
��������Ӧ���ڵ�2minʱ��X��ת����Ϊ ��
����a mol X��b mol Y�Ļ�����巢��������Ӧ����Ӧ��ijʱ�̸����ʵ���ǡ�����㣺n (X) = n (Y) = n (Z)����ԭ���������a : b =__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ҩ�ﰢ˾ƥ�ֿ���ˮ�����Ƶã����ǵĽṹ��ͼ��ʾ���й�˵����ȷ����

A�����ð�˾ƥ�֣��������ˮ�������Ӧʱ���ɾ���ע��NaHCO3��Һ
B����˾ƥ�ֵķ���ʽΪC9H10O4
C��1 mol��˾ƥ����������2 mol NaOH
D��ˮ������Է���ȡ�����ӳɡ��������Ӿ۷�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����2H2(g)+O2(g)=2H2O(l);��H=��572kJ/mol
��2H2(g)+O2(g)=2H2O(g);��H=��484kJ/mol
��CH4(g)+2O2(g)=2H2O(l)+CO2(g);��H=��890kJ/mol
��1����֪H-H�ļ���436kJ/molO=O�ļ���496kJ/molH-O�ļ���463kJ/mol�������������ݼ����٢���һ����Ӧ����ͨ������ֱ�Ӽ���ó� ��������д����Ӧ H2O ( l ) = H2O ( g )���ʱ���H= ��
��2���������ɼ���CO2��g��+4H2( g ) =CH4( g ) +2H2O( g )���ʱ���H= ��
��3�����٢ڢ���������ʽ����һ����ȼ���ȵ��Ȼ�ѧ����ʽ �����Ӧ����ʽ����ţ���״���£�ȡ����������Ļ������11.2 L��ȫȼ�պ�ָ������£���ų�������Ϊ263.8kJ�������������м������������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϣ���500-600�����м��ͨ������������ˮ�Ȼ������������м��ͨ���Ȼ���������ˮ�Ȼ�������������ͼ��ʾ��װ��ģ���������̽���ʵ�顣

�ش��������⣺
��1����ȡ��ˮ�Ȼ�����ʵ���У�A�з�Ӧ�Ļ�ѧ����ʽΪ ��������1molCl2ʱ��ת�Ƶĵ�����Ϊ ������˿�������� ��װ��B�м�����Լ��� ��װ��D�м�����Լ��� ��
��2����ȡ��ˮ�Ȼ�������ʵ���У�β���ijɷ��� ��������D��װ�ý���β�����������ڵ������� �� ��
��3���������������Ƶõ�FeCl2�Ậ������FeCl3���ʣ�����˵������ȷ����
A������FeCl3���õ��Լ���KSCN��Һ
B��������������м�������Fe�۳�ȥ����
C���������������ͨ������Cl2��ȥ����
D�����Ƶô�����FeCl2����ʵ�������Ӧ�ȵ�ȼA���ľƾ��ƣ��ڵ�ȼC���ľƾ��ơ�
��4������һ��FeCl2��FeCl3����ij��ѧ��ȤС��Ϊ�ⶨ���ɷֵĺ���������������ʵ�飺
ʵ��1������ȡһ����������Ʒ������Ʒ�ܽ⣻�����ܽ�����Һ�м���������AgNO3��Һ�����������������������ˡ�ϴ�ӡ�����õ���ɫ����28.7g��
ʵ��2������ȡ��ʵ��1����ͬ��������Ʒ���ܽ⣻������������NaOH��Һ�������������ˡ�ϴ�Ӻ������յ��������ټ��٣��õ�����6.4g������Ʒ��FeCl3�����ʵ���Ϊ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com