
【题目】观察下列几个装置示意图,有关叙述正确的是( ) 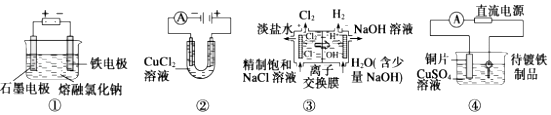
A.装置①工业上可用于生产金属钠,电解过程中石墨电极产生金属
B.装置②中阳极产生的气体可以使湿润的淀粉碘化钾试纸变蓝
C.装置③中的离子交换膜允许阳离子、阴离子和小分子水通过
D.装置④的待镀铁制品应与电源正极相连
科目:高中化学 来源: 题型:
【题目】某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作: A.用250mL容量瓶等仪器配制成250mL烧碱溶液;
B.用移液管(或碱式滴定管)量取25mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂;
C.在天平上准确称取烧碱样品W g,在烧杯中加蒸馏水溶解;
D.将物质的量浓度为M molL﹣1的标准HCl溶液装入酸式滴定管,调整液面,记下开始刻度数V1 mL;
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点耗酸体积V2 mL.
回答下列问题:
(1)正确的操作步骤是(填写字母)→→→D→
(2)滴定时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视
(3)终点时颜色变化是
(4)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有(填字母序号)
A.滴定终点读数时俯视
B.锥形瓶水洗后未干燥
C.酸式滴定管使用前,水洗后未用盐酸润洗
D.酸式滴定管在滴定前有气泡,滴定后气泡消失
(5)该烧碱样品的纯度计算式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.实验室用下图装置制取并研究SO2的性质。
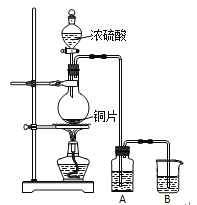
完成下列填空:
(1)圆底烧瓶中反应的化学方程式为_____________________________________。
(2)若A中盛放品红溶液,可以验证的SO2性质是______________。若要验证SO2的还原性,A中应盛放_________溶液。B中应盛放_________溶液。
II.为测定反应后的溶液中残留的硫酸浓度,实验小组进行如下探究。
(3)甲组:取1 mL反应液加水稀释至100 mL,再取10 mL稀释液与足量锌粒用下图装置进行测定。在读取反应前后量气管中液面读数时应先调节水准管与量气管中液面等高,这样操作的目的是________。
实验测得反应生成的氢气体积为22.4 mL(已换算到标准状况),计算原反应液中残留的硫酸浓度为______mol/L。

(4)乙组:欲通过加入足量的BaCl2溶液,测定生成的BaSO4沉淀质量来达到实验目的。该设计思路不可行,理由是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知气态烃A中碳的质量分数为92.3%,C与D互为同分异构体,F含有两个与乙醇相同的官能团,有关物质的转化关系如图:
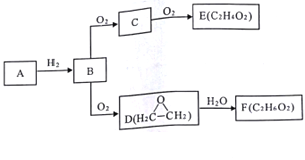
请回答:
(1)写出B的电子式___________________。
(2)C→E的反应类型___________________。
(3)D→F的化学方程式___________________。
(4)下列说法正确的是___________________。
A. 可用燃烧法鉴别A和B
B. C在一定条件下可与氢气发生还原反应
C. E和F在浓硫酸作用下加热反应,产物只有一种
D. 与D的最简式相同,相对分子质量为88的物质可能是E的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向稀硫酸溶液中逐渐加入氨水,当溶液中c(NH4+)=2c(SO42﹣)时,溶液的pH( )
A. 大于7 B. 等于7 C. 小于7 D. 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质反应后可生成 BrCH2CH2Br 的是( )
A.乙烯和溴化氢加成
B.乙烷和溴化氢光照
C.乙烯通入溴的四氯化碳溶液中
D.乙烷通入溴的四氯化碳溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空:
(1)碳酸钠溶液中各离子按照浓度从大到小的顺序依次为: .
(2)下表是几种常见弱酸的电离平衡常数(25℃)
酸 | H2CO3 | CH3COOH | HClO |
K | K1=4.4×10﹣7;K 2=4.7×10﹣11 | K=1.76×10﹣5 | K=2.95×10﹣8 |
根据分析表格中数据可知,H2CO3、CH3COOH、HClO 三种酸的酸性从强到弱依次是;25℃时,等浓度的Na2CO3、NaAc 和NaClO三种溶液的pH从小到大依次是 .
(3)常温下,将0.02molL﹣1 的 Ba(OH)2溶液100mL和0.02molL﹣1的NaHSO4溶液100mL混合,若忽略溶液体积变化,则混合后的溶液的 pH 为 .
(4)25℃时,Ksp[Mg(OH)2]=5.61×10﹣12 , Ksp[MgF2]=7.42×10﹣11 . 该温度下饱和Mg(OH)2溶液与饱和 MgF2溶液相比,(填化学式)溶液中的 c(Mg2+)大.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联合国卫生组织认为我国使用的铁锅是有益于人类健康的理想炊具。其主要原因是( )
A. 价格便宜,不易生锈 B. 铁具有银白色光泽,导电性好
C. 烹调的食物中留有人体需要的铁元素 D. 传热慢,保温性能好
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com