
【题目】能源、材料和信息是现代社会的三大“支柱”。
(1)目前,利用金属或合金储氢的研究已取得很大进展,图是一种镍基合金储氢后的晶胞结构图.
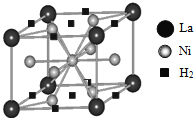
①Ni原子的价电子排布式是_____。
②该合金储氢后,含1mol La的合金可吸附![]() 的数目为_____。
的数目为_____。
(2)南师大结构化学实验室合成了一种多功能材料--对硝基苯酚水合物(化学式为![]() N
N![]() 1.5
1.5![]() O)。实验表明,加热至94℃时该晶体能失去结晶水,由黄色变成鲜亮的红色,在空气中温度降低又变为黄色,具有可逆热色性;同时实验还表明它具有使激光倍频的二阶非线性光学性质。
O)。实验表明,加热至94℃时该晶体能失去结晶水,由黄色变成鲜亮的红色,在空气中温度降低又变为黄色,具有可逆热色性;同时实验还表明它具有使激光倍频的二阶非线性光学性质。
①晶体中四种基本元素的电负性由大到小的顺序是_____。
②对硝基苯酚水合物失去结晶水的过程中,破坏的微粒间作用力是_____。
(3)科学家把NaN![]() 和N
和N![]() O在一定条件下反应得到一种白色晶体,已知其中阴离子与SO42-互为等电子体,且该阴离子中的各原子的最外层电子都满足8电子稳定结构.该阴离子的电子式是_____,其中心原子N的杂化方式是_____。
O在一定条件下反应得到一种白色晶体,已知其中阴离子与SO42-互为等电子体,且该阴离子中的各原子的最外层电子都满足8电子稳定结构.该阴离子的电子式是_____,其中心原子N的杂化方式是_____。
【答案】3d84s2 3NA O>N>C>H 氢键 ![]() sp3
sp3
【解析】
(1)①Ni是28号元素,其核外有28个电子,镍原子3d、4s能级上电子为其价电子,根据构造原理知Ni原子的价电子排布式为3d84s2,
故答案为:3d84s2 ;
②该晶胞中氢气分子个数=8×![]() + 2×
+ 2×![]() =3,La原子个数=8×
=3,La原子个数=8×![]() =1,所以该物质中氢分子和La原子个数比是3:1,则含1mol La的合金可吸附H2的数目为3NA,
=1,所以该物质中氢分子和La原子个数比是3:1,则含1mol La的合金可吸附H2的数目为3NA,
故答案为:3NA;
(2)①元素的非金属性越强其电负性越强,O、N、C、H的非金属性逐渐减弱,所以O、N、C、H的电负性逐渐减弱,则O、N、C、H的电负性由大到小的顺序是O>N>C>H,
故答案为:O>N>C>H;
②对硝基苯酚水合物之间氧原子和氢原子间存在氢键,所以对硝基苯酚水合物失去结晶水的过程中,破坏的微粒间作用力是氢键,
故答案为:氢键;
(3)原子个数相等价电子数相等的微粒属于等电子体,且等电子体结构相似,阴离子与SO42-互为等电子体,且该阴离子中的各原子的最外层电子都满足8电子稳定结构,则该离子是NO43-,其电子式为:![]() ,该离子中价层电子对= 4+
,该离子中价层电子对= 4+![]() (5+3-4×2)=4,所以N原子采用sp3杂化,
(5+3-4×2)=4,所以N原子采用sp3杂化,
故答案为: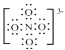 ,sp3。
,sp3。


科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种重要的消毒剂,可用ClO2为原料制取。某化学兴趣小组同学展开对漂白剂亚氯酸钠(NaClO2)的研究。
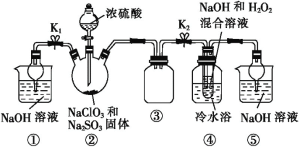
已知:饱和NaClO2溶液在温度低于38 ℃时析出的晶体是NaClO2·3H2O,高于38 ℃时析出的晶体是NaClO2,高于60 ℃时 NaClO2分解成NaClO3和NaCl。Ba(ClO2)2可溶于水。利用如图所示装置进行实验。
(1)装置①的作用是________,装置④中反应生成NaClO2的离子方程式为______ 。
(2)从装置④反应后的溶液中获得NaClO2晶体的操作步骤为:①_______,55 ℃蒸发结晶;②趁热过滤;③用38~60 ℃的温水洗涤;④___________________,得到成品。如果撤去④中的冷水浴,可能导致产品中混有的杂质是______________。
(3)设计实验检验所得NaClO2晶体是否含有杂质Na2SO4 : _______________________。
(4)为了测定NaClO2粗品的纯度,取10.0 g上述初产品溶于水配成1 L溶液,取出10 mL溶液于锥形瓶中,再加入足量酸化的KI溶液,充分反应后(NaClO2被还原为Cl-,杂质不参加反应),加入2~3滴淀粉溶液,用0.20 mol·L-1的Na2S2O3标准液滴定,达到注定终点时的现象为:_____________________________________________。重复3次,消耗Na2S2O3溶液的体积依次为:19.50 mL、20.50 mL、22.00 mL,则NaClO2粗品的纯度为_____。(提示:2Na2S2O3+I2=Na2S4O6+2NaI)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】罗氟司特是治疗慢性阻塞性肺病的特效药物,其合成中间体F的一种合成路线如下:
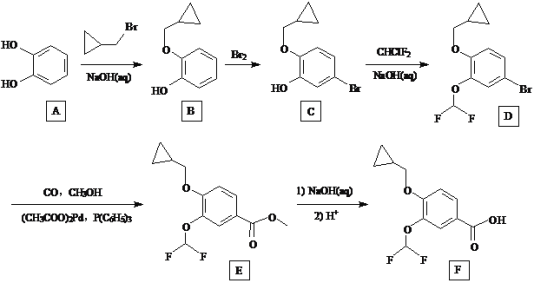
回答下列问题:
(1)A的化学名称为__________,D的分子式为__________
(2)由B生成C的化学方程式是____________。
(3)E→F的反应类型为___________,F中含氧官能团的名称为____________。
(4)上述合成路线中,有3步反应都使用NaOH溶液来提高产率,其原理是_______。
(5)![]() 的链状同分异构体有_______种(不包括立体异构),写出其中核磁共振氢谱有两组峰的结构简式:__________。
的链状同分异构体有_______种(不包括立体异构),写出其中核磁共振氢谱有两组峰的结构简式:__________。
(6)设计以对甲基苯酚为原料制备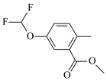 的合成路线:______(其他试剂任选)。
的合成路线:______(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】V L浓度为0.5 mol·L-1的盐酸,欲使其浓度增大1倍,采取的措施合理的是( )。
A. 通入标准状况下的HCl气体11.2V L
B. 加入10 mol·L-1的盐酸0.1V L,再稀释至1.5V L
C. 将溶液加热浓缩到0.5V L
D. 加入V L 1.5 mol·L-1的盐酸混合均匀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(![]() )广泛存在于食品中,人们对其及相关产品进行了深入研究。
)广泛存在于食品中,人们对其及相关产品进行了深入研究。
(1) ![]() (s)═
(s)═ ![]() O(g)+CO(g)+C
O(g)+CO(g)+C![]() (g)△H=+340kJmo
(g)△H=+340kJmo![]() 在密闭容器中反应,保持温度不变,下列有关选项正确的是_____(填序号)
在密闭容器中反应,保持温度不变,下列有关选项正确的是_____(填序号)
A 恒容时,容器的压强不再变化,说明该反应已达到化学平衡状态
B 恒压时,容器的体积不再变化,说明该反应已达到化学平衡状态
C 气体摩尔体积不再发生变化,说明该反应已达到化学平衡状态
D 气体平均摩尔质量不再发生变化,说明该反应已达到化学平衡状态
E 气体总质量不再发生变化,说明该反应已达到化学平衡状态
(2)草酸分解所需燃料可以是CO,通过甲烷制备CO:C![]() (g)+C
(g)+C![]() (g)→2CO(g)+2
(g)→2CO(g)+2![]() (g)△H>O.常温下,在2L的密闭容器中通入4molC
(g)△H>O.常温下,在2L的密闭容器中通入4molC![]() 气体和6molC
气体和6molC![]() 气体发生反应,5min后达到平衡,测得CO气体的浓度为0.1mol
气体发生反应,5min后达到平衡,测得CO气体的浓度为0.1mol![]() 。
。
①平衡时,该反应的平均反应速率v(C![]() )=_____mol
)=_____mol![]() mi
mi![]() 。
。
②在不改变反应混合物用量的前提下,为了提高C![]() 气体的转化率,可采取的措施是_____。(答出一方面即可)
气体的转化率,可采取的措施是_____。(答出一方面即可)
(3)草酸(![]() )是二元弱酸,KH
)是二元弱酸,KH![]() 溶液呈酸性。向10mL 0.01mol
溶液呈酸性。向10mL 0.01mol![]() 的
的![]() 溶液滴加0.01mol
溶液滴加0.01mol![]() KOH溶液V(mL),回答下列问题。
KOH溶液V(mL),回答下列问题。
①当V=10mL时,溶液中H![]() 、
、![]() 、
、![]() 、
、![]() 的浓度从大到小的顺序为_____。
的浓度从大到小的顺序为_____。
② 当V=a mL时,溶液中离子浓度有如下关系:c(![]() )=2c(
)=2c(![]() )+c(H
)+c(H![]() );当V=b mL时,溶液中离子浓度有如下关系:c(
);当V=b mL时,溶液中离子浓度有如下关系:c(![]() )=c(
)=c(![]() )+c(H
)+c(H![]() )+c(
)+c(![]() );则a_____b(填“<”,“=”或“>”)。
);则a_____b(填“<”,“=”或“>”)。
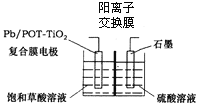
(4)电解饱和草酸溶液可以制得高档香料乙醛酸(![]() ),装置如图所示,写出复合膜电极的电极反应式_____。
),装置如图所示,写出复合膜电极的电极反应式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为19。Y原子的电子层数与最外层电子数的比等于1/3,Z原子最外层电子数与内层电子数的比为1:10。下列说法正确的是
A. 非金属性:Y<X<W
B. 简单气态氢化物的热稳定性:Y<X
C. 化合物ZW、XY中化学键类型相同
D. X、W的最高价氧化物的水化物均为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,![]() 和
和![]() 的电离常数分别为
的电离常数分别为![]() 和
和![]() 。将
。将![]() 和体积均相同的两种酸溶液分别稀释,其
和体积均相同的两种酸溶液分别稀释,其![]() 随加水体积的变化如图所示。下列叙述正确的是( )
随加水体积的变化如图所示。下列叙述正确的是( )

A. 曲线Ⅰ代表![]() 溶液
溶液
B. 溶液中水的电离程度:b点>c点
C. 从c点到d点,溶液中 保持不变(其中
保持不变(其中![]() 、
、![]() 分别代表相应的酸和酸根离子)
分别代表相应的酸和酸根离子)
D. 相同体积a点的两溶液分别与![]() 恰好中和后,溶液中
恰好中和后,溶液中![]() 相同
相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】德国化学家凯库勒研究提出的苯分子结构模型如图所示:
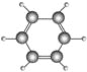
(1)请根据苯的分子结构模型,写出苯的分子式_______,结构式____________,结构简式________________。
(2)向试管中加入3 mL酸性高锰酸钾溶液,再加入1 mL苯,振荡试管。观察到的实验现象是_______________。
(3)向试管中加入1 mL溴水,再加入3 mL苯,振荡试管。观察到的实验现象是_____________。
(4)你认为凯库勒提出的苯的分子结构符合实验事实吗?________,理由是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、现象和所得结论都正确的是
选项 | 实验 | 现象 | 结论 |
A | 向滴有酚酞的 Na2CO3 溶液中加入少量氯化钡固体,振荡 | 溶液红色变浅 | Na2CO3溶液存在水解平衡 |
B | 向X溶液中滴加几滴新制氯水,振 荡 ,再加入少量KSCN溶液 | 溶液变为红色 | X溶液中一定含有Fe2+ |
C | 检验食盐是否加碘( KIO3), 取少量食盐溶于水,用淀粉碘化钾试纸检验 | 试纸不变蓝 | 该食盐不含有KIO3 |
D | 向蛋白质溶液中加入CuSO4或( NH4)2 SO4 的饱和溶液 | 均有沉淀生成 | 蛋白质均发生了盐析 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com