
【题目】固定容积为2L的密闭容器中发生反应xA(g)+yB(g)zC(g),图I表示t℃时容器中各物质的量随时间的变化关系,图II表示平衡常数K随温度变化的关系.结合图象判断,下列结论正确的是( ) 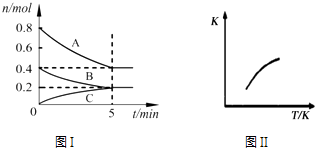
A.该反应可表示为:2A(g)+B(g)C(g)△H<0
B.t℃时该反应的平衡常数K=6.25
C.当容器中气体密度不再变化时,该反应达到平衡状态
D.t℃,在第6 min时再向体系中充入0.4 mol C,再次达到平衡时C的体积分数大于0.25
【答案】D
【解析】解:A.根据图可知A物质的量减小0.4mol,B物质的量减小0.2mol,A、B均为反应物,C物质的量增加0.2mol,为生成物,根据变化的物质的量之比等于反应中计量数之比,写出化学方程式为2A(g)+B(g)C(g),根据图Ⅱ可知,温度升高,平衡常数增大,说明正反应为吸热反应,所以热化学方程式为:2A(g)+B(g)C(g)△H>0,故A错误;B.图I中5min时达到化学平衡,平衡浓度分别为c(A)= ![]() =0.2mol/L,c(B)=
=0.2mol/L,c(B)= ![]() =0.1mol/L、c(C)=
=0.1mol/L、c(C)= ![]() =0.1mol/L,则K=
=0.1mol/L,则K= ![]() =25,故B错误;
=25,故B错误;
C.由 ![]() 可知,m不变,V不变,则ρ是定值,因此当容器中气体密度不再变化时,该反应不一定达到平衡状,故C错误;
可知,m不变,V不变,则ρ是定值,因此当容器中气体密度不再变化时,该反应不一定达到平衡状,故C错误;
D.图I中5min时,C的体积分数为 ![]() =0.25,充入0.4 mol C,虽平衡逆向移动,但C的体积分数增大,故D正确;
=0.25,充入0.4 mol C,虽平衡逆向移动,但C的体积分数增大,故D正确;
故选D.
A.根据反应物减小,生成物增加,变化的物质的量之比等于反应中计量数之比,写出化学方程式,根据图Ⅱ可知,温度升高,平衡常数增大,说明正反应为吸热反应;
B.图I中5min时达到化学平衡,根据c= ![]() 平衡浓度,带入K表达式计算;
平衡浓度,带入K表达式计算;
C.由 ![]() 可知,m不变,V不变,则ρ是定值;
可知,m不变,V不变,则ρ是定值;
D.图I中5min时,C的体积分数为 ![]() =0.25,充入0.4 mol C,条件的改变大于平衡移动的改变.
=0.25,充入0.4 mol C,条件的改变大于平衡移动的改变.


科目:高中化学 来源: 题型:
【题目】肉桂酸甲酯是调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精,用于肥皂、洗涤剂、风味剂和糕点的调味,在医药工业中作为有机合成的中间体.合成肉桂酸甲酯的工业流程如图所示: 
已知:
I.醛与醛能发生反应,原理如下:![]() +CH3CHO
+CH3CHO ![]()
![]()
![]() RCH=CHCHO
RCH=CHCHO
Ⅱ.烃A在标准状况下的密度为1.25g/L.
请回答:
(1)化合物H中的官能团为;
(2)肉桂酸甲酯的结构简式为;J的结构简式为;
(3)G→H的反应类型为;
(4)写出反应B→C的化学方程式;H→I的反应(填“能”或“不能”)改用酸性高锰酸钾溶液,简述理由: .
(5)符合下列条件的I的同分异构体共有5种.写出另两种同分异构体的结构简式: A.能发生水解反应 B.与银氨溶液作用出现光亮的银镜 C.能与溴发生加成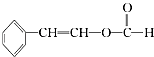 、
、 ![]() 、、 .
、、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中,能在溶液中大量共存的是( )
A. H+、NO3-、Cl-、Fe2+B. Na+、Mg2+、SO42-、OH-
C. Cu2+、Ba2+、NO3-、CO32-D. K+、Na+、OH-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚砜(SOCl2)为无色或浅黄色发烟液体,易挥发,遇水反应,其制取过程的相关反应如下:S(s)+Cl2(g) ![]() SCl2(l) (Ⅰ)
SCl2(l) (Ⅰ)
SCl2(l)+SO3(l)═SOCl2(l)+SO2(g)(Ⅱ)
已知二氯化硫(SCl2)熔点﹣78°C,沸点59°C,如图是实验室由氯气与硫合成二氯化硫的装置.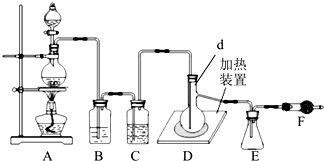
(1)仪器组装完成后,检查装置气密性的操作是;反应前要先排尽系统中空气,此做法目的是 .
(2)装置D中玻璃仪器d的名称是 , 向其中放入一定量的硫粉,加热使之融化,轻轻摇动使硫附着在容器的内壁,形成一薄层膜,这样做的优点是 .
(3)实验时,为防止E中液体挥发,可采取的措施是 . 装置F(盛放碱石灰)的作用是 , .
(4)工业上以硫黄、液氯和液体三氧化硫为原料,能生产高纯度(99%以上)氯化亚砜,为使原子的利用率达到100%,三者的物质的量比为;已知:SOCl2+4NaOH═Na2SO3+2NaCl+2H2O.
供选择的试剂:稀盐酸、稀硝酸、氯化钡溶液、硝酸银溶液、品红溶液请设计简单的实验来验证氯化亚砜与水完全反应的产物,简要说明实验操作、现象和结论 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蓄电池放电时是起原电池的作用,在充电时起电解池的作用.下式是爱迪生蓄电池分别在充电、放电时的反应:Fe+NiO2+2H2O ![]() Fe(OH)2+Ni(OH)2 , 下列有关爱迪生电池的各种推断中错误的是( )
Fe(OH)2+Ni(OH)2 , 下列有关爱迪生电池的各种推断中错误的是( )
A.放电时铁做负极,NiO2做正极
B.充电时阴极上的电极反应为:Fe(OH)2+2e﹣═Fe+2OH﹣
C.放电时,电解质溶液中的阴离子是向正极方向移动
D.蓄电池的两个电极必须浸入在碱性溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g)C(g)+D(g)过程中的能量变化如图所示,下列说法正确的是( ) 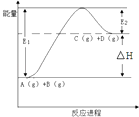
A.该反应是放热反应
B.加入催化剂后,反应加快,△H减小
C.反应物的总键能小于生成物的总键能
D.反应达到平衡时,升高温度,A的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于同温同压下等体积的CO2和CO的叙述:①质量相等 ②密度相等 ③所含分子数相等 ④所含原子个数相等,其中正确的是( )
A. ③ B. ②③④ C. ③④ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学学习小组在帮助老师整理实验室的化学试剂时,发现一瓶无色溶液,标签破损如下图,据老师回忆,该药品应该是中学化学常用试剂。该小组同学根据已掌握的知识,对溶液进行鉴定。下列说法错误的是
A. 该小组同学推测它的阳离子可能是H+、Na+、K+、NH4+中的某一个
B. 若要证明阳离子是否为NH4+,其方法是: 取少量溶液于试管中加稀NaOH溶液,若产生能使湿润的红色石蕊试纸变蓝的气体,则阳离子为NH4+
C. 某同学操作时不慎将一滴溶液滴落在纸上,纸变黑,说明该溶液为浓硫酸
D. 验证阳离子是否为Na+或者K+的实验方法是焰色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】催化技术可处理汽车尾气:2NO+2CO2CO2+N2 , 某温度下在容积不变的密闭容器中通入NO 和CO,不同时间NO 和CO 的浓度如下表.下列说法中不正确的是( )
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/×10﹣3molL﹣1 | 1.00 | 0.45 | 0.25 | 0.15 | 0.10 | 0.10 |
c(CO)/×10﹣3molL﹣1 | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
A.2 s 内的平均反应速率υ(N2)=1.875×10﹣4 molL﹣1s﹣1
B.在该温度下K=5
C.若将容积缩小为原来的一半,NO 转化率大于90%
D.某时刻再充入0.1 mol NO,0.36 mol CO,重新达平衡后CO 浓度比原平衡大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com