
����Ŀ��A��B��C��D��E��Ϊ������Ԫ�أ�ԭ������������������ݱ�����Ϣ�ش��������⣺
Ԫ�� | Ԫ�����ʻ�ṹ |
A | ���������������ڲ��������2�� |
B | BԪ�صĵ����ڿ����к������ |
C | CԪ���ڵؿ��к������ |
D | DԪ����ͬ�����н�������ǿ |
E | ���³�ѹ�£�EԪ���γɵĵ����ǵ���ɫ���壬���ڻ�ɽ�ڸ������� |
��1��E��Ԫ�����ڱ��е�λ��_____________��
��2��D������������ˮ�������ʽ___________��������ѧ������____________��
��3��B��C��D��E�����Ӱ뾶�ɴ�С˳��Ϊ_____________�������ӷ��ű�ʾ����
��4����A��B��C����Ԫ����ɵ�һ�ֳ�����ʽ�������D������������ˮ���ﷴӦ�����ӷ���ʽ��_____________________________��
���𰸡��������ڵڢ�A�� ![]() ���Ӽ������ۼ� S2->N3->O2->Na+ NH4++HCO3-+2OH-��NH3��H2O+CO32-+H2O
���Ӽ������ۼ� S2->N3->O2->Na+ NH4++HCO3-+2OH-��NH3��H2O+CO32-+H2O
��������
A��B��C��D��E��Ϊ������Ԫ�أ���ԭ��������������A���������������ڲ��������2����ԭ��ֻ����2�����Ӳ㣬����������Ϊ4����AΪ̼Ԫ��;BԪ�صĵ����ڿ����к�����࣬��BΪNԪ��;CԪ���ڵؿ��к�����࣬��CΪOԪ��;DԪ����ͬ�����н�������ǿ��ԭ�����������������ڵ�������IA�壬��DΪNa;���³�ѹ�£�EԪ���γɵĵ����ǵ���ɫ���壬���ڻ�ɽ�ڸ�����������EΪSԪ�ء�
(1)EΪ��Ԫ�أ���Ԫ�����ڱ��е�λ��:�������ڵ���A�壬��ˣ�������ȷ����:�������ڵ���A��;
(2) Na������������ˮ�������������ƣ�����ʽΪ![]() ��������ѧ�����������Ӽ����ۼ���
��������ѧ�����������Ӽ����ۼ���
(3)���Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС�����Ӳ�Խ�����Ӱ뾶Խ�����Ӱ뾶: S2->N3->O2->Na+
(4)��C��N��O��HԪ����ɵ�һ�ֳ�������ʽ��ΪNH4HCO3��D������������Ӧ��ˮ����ΪNaOH��̼������������NaOH��Ӧ�����ӷ���ʽΪ: NH4++HCO3-+2OH-��NH3��H2O+CO32-+H2O



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ϼ�G�����������кܶ���;,��ϳ�·������:

��֪:��R1��CHO+R2��CH2��CHO![]()
![]() (R1��R2������������ԭ��)
(R1��R2������������ԭ��)
��D��A��Ϊͬϵ��;����ͬ������,D����������������ܶ�Ϊ39��
(1)A��������____,G�к��������ŵ�������____��
(2)�ڵķ�Ӧ������____,B��F�Ľṹ��ʽ�ֱ�Ϊ______��______��
(3)д��һ���ܼ���A��D���Լ�:______;C�ж���ͬ���칹��,�������ڷ����廯�������____�֡�
(4)д����Ӧ�ٵĻ�ѧ����ʽ:_____________��
(5)G��ͬ���칹�� ��һ����Ҫ��ҩ���м���,��ϳ�·����G����,����
��һ����Ҫ��ҩ���м���,��ϳ�·����G����,����![]() Ϊԭ��������ĺϳ�·��(��������ԭ����ѡ)_________��
Ϊԭ��������ĺϳ�·��(��������ԭ����ѡ)_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.�����ϩ��![]() ������������ԭ�ӹ�ƽ��
������������ԭ�ӹ�ƽ��
B.ͬ����Ԫ�غ������������˵���������Ӷ�����
C.������������ˮ������������۵�ϸߣ���Ҫԭ��������й�
D.NO![]() ��������ԭ���ϵŵ��Ӷ�����0�����幹��Ϊƽ��������
��������ԭ���ϵŵ��Ӷ�����0�����幹��Ϊƽ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼����[La2(CO3)3]���������Ƹ�������Ѫ֢��ij��ѧС������ͼװ��ģ���Ʊ�̼���磬��ӦΪ2LaCl3+6NH4HCO3=La2(CO3)3��+6NH4Cl+3CO2��+3H2O������˵����ȷ���ǣ� ��
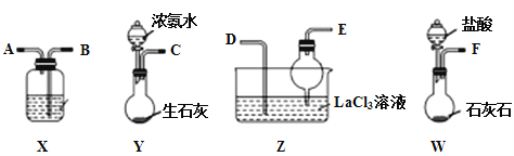
A.�������ҽӿڵ�����˳��F��B��A��D��E��C
B.װ��X��ʢ�ŵ��Լ�Ϊ����Na2CO3��Һ
C.װ��Z���ø���ܵ���ҪĿ��������Ӵ�������ӿ������ܽ�
D.ʵ�鿪ʼʱӦ�ȴ�Y�з�Һ©������ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѹ���ʻ�������������ԭ��Ϊ��Ni(s)+4CO(g)![]() Ni(CO)4(g)��230��ʱ���÷�Ӧ��ƽ�ⳣ��K=2��10-5����֪��Ni(CO)4�ķе�Ϊ42.2�棬�������ʲ����뷴Ӧ��
Ni(CO)4(g)��230��ʱ���÷�Ӧ��ƽ�ⳣ��K=2��10-5����֪��Ni(CO)4�ķе�Ϊ42.2�棬�������ʲ����뷴Ӧ��
��һ�Σ���������CO��Ӧת������̬Ni(CO)4��
�ڶ��Σ�����һ�η�Ӧ���������������������230���Ƶøߴ����������ж���ȷ���ǣ� ��
A.�����¶ȣ��÷�Ӧ��ƽ�ⳣ����С
B.�÷�Ӧ�ﵽƽ��ʱ��v����[Ni(CO)4]=4v����(CO)
C.��һ�Σ���30���50������֮��ѡ��Ӧ�¶ȣ�ѡ50��
D.�ڶ��Σ�Ni(CO)4�ֽ��ʽϵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2O2���ȶ����ֽ⣬Fe3����Cu2���ȶ���ֽ�������ã�Ϊ�Ƚ�Fe3����Cu2����H2O2�ֽ�Ĵ�Ч����ij��ѧ�о�С��ͬѧ�ֱ��������ͼ�ס�������ʵ��װ�á�
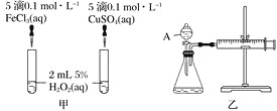
��1��������ͼ��װ�ã���ͨ���۲�__________���Ӷ����ԱȽϵó����ۡ�
��2����ͬѧ�����FeCl3��ΪFe2(SO4)3��Ϊ�������������� ________��д��H2O2�ڶ������̴������·�����Ӧ�Ļ�ѧ����ʽ��___________��
��3����������ʵ��ɽ��ж���������ͼ��������A������Ϊ________��ʵ��ʱ��������40mL����Ϊ����������Ӱ��ʵ������ؾ��Ѻ��ԣ�ʵ���л���Ҫ������������________��
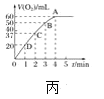
��4����0.1molMnO2��ĩ����50 mL H2O2��Һ�У��ڱ�״���·ų�����������ʱ��Ĺ�ϵ��ͼ����ʾ�����ͷ�Ӧ���ʱ仯��ԭ��________��H2O2��ʼ���ʵ���Ũ��Ϊ_______(������λС��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ߴ���������Ϊ�ϳ���������Ԫ�������ϵ�ԭ�ϣ���ҵ�Ͽ�����Ȼ�������̷������̿���Fe��Al��Mg��Zn��Ni��Si��Ԫ�أ��Ʊ�����������ͼ��ʾ���ش��������⣺
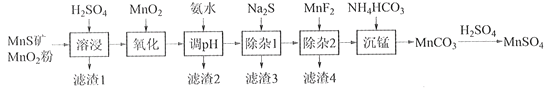
��ؽ�������[c0(Mn+)=0.1 mol��L1]�γ��������������pH��Χ���£�
�������� | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
��ʼ������pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
������ȫ��pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
��1��������1������S��__________________________��д�����ܽ����ж������������̷�Ӧ�Ļ�ѧ����ʽ____________________________________________________��
��2����������������������MnO2�������ǽ�________________________��
��3������pH��������������Һ��pH��ΧӦ����Ϊ_______~6֮�䡣
��4��������1����Ŀ���dz�ȥZn2+��Ni2+��������3������Ҫ�ɷ���______________��
��5��������2����Ŀ��������MgF2������ȥMg2+������Һ��ȹ��ߣ�Mg2+��������ȫ��ԭ����_____________________________________________________________________��
��6��д���������������ӷ���ʽ___________________________________________________��
��7����״��������Ԫ���Ͽ���Ϊ����ӵ���������ϣ��仯ѧʽΪLiNixCoyMnz2������Ni��Co��Mn�Ļ��ϼ۷ֱ�Ϊ+2��+3��+4����x=y=![]() ʱ��z=___________��
ʱ��z=___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ѱ�(TiO2)��Ϊ��ɫ���Ϻ��������㷺�������ᡢ��ֽ�ȹ�ҵ�����С�һ����������(��FeTiO3��������CaO��Fe2O3��SiO2)Ϊԭ�������Ѱ۵Ĺ���������ͼ��
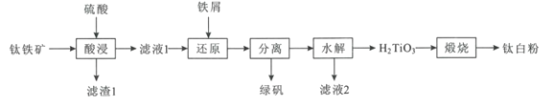
�ش��������⣺
(1)������������������¶�Ϊ150~200������������������Һ1���е���Ҫ�ɷ��к���TiOSO4���������������Ҫ�����ķ�Ӧ����ʽΪ___��
(2)������1������Ҫ�ɷ���___��
(3)����ԭ"�м��������м��Ŀ����___��
(4)��������������ܽ�����±���ʾ�������̷�(FeSO4��7H2O)���ױ������������������õ��̷��IJ���Ϊ___��
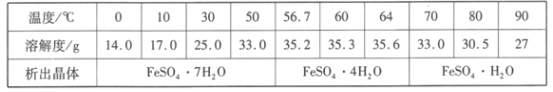
(5)��ˮ������Ҫ������90���Ŀ����___��
(6)����Һ2���ɷ��ص�___����ѭ�����á�
(7)��ҵ�Ͻ��Ѱ��뽹̿��������������TiCl4��һ�ֿ�ȼ���壬��Ӧ�Ļ�ѧ����ʽΪ___������������Χ�ͼ��ȵ��������ý���þ��ԭTiCl4��ȡ������Խ�Ľ����ѡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڵؿ���SiO2��HF��������ƽ�⣺SiO2(s)+4HF(g)![]() SiF4(g)+2H2O(g)����H= +148.9 kJ�����������Ӧ�����������ܱ������з���������Ӧ�ﵽƽ��ʱ��()
SiF4(g)+2H2O(g)����H= +148.9 kJ�����������Ӧ�����������ܱ������з���������Ӧ�ﵽƽ��ʱ��()
A.2v(����HF)=v(�桢H2O)B.v(H2O)=2v(SiF4)
C.SiO2���������ֲ���D.��Ӧ�ﲻ��ת��Ϊ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com