
【题目】常温下,用0.1molL﹣1的CH3COOH溶液滴定20mL 0.1molL﹣1的NaOH溶液,当滴加VmLCH3COOH溶液时,混合溶液的pH=7.已知CH3COOH的电离平衡常数为Ka,忽略混合时溶液体积的变化,下列关系式正确是( )
A.Ka=![]() B.V=
B.V=![]()
C.Ka=![]() D.Ka=
D.Ka=![]()
【答案】A
【解析】
试题分析:当滴加VmLCH3COOH溶液时,混合溶液的pH=7,此时溶液中c(OH﹣)=c(H+)=10﹣7mol/L,由电荷守恒c(Na+)=c(CH3COO﹣)=![]() mol/L,根据物料守恒c(CH3COO﹣)+c(CH3COOH)=
mol/L,根据物料守恒c(CH3COO﹣)+c(CH3COOH)=![]() mol/L,联立计算c(CH3COOH),CH3COOH的电离平衡常数为Ka=
mol/L,联立计算c(CH3COOH),CH3COOH的电离平衡常数为Ka=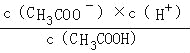 ,代入Ka表达式进行计算.
,代入Ka表达式进行计算.
解:当滴加VmLCH3COOH溶液时,混合溶液的pH=7,此时溶液中c(OH﹣)=c(H+)=10﹣7mol/L,
由电荷守恒:c(OH﹣)+c(CH3COO﹣)=c(H+)+c(Na+),可知c(Na+)=c(CH3COO﹣)=![]() =
=![]() mol/L,
mol/L,
根据物料守恒c(CH3COO﹣)+c(CH3COOH)=![]() mol/L,则c(CH3COOH)=(
mol/L,则c(CH3COOH)=(![]() ﹣
﹣![]() )mol/L=
)mol/L=![]() mol/L,
mol/L,
CH3COOH的电离平衡常数为Ka= =
= =
=![]() ,则V=
,则V=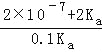 ,
,


科目:高中化学 来源: 题型:
【题目】I.被誉为改变未来世界的十大新科技之一的燃料电池。 右图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.

试回答下列问题:
(1)燃料电池的优点是________;电解质溶液中的OH-移向______极(填“负”或“正”).
(2)写出氢氧燃料电池工作时正极反应式:_______________________。
(3)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为___________.
(4)利用该装置可以处理氮的氧化物和NH3 尾气,总反应为:6NO2 +8NH3=7N2+12H2O,负极反应式为__________。
II.将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为80 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为41g,试计算:
(1)产生氢气的体积(标准状况)为________________;
(2)通过导线的电子数为__________(用NA表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各图的叙述,正确的是
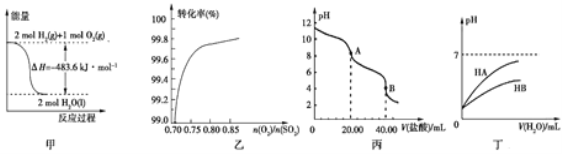
A. 图甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6 kJ·mol-1
B. 图乙表示反应2SO2(g)+O2(g)![]() 2SO3(g)在其他条件不变时,O2的转化率随
2SO3(g)在其他条件不变时,O2的转化率随![]() 的变化关系
的变化关系
C. 图丙表示用0.100 0 mol·L-1的盐酸滴定20.00 mL 0.100 0 mol·L-1Na2CO3溶液的曲线,从A点到B点反应的离子方程式为:CO32-+2H+![]() CO2↑+H2O
CO2↑+H2O
D. 图丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液的pH随加水量的变化,则同浓度溶液的pH:NaA<NaB
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铝合金中含有元素:铝、镁、铜、碳,为测定该合金中铝的含量。
Ⅰ 甲同学设计如下实验:
(1)称取样品a g(精确到0.1 g),溶于足量稀盐酸,过滤。
(2)向步骤(1)所得滤液中加入过量的氢氧化钠溶液,过滤并洗涤滤渣。有关反应的离子方程式是_________________________________、____________________________________________。
(3)向步骤(2)所得滤液中通入过量的二氧化碳气体,过滤并洗涤滤渣。有关反应的离子方程式是_________________________________、____________________________________________。
(4)将步骤(3)所得的滤渣烘干并灼烧至恒重、冷却后称量,其质量为b g。有关反应的化学方程式是_________________________________。原样品中铝的质量分数是__________。
Ⅱ 乙同学认为也可以向一定质量的样品中直接加足量氢氧化钠溶液充分反应后,将剩余固体过滤、洗涤、干燥后称量,即可计算该合金中铝的含量。有关反应的离子方程式是____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】艾司洛尔是预防和治疗手术期心动过速或高血压的一种药物,艾司洛尔的一种合成路线如下:
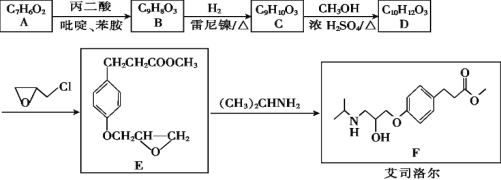
回答下列问题:
(1)丙二酸的结构简式为_______;E中含氧官能团的名称是_______。
(2)D生成E的反应类型为____________。
(3)C的结构简式为________________。
(4)A遇FeCl3溶液发生显色反应,1 mol A和1 mol丙二酸在吡啶、苯胺中反应生成1 mol B、1 mol H2O和1 mol CO2,B能与溴水发生加成反应,推测A生成B的化学方程式为____。
(5)X是B的同分异构体,X同时满足下列条件的结构共有____种,其中核磁共振氢谱有五组峰的结构简式为____。
①可与碳酸氢钠溶液反应生成二氧化碳
②遇FeCl3溶液发生显色反应
③除苯环外不含其他环
(6)写出以苯甲醇和丙二酸为原料制备![]() 的合成路线________(其他试剂任选)。
的合成路线________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 用坩埚灼烧MgCl2·6H2O的化学方程式为:MgCl2·6H2O![]() MgCl2+6H2O
MgCl2+6H2O
B. 根据表中提供的数据,等物质的量浓度的NaClO、NaHCO3 混合溶液中,有c(HCO![]() )>c(ClO-)>c(OH-)
)>c(ClO-)>c(OH-)

C. 常温下,将pH=2的稀硫酸稀释10倍,其中各离子的物质的量浓度都变为原来的十分之一
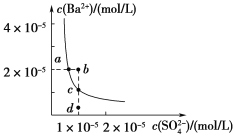
D. 某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示,溶度积常数Ksp=c(Ba2+)·c(SO![]() ),则加入Na2SO4可使溶液由a点变到b点;通过蒸发可以使溶液由d点变到c点
),则加入Na2SO4可使溶液由a点变到b点;通过蒸发可以使溶液由d点变到c点
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在一个2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
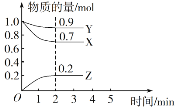
(1)该反应的化学方程式为_______________。
(2)反应开始至2 min,以气体Z表示的平均反应速率为________。
(3)可以判断上述反应已经达到平衡的是________。
A.v(A)∶v (B)∶v (C)等于化学计量数之比
B.密闭容器中总压强不变 C.密闭容器中混合气体的密度不变
D.混合气体的平均相对分子质量不再改变 E.n(A)∶n(B)∶n(C)等于化学计量数之比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是 ( )

A. ③中选用NaOH溶液吸收多余的SO2
B. 上下移动①中铜丝可控制SO2的量
C. ②中选用品红溶液验证SO2的生成
D. 为确认CuSO4生成,向①中加水,观察颜色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com