
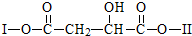 (其中I、II为未知部分的结构)为推测X的分子结构,进行如图的转化:
(其中I、II为未知部分的结构)为推测X的分子结构,进行如图的转化: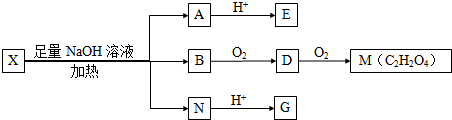
 ,可知B为HOCH2CH2OH,则D为OHC-CHO,G为
,可知B为HOCH2CH2OH,则D为OHC-CHO,G为 ,E的结构应为:
,E的结构应为: ,X结构简式为
,X结构简式为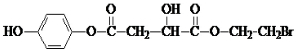 ,据此解答.
,据此解答. ,可知B为HOCH2CH2OH,则D为OHC-CHO,G为
,可知B为HOCH2CH2OH,则D为OHC-CHO,G为 ,E的结构应为:
,E的结构应为: ,X结构简式为
,X结构简式为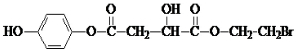 ,
, ,分子所含官能团的名称是:羧基、羟基,故答案为:HOOC-COOH;羧基、羟基;
,分子所含官能团的名称是:羧基、羟基,故答案为:HOOC-COOH;羧基、羟基; ,含有苯环,可以与氢气发生加成反应,属于酚类,易被氧化,可以发生取代反应,不能发生消去反应,故答案为:b;
,含有苯环,可以与氢气发生加成反应,属于酚类,易被氧化,可以发生取代反应,不能发生消去反应,故答案为:b;| 催化剂 |
| △ |
| 催化剂 |
| △ |
 ,在一定条件下发生反应生成分子组成为C4H4O4的有机物,该有机物可使溴的四氯化碳溶液褪色,含有不饱和键,故为羟基发生消去反应生成生成HOOC-CH=CH-COOH,反应方程式为
,在一定条件下发生反应生成分子组成为C4H4O4的有机物,该有机物可使溴的四氯化碳溶液褪色,含有不饱和键,故为羟基发生消去反应生成生成HOOC-CH=CH-COOH,反应方程式为
| 一定条件 |

| 一定条件 |
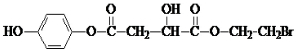 ,
,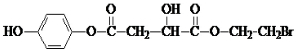 ;
; 互为同分异构体,F的分子中只含有羧基、羟基和醛基三种官能团,且同一个碳原子上不能同时连有两个羟基,则结构中含有1个羧基、1个醛基和2个羟基,分别连接在3个碳原子上,可能的结构有
互为同分异构体,F的分子中只含有羧基、羟基和醛基三种官能团,且同一个碳原子上不能同时连有两个羟基,则结构中含有1个羧基、1个醛基和2个羟基,分别连接在3个碳原子上,可能的结构有 ,故答案为:2种.
,故答案为:2种.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
A、向NH4HCO3溶液中加入过量的Ba(OH)2溶液并加热:Ba2++2OH-+NH4++HCO3-
| ||||
| B、用白醋除铁锈:Fe2O3+6H+═3H2O+2Fe3+ | ||||
| C、次氯酸钠溶液中通入过量二氧化硫:ClO-+H2O+SO2=HClO+HSO3- | ||||
D、用惰性电极电解饱和MgCl2溶液:2Cl-+2H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径大小顺序为:E>D>C>B>A |
| B、A、B、C、D四种元素都属于非金属元素,它们之间只能形成共价化合物 |
| C、B、C、D、E四种元素与A 元素形成的最简单化合物的沸点依次升高 |
| D、D与A、E均可形成具有强氧化性的化合物,可用于城市自来水的杀菌消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
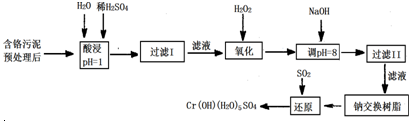
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
| pH | 3.7 | 9.6 | 11.1 | 8 | 9(>9溶解) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| NaOH/g | 109 | 118 | 129 | 146 | 177 | 300 | 313 | 318 | 337 |
| NaCl/g | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、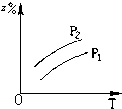 |
B、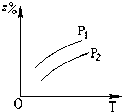 |
C、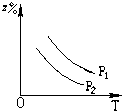 |
D、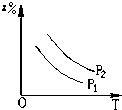 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com