
ЎҫМвДҝЎҝДіСРҫҝРФС§П°РЎЧй¶ФВБИИ·ҙУҰКөСйХ№ҝӘСРҫҝЎЈПЦРРёЯЦР»ҜС§ҪМІДЦР¶ФЎ°ВБИИ·ҙУҰЎұөДПЦПуУРХвСщөДГиКцЈәЎ°·ҙУҰ·ЕіцҙуБҝөДИИЈ¬Іў·ўіцТ«СЫөД№вГўЎұЎўЎ°ЦҪВ©¶·өДПВІҝұ»ЙХҙ©Ј¬УРИЫИЪОпВдИлЙіЦРЎұЎЈІйФДЎ¶»ҜС§КЦІбЎ·ЦӘЈ¬AlЎўAl2O3ЎўFeЎўFe2O3ИЫөгЎў·РөгКэҫЭИзПВЈә
ОпЦК | Al | Al2O3 | Fe | Fe2O3 |
ИЫөг/Ўж | 660 | 2054 | 1535 | 1462 |
·Рөг/Ўж | 2467 | 2980 | 2750 | -- |
ўсЈ®ЈЁ1Ј©ДіН¬С§НЖІвЈ¬ВБИИ·ҙУҰЛщөГөҪөДИЫИЪОпУҰКЗМъВБәПҪрЎЈАнУЙКЗЈәёГ·ҙУҰ·ЕіцөДИИБҝК№МъИЫ»ҜЈ¬¶шВБөДИЫөгұИМъөНЈ¬ҙЛКұТәМ¬өДМъәНВБИЫәПРОіЙМъВБәПҪрЎЈДгИПОӘЛыөДҪвКНКЗ·сәПАнЈҝҙрЈә_____ ЈЁМоЎ°әПАнЎұ»тЎ°І»әПАнЎұЈ©
ЈЁ2Ј©ЙијЖТ»ёцјтөҘөДКөСй·Ҫ°ёЈ¬ЦӨГчЙПКцЛщөГөДҝйЧҙИЫИЪОпЦРә¬УРҪрКфВБЎЈёГКөСйЛщУГКФјБКЗ_____ Ј¬·ҙУҰөДАлЧУ·ҪіМКҪОӘ____ __ЎЈ
ЈЁ3Ј©КөСйКТИЬҪвёГИЫИЪОпЈ¬ПВБРКФјБЦРЧоәГөДКЗ___ ___ЈЁМоРтәЕЈ©ЎЈ
AЈ®ЕЁБтЛб BЈ®ПЎБтЛб CЈ®ПЎПхЛб DЈ®ЗвСх»ҜДЖИЬТә
ўтЈ®КөСйСРҫҝ·ўПЦЈ¬ПхЛб·ўЙъСх»Ҝ»№Фӯ·ҙУҰКұЈ¬ПхЛбөДЕЁ¶ИФҪПЎЈ¬¶ФУҰ»№ФӯІъОпЦРөӘФӘЛШөД»ҜәПјЫФҪөНЎЈДіН¬С§ИЎТ»¶ЁБҝЙПКцөДИЫИЪОпУлТ»¶ЁБҝәЬПЎөДПхЛбід·Ц·ҙУҰЈ¬·ҙУҰ№эіМЦРОЮЖшМе·ЕіцЎЈФЪ·ҙУҰҪбКшәуөДИЬТәЦРЈ¬ЦрөОјУИл4molL-1өДЗвСх»ҜДЖИЬТәЈ¬ЛщјУЗвСх»ҜДЖИЬТәөДМе»эЈЁmLЈ©УлІъЙъөДіБөнөДОпЦКөДБҝЈЁmolЈ©өД№ШПөИзНјЛщКҫЎЈКФ»ШҙрПВБРОКМвЈә
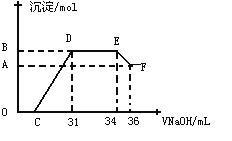
ЈЁ4Ј©НјЦРOC¶ОГ»УРіБөнЙъіЙЈ¬ҙЛҪЧ¶О·ўЙъ·ҙУҰөДАлЧУ·ҪіМКҪОӘ______ЎЈ
ЈЁ5Ј©ФЪDE¶ОЈ¬іБөнөДОпЦКөДБҝГ»УРұд»ҜЈ¬ФтҙЛҪЧ¶О·ўЙъ·ҙУҰөДАлЧУ·ҪіМКҪОӘ Ј¬ЙПКцПЦПуЛөГчИЬТәЦР____ҪбәПOHЎӘөДДЬБҰұИ______ЗҝЈЁМоАлЧУ·ыәЕЈ©ЎЈ
ЈЁ6Ј©Bөг¶ФУҰөДіБөнөДОпЦКөДБҝОӘ____ __molЈ¬Cөг¶ФУҰөДЗвСх»ҜДЖИЬТәөДМе»эОӘ____ __mLЎЈ
Ўҫҙр°ёЎҝўсЈЁ1Ј©әПАнЈЁ1·ЦЈ© ЈЁ2Ј©NaOHИЬТәЈЁ1·ЦЈ©Ј»2Al+2OHЎӘ+H2O=2AlO2ЎӘ+3H2ЎьЈЁ2·ЦЈ©Ј»
ЈЁ3Ј©BЈЁ2·ЦЈ©Ј»ўтЈЁ4Ј©H++OHЎӘЁTH2O ЈЁ2·ЦЈ© ЈЁ5Ј©NH4++OHЎӘЁTNH3H2OЈЁ2·ЦЈ©Ј» Al3+ЎўFe3+ЎўH+ЈЁ1·ЦЈ©Ј» NH4+ЈЁ1·ЦЈ©Ј» ЈЁ6Ј©0.032ЈЁ2·ЦЈ©Ј»7ЈЁ2·ЦЈ©ЎЈ
ЎҫҪвОцЎҝ
КФМв·ЦОцЈәўсЈЁ1Ј©ВБөДИЫөгұИМъөНЈ¬ЙъіЙМъәНТәМ¬ВБТ»ЖрөОВдөҪКўУРЙіЧУөДИЭЖчЦРРОіЙәПҪрЈ¬ЛщТФВБИИ·ҙУҰЛщөГөҪөДИЫИЪОпКЗМъВБәПҪрЈ¬ЛщТФәПАнЎЈ
ЈЁ2Ј©ВБәНЗвСх»ҜДЖИЬТә·ҙУҰЙъіЙЖшМеЈ¬ЛщТФҝЙТФУГЗвСх»ҜДЖјмСйЛщөГөДИЫИЪОпЦРКЗ·сә¬УРВБЈ¬·ҙУҰ·ҪіМКҪОӘ2Al+2OHЎӘ+H2O=2AlO2ЎӘ+3H2ЎьЈ»
ЈЁ3Ј©AЎўЕЁБтЛбТЧК№МъВБ¶Ы»ҜЈ¬І»ДЬК№әПҪрИЬҪвЈ¬ҙнОуЈ»BЎў»оЖГҪрКфУлПЎБтЛб·ҙУҰЈ¬ИЫИЪОпҝЙИЬҪвУЪПЎБтЛбЦРЈ¬ХэИ·Ј»CЎўПЎПхЛбУлҪрКф·ҙУҰЙъіЙОЫИҫРФЖшМеЈ¬І»КЗЧојССЎФсЈ¬ҙнОуЈ»DЎўМъІ»УлЗвСх»ҜДЖ·ҙУҰЈ¬І»ДЬҪ«ИЫИЪОпИ«ІҝИЬҪвЈ¬ҙнОуЎЈЛщТФСЎBЎЈ
ўтЈЁ4Ј©OЎъCЦ®јд·ўЙъөД·ҙУҰКЗЛбјоЦРәН·ҙУҰЈ¬АлЧУ·ҪіМКҪОӘH++OHЎӘЁTH2O ЎЈ
ЈЁ5Ј©DEТ»¶ОіБөнөДЦКБҝГ»УРұд»ҜЈ¬ёГ·ҙУҰОӘп§ёщАлЧУУлЗвСхёщАлЧУҪбәПЙъіЙТ»Л®әП°ұЈ¬·ҪіМКҪОӘNH4++OHЎӘЁTNH3H2OЈ»ЙПКцПЦПуЛөГчИЬТәЦРЧоПИҪбәПЗвСхёщАлЧУөДКЗЗвАлЧУЈ¬И»әуОӘВБАлЧУәНМъАлЧУЈ¬ЧоәуҪбәПЗвСхёщАлЧУөДКЗп§ёщАлЧУЈ¬ЛщТФИЬТәЦРөДАлЧУҪбәПЗвСхёщАлЧУөДДЬБҰЧоЗҝөДКЗЗвАлЧУЈ¬ЧоИхөДОӘп§ёщАлЧУЎЈ
ЈЁ6Ј©УЙНјҝЙЦӘЈ¬EF¶ППыәДөДЗвСх»ҜДЖИЬТәОӘ36-34=2mLЈ¬ёГјЖЛгІОјы·ҙУҰөДЗвСх»ҜДЖөДОпЦКөДБҝОӘ0.002ЎБ4=0.008molЈ¬ёщҫЭ·ҪіМКҪјЖЛгЈ¬ЗвСх»ҜВБөДОпЦКөДБҝОӘ0.008ДҰ¶ыЈ¬ФтҪрКф»мәПОпЦРВБОӘ0.008ДҰ¶ыЈ¬ЙиМъОӘxmolЈ¬ВБОӘ0.008molЈ¬ЙъіЙөДПхЛбп§ОӘЈЁ34-31Ј©ЎБ0.001ЎБ4=0.012molЈ¬УЙУЪПхЛб№эБҝЈ¬Мъ·ҙУҰЙъіЙПхЛбМъЈ¬УЙөзЧУКШәг·ЦОцЈ¬3x+0.008ЎБ3=0.012ЎБ3 x=0.024molЈ¬јҙ·ҙУҰЙъіЙЗвСх»ҜМъөДОпЦКөДБҝОӘ0.024molЈ¬ЙъіЙіБөнөДЧЬОпЦКөДБҝОӘ0.008+0.024=0.032molЈ»өОјУЗвСх»ҜДЖМе»эОӘ31mLКұЈ¬ЗвАлЧУәНВБАлЧУәНМъАлЧУ¶ј·ҙУҰЈ¬ФтCөгЗвСх»ҜДЖИЬТәөДМе»эОӘ0.031-0.024ЎБ3/4-0.008ЎБ3/4=0.00 7LЈ¬јҙ7mLЎЈ


 ФД¶БҝміөПөБРҙр°ё
ФД¶БҝміөПөБРҙр°ё
| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝИзНјОӘДіЦЦјЧҙјИјБПөзіШКҫТвНјЈ¬№ӨЧчКұөзЧУБчПтИзНјЛщКҫЎЈПВБРЕР¶ПХэИ·өДКЗ
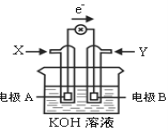
AЈ®XОӘСхЖш
BЈ®өзј«A·ҙУҰКҪЈәCH3OH-6e-+H2O = CO2+6H+
CЈ®Bөзј«ёҪҪьИЬТәpHФцҙу
DЈ®өзіШ№ӨЧчКұЈ¬ИЬТәЦРөзЧУУЙөзј«BБчПтөзј«A
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРҙлК©ҝП¶ЁДЬК№»ҜС§ЖҪәвТЖ¶ҜөДКЗ
A. Фцҙу·ҙУҰОпөДБҝ B. ФцјУС№Зҝ C. ЙэёЯОВ¶И D. К№УГҙЯ»ҜјБ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРёчЧйТәМе»мәПОпЈ¬ДЬУГ·ЦТәВ©¶··ЦАлөДКЗЈЁ Ј©
AЈ®ТТЛбәНЛ® BЈ®ТәдеәНұҪ CЈ®ұҪәНЛ® DЈ®ТТҙјәНЛ®
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ БҪ·ЭВБРјЈ¬өЪТ»·ЭУл№эБҝөДСОЛб·ҙУҰЈ¬өЪ¶ю·ЭУл№эБҝөДNaOHИЬТә·ҙУҰЈ¬ІъЙъЗвЖшөДМе»эұИОӘ1Јә2Ј¬ФтөЪТ»·ЭУлөЪ¶ю·ЭВБРјөДЦКБҝұИОӘ
A. 1Јә1 B. 1Јә2 C. 1Јә3 D. 1Јә4
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝДіИЬТәЦРҝЙДЬә¬УРH+ЎўNH4+ЎўMg2Ј«ЎўAl3+ЎўFe3Ј«ЎўCO32-ЎўSO42-ЎўNO3-ЦРөДјёЦЦЎЈ
ўЩ ИфјУИлРҝБЈЈ¬ЧоЦХІъЙъОЮЙ«ОЮО¶өДЖшМеЈ»
ўЪ ИфјУИлNaOHИЬТәЈ¬ІъЙъ°ЧЙ«іБөнЈ¬ЗТІъЙъөДіБөнБҝУлјУИлNaOHөДОпЦКөДБҝЦ®јдөД№ШПөИзНјЛщКҫЎЈФтПВБРЛө·ЁХэИ·өДКЗЈЁЈ©
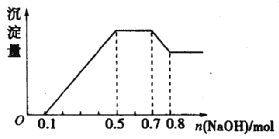
AЈ®ИЬТәЦРөДСфАлЧУЦ»УРHЈ«ЎўMg2Ј«ЎўAl3Ј«
BЈ®ИЬТәЦРn(NH4+)=0.2mol
CЈ®ИЬТәЦРТ»¶ЁІ»ә¬CO32-Ј¬ҝЙДЬә¬УРSO42-әНNO3-
DЈ®n(H+):n(Al3+):n(Mg2+)=1:1:1
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝДіОВ¶ИКұЈ¬ФЪИЭ»эОӘ3 LөДГЬұХИЭЖчЦРЈ¬XЎўYЎўZИэЦЦОпЦКөДОпЦКөДБҝЛжКұјдұд»ҜөДЗъПЯИзНјЛщКҫЈ¬УЙНјЦРКэҫЭ·ЦОцЈә
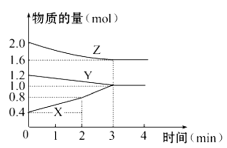
ЈЁ1Ј©ёГ·ҙУҰөД»ҜС§·ҪіМКҪОӘ____________ _______ЎЈ
ЈЁ2Ј©·ҙУҰҝӘКјЦБ2 minД©Ј¬XөД·ҙУҰЛЩВКОӘ_____ ____ЎЈ
ЈЁ3Ј©ёГ·ҙУҰКЗУЙ__________ЈЁМоРтәЕЈ©ҝӘКјөДЎЈ
ўЩХэ·ҙУҰ ўЪДж·ҙУҰ ўЫХэЎўДж·ҙУҰН¬Кұ
ЈЁ4Ј©ИфФцјУYөДУГБҝЈ¬»ҜС§·ҙУҰЛЩВКІ»ұд»ҜЈ¬ФтYОӘ__ ___М¬ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРОпЦККфУЪҙҝҫ»ОпөДКЗ
AЈ®ЖҜ°Ч·Ы BЈ®деЛ® CЈ®өвҫЖ DЈ®ТәВИ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРЛө·ЁХэИ·өДКЗ
AЈ®ПЛО¬ЛШЎўХбМЗЎўЖПМСМЗәНЦ¬·ҫФЪТ»¶ЁМхјюПВ¶јҝЙ·ўЙъЛ®Ҫв·ҙУҰ
BЈ®УНЦ¬¶јІ»ДЬК№деөДЛДВИ»ҜМјИЬТәНКЙ«
CЈ®КҜУН·ЦБуЎўГәөДёЙБуҫщОӘОпАнұд»Ҝ
DЈ®өн·ЫЎўө°°ЧЦКәНМмИ»ПрҪәҫщКЗМмИ»ёЯ·ЦЧУ»ҜәПОп
Ійҝҙҙр°ёәНҪвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com