
升高温度,下列数据不一定增大的是
A.化学反应速率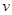 | B.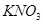 的溶解度S 的溶解度S |
| C.化学平衡常数K | D.水的离子积常数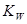 |
 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:单选题
在2 L的密闭容器中发生反应xA(g)+yB(g) zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是( )。
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是( )。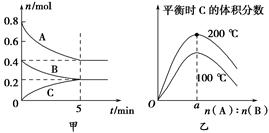
A.200 ℃时,反应从开始到平衡的平均速率v(B)=0.04 mol·L-1·min-1
B.200℃时,该反应的平衡常数为25 L2/mol2
C.当外界条件由200℃降温到100℃,原平衡一定被破坏,且正逆反应速率均增大
D.由图乙可知,反应xA(g)+yB(g) zC(g)的ΔH<0,且a=2
zC(g)的ΔH<0,且a=2
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
电镀废液中Cr2O72-可通过下列反应转化成铬黄(PbCrO4):
Cr2O72-(aq)+ 2Pb2+(aq)+ H2O(l)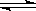 2PbCrO4(s)+ 2H+(aq)△H<0
2PbCrO4(s)+ 2H+(aq)△H<0
该反应达平衡后,改变条件,下列说法正确的是
| A.移走部分PbCrO4固体,Cr2O72-转化率升高 |
| B.升高温度,该反应的平衡常数(K)增大 |
| C.加入少量NaOH固体,自然沉降后,溶液颜色变浅 |
| D.加入少量K2Cr2O7固体后,溶液中c(H+)不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在一定温度下的恒容容器中,标志反应A(s)+2B(g) 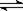 C(g)+D(g)已达平衡状态的是
C(g)+D(g)已达平衡状态的是
| A.混合气体的压强不随时间变化而变化 |
| B.混合气体的密度不随时间变化而变化 |
| C.气体总物质的量不随时间变化而变化 |
| D.单位时间内生成n mol C,同时消耗2n mol B |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在A2+3B2 = 2C的反应中,经过t秒钟后,C的浓度增加了0.6mol/L,在此期间,反应速率V(B2)=0.45mol/(L·S),则t值为
| A.1秒 | B.1.5秒 | C.2秒 | D.2.5秒 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
工业上可利用甲烷除去NO气体,反应为CH4(g)+4NO(g)  CO2(g)+2N2(g)+2H2O(g) ΔH<0。在恒容的密闭容器中,下列有关说法正确的是( )
CO2(g)+2N2(g)+2H2O(g) ΔH<0。在恒容的密闭容器中,下列有关说法正确的是( )
| A.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
| B.单位时间内消耗CH4和N2的物质的量比为1∶2时,反应达到平衡 |
| C.平衡时,其他条件不变,增加CH4的浓度,氮氧化物的转化率减小 |
| D.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知2SO2(g)+O2(g)  2SO3(g),起始时SO2和O2分别为20mol和10mol,达到平衡时SO2的转化率为80%。若从SO3开始进行反应,在相同的条件下,欲使平衡时各成分的体积分数与前者相同,则起始时SO3的物质的量及SO3的转化率分别为
2SO3(g),起始时SO2和O2分别为20mol和10mol,达到平衡时SO2的转化率为80%。若从SO3开始进行反应,在相同的条件下,欲使平衡时各成分的体积分数与前者相同,则起始时SO3的物质的量及SO3的转化率分别为
| A.10mol 10% | B.20mol 20% | C.20mol 40% | D.30mol 80% |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
可逆反应N2(g)+ 3H2(g) 
 2NH3 (g)达到平衡状态,下列说法中正确的是( )
2NH3 (g)达到平衡状态,下列说法中正确的是( )
| A.该反应停止,N2和H2不再化合 | B.N2、H2、NH3浓度不变 |
| C.N2、H2、NH3浓度相等 | D.N2、H2、NH3的物质的量之比为1:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列事实不能用勒夏特列原理解释的是
①氯化铁溶液加热蒸干最终得不到氯化铁固体 ②铁在潮湿的空气中容易生锈
③实验室可用排饱和食盐水的方法收集氯气
④常温下,将1 mL pH=3的醋酸加水稀释至100 mL,测得其pH<5
⑤钠与氯化钾共融制备钾:Na(l)+KCl(l)  K(g)+NaCl(l)
K(g)+NaCl(l)
⑥二氧化氮与四氧化二氮的平衡体系,加压后颜色加深
| A.②⑥ | B.①②③ | C.②⑤⑥ | D.①③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com