
【题目】下列事实不能用沉淀溶解平衡原理解释的是![]()
A.误食可溶性钡盐,用![]() 的硫酸钠溶液洗胃
的硫酸钠溶液洗胃
B.除去硫酸铜溶液中的铁离子,可加![]() ,调节pH
,调节pH
C.在AgI的沉淀体系中加硫化钠溶液,出现黑色沉淀
D.在配制![]() 溶液时,用稀盐酸溶解
溶液时,用稀盐酸溶解
【答案】A
【解析】
能用沉淀溶解平衡原理解释,说明存在难溶电解质的溶解平衡,且改变外界条件,平衡发生移动,以此解答该题。
A.硫酸根离子与钡离子反应为复分解反应,不属于沉淀的转化,故A不能用沉淀溶解平衡原理解释;
B.氢氧化铁的溶解度较小,加入氢氧化铜,可调节pH,利于生成氢氧化铁,存在沉淀的转化,故B能用沉淀溶解平衡原理解释;
C.在AgI的沉淀体系中加硫化钠溶液,出现黑色沉淀,说明生成溶解度更小的硫化银,存在沉淀的转化,故C能用沉淀溶解平衡原理解释;
D.在配制![]() 溶液时,用稀盐酸溶解,可抑制氢氧化铁的生成,防止溶液浑浊,与难溶电解质的溶解平衡有关,故D能用沉淀溶解平衡原理解释。
溶液时,用稀盐酸溶解,可抑制氢氧化铁的生成,防止溶液浑浊,与难溶电解质的溶解平衡有关,故D能用沉淀溶解平衡原理解释。
答案选A。


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】某课外活动小组的同学欲探究镁与浓硫酸的反应,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫外,还可能产生氢气。为验证甲、乙两同学的判断是否正确,丙同学设计的实验装置如图所示(镁粉与浓硫酸共热时产生的气体为X,且该气体发生装置已略去)。

(1)仪器E的名称是_____________。
(2)镁粉与浓硫酸共热时生成二氧化硫的化学方程式为_____________。
(3)乙同学认为还可能产生氢气的理由是_____________。
(4)B 中加入的试剂是_______,其作用是_____________。
(5)装置A中发生反应的离子方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容条件下发生反应A(g)+3B(g)2 C(g)(△H<0),改变其他反应条件,在Ⅰ、Ⅱ阶段体系中各物质浓度随时间变化的曲线如下图所示,下列说法中正确的是
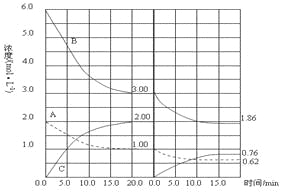
A.第Ⅰ阶段用C表示的平衡前的反应速率υ (C)=0.1 mol/(L·s)
B.第Ⅱ阶段中B的平衡转化率αⅡ(B)为0.019
C.第Ⅰ阶段的平衡常数KⅠ与第Ⅱ阶段平衡常数KⅡ的大小关系是:KⅠ﹤KⅡ
D.由第一次平衡到第二次平衡,可能采取的措施是从反应体系中移出产物C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中,一定条件下进行反应:NO(g)+CO(g)=1/2N2(g)+CO2(g) ΔH=-373.2 kJ/mol。如图曲线a表示该反应过程中,NO的转化率与反应时间的关系,若改变起始条件,使反应过程按照曲线b进行,可采取的措施是( )

A. 加催化剂 B. 向密闭容器中加入氩气
C. 降低温度 D. 增大反应物中NO的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值。下列说法正确的是( )
A.将0.2 molFeCl3 水解制成胶体,所得胶体粒子数为0.2 NA
B.25℃时,1LpH=13的Ba(OH)2溶液中含有OH-离子数为0.2 NA
C.0.1mol·L1 NH4Cl溶液中 NH![]() 数小于0.1 NA
数小于0.1 NA
D.1L 2mol·L1K2S溶液中H2S、S2-和HS-的总数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜是一种重要的化工原料,一种利用低品位铜矿![]() 主要含有Cu2S、CuS、FeO、Fe2O3、SiO2等
主要含有Cu2S、CuS、FeO、Fe2O3、SiO2等![]() 为原料制取CuCl的工艺流程如下:
为原料制取CuCl的工艺流程如下:

(1)反应Ⅰ“浸取”前需将铜矿粉碎的目的是___________________________;
(2)滤渣Ⅰ的成分除S和![]() 外还含有___________,反应 Ⅰ中
外还含有___________,反应 Ⅰ中![]() 的作用为_______________
的作用为_______________
(3)已知生成氢氧化物的pH如下表,则反应Ⅱ“中和”时,用氨水调pH的范围是______________。
物质 |
|
|
|
开始沉淀pH |
|
|
|
完全沉淀pH |
|
|
|
(4)检验滤液Ⅱ中是否含有![]() 所需要的试剂是:______________
所需要的试剂是:______________
(5)①反应Ⅲ中生成难溶![]() 的离子方程式:______________
的离子方程式:______________
②反应Ⅳ所对应的化学方程式:______________________________
(6) CuCl的定量分析
步骤1.取样品0.7500g和30.0mL 1.0mol·L-1过量的FeCl3溶液置于250mL的锥形瓶中,不断摇动。
步骤2.待样品溶解后,平均分为3份,用0.1000mol·L-1 Ce(SO4)2标准溶液进行滴定。
三次实验测得数据如下表
序号 | 1 | 2 | 3 |
起始读数 |
|
|
|
终点读数 |
|
|
|
已知:![]() ;
;![]() 。
。
①数据处理:计算得CuCl的纯度为_________![]()
②误差下列操作会使测定结果偏高的是______________
A.锥形瓶中有少量蒸馏水
B.滴定终点读数时仰视滴定管刻度线
C.0.1000mol·L-1硫酸铈溶液久置后浓度变小
D.滴定前滴定管尖嘴无气泡,滴定后产生气泡
E.用量筒取10.0mL 1.0mol·L-1的![]() 溶液时仰视刻度线
溶液时仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体缺乏维生素A,会出现皮肤干燥、夜盲症等症状。维生素A又称视黄醇,分子结构如图所示,下列说法正确的是( )
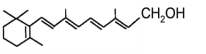
A.维生素A是一种易溶于水的醇
B.维生素A能被氧化得到酮
C.1mol维生素A最多能与5molH2发生加成反应
D.维生素A的分子式为C20H32O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用电解饱和食盐水来制取烧碱,所用的食盐水需两次精制。第一次精制主要是用沉淀法除去粗盐水中Ca2+、Mg2+、Fe3+、SO42-等离子,过程如下:
Ⅰ.向粗盐水中加入过量BaCl2溶液,过滤;
Ⅱ.向所得滤液中加入过量Na2CO3溶液,过滤;
Ⅲ.用盐酸调节滤液的pH,获得一次精制盐水。
(1)过程Ⅰ中除去的离子是______。
(2)表是过程Ⅰ、Ⅱ中生成的部分沉淀及其在20℃时的溶解度(g/100 gH2O):
CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 | Fe(OH)3 |
2.6×10-2 | 2.5×10-4 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 | 4.8×10-9 |
运用表中信息回答下列问题:
①过程Ⅱ中生成的主要沉淀除CaCO3和Mg2(OH)2CO3外还有______。
②过程Ⅰ选用的是BaCl2而不选用CaCl2,原因是______。
③除去Mg2+的离子方程式是______。
④检测Ca2+、Mg2+、Ba2+是否除尽时,只需检测Ba2+即可,原因是______。
(3)第二次精制要除去微量的I-、IO3-、NH4+、Ca2+、Mg2+,流程示意图如图:
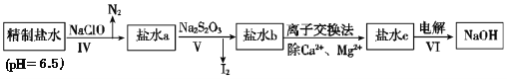
①过程Ⅳ除去的离子是______。
②盐水b中含有SO42-,Na2S2O3将IO3-还原为I2的离子方程式是______。
③在过程Ⅴ中所用的Na2S2O3俗称海波,是一种重要的化工原料。商品海波主要成分是Na2S2O3·5H2O为了测定其含Na2S2O3·5H2O的纯度,称取8.00 g样品,配制成250.0 mL溶液,取25.00 mL于锥形瓶中,滴加淀粉溶液作指示剂,再用浓度为0.0500 mol/L的碘水滴定(发生反应2S2O32-+I2=S4O62-+2I-),滴定达到终点时的现象是______。下表记录滴定结果:
滴定次数 | 滴定前读数(mL) | 滴定滴定后读数(mL) |
第一次 | 0.30 | 31.12 |
第二次 | 0.36 | 31.56 |
第三次 | 1.10 | 31.88 |
计算样品的纯度为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用0.1000 mol·L-1的HCl标准溶液滴定20.00mL未知浓度的NaOH溶液,下列说法正确的是

A.可以用如图所示的装置及操作进行滴定
B.指示剂可以使用紫色石蕊
C.滴加盐酸的速度应保持匀速,且需不断摇荡锥形瓶
D.若滴加盐酸的滴定管滴定前有气泡,滴定终了无气泡,则所测NaOH溶液浓度偏大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com