

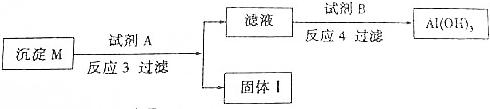
分析 在制四氢铝锂的流程中,在高温高压的条件下,氩气作保护气,Na、Al作还原剂,H2作氧化剂,发生氧化还原反应生成四氢铝锂(LiAlH4),四氢铝钠在乙醚溶剂中与氯化锂发生复分解反应生成四氢铝锂.
(1)LiH易与空气中的氧气发生反应;(2)Na、Al作还原剂,H2作氧化剂,发生氧化还原反应;(3)氧化还原反应中,氧化剂中元素化合价降低;
(4)分离(3)中反应生成的LiOH与Al(OH)3,根据Al(OH)3具有两性将它们分离.
解答 解:(1)LiH易与空气中的氧气发生反应,反应1中,在通入氢气之前先通入Ar气的目的是防止LiH与O2反应着火燃烧,Ar气作保护气,
故答案为:作保护气;(2)反应1的化学反应方程式:Na+Al+2H2=NaAlH4,故答案为:Na+Al+2H2=NaAlH4;(3)LiAlH4+4H2O═LiOH+Al(OH)3+4H2↑,该反应的氧化剂为水,故答案为:水;
(4)Al(OH)3具有两性,它与NaOH反应的离子方程式:Al(OH)3+OH-=[Al(OH)4]-,在滤液中通过量的CO2可得Al(OH)3,
故答案为:Al(OH)3+OH-=[Al(OH)4]-;CO2.
点评 本题考查知识点较多,涉及物质的分离、氧化还原反应、离子方程式的书写、元素化合物的性质等,属于拼合型题目,需要学生具备扎实的基础,难度中等.


科目:高中化学 来源:2017届广东省山一高三上第二次统测化学试卷(解析版) 题型:选择题
下列反应中,相关示意图错误的是( )
A | B | C | D |
将二氧化硫通入到一定量氯水中 | 将NaHCO3溶液滴入到一定量Ba(OH)2溶液中 | 将铜粉加入到一定量浓硝酸中 | 将铁粉加入到一定量氯化铁溶液中 |
|
|
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
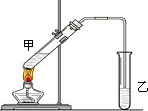 俗话说,“陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程.请回答下列问题:
俗话说,“陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程.请回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
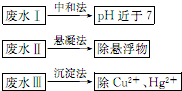 水处理技术在生产、生活中应用广泛,对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施.
水处理技术在生产、生活中应用广泛,对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
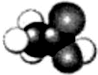 乙酸是食醋的主要成分,它的分子结构模型如图所示.
乙酸是食醋的主要成分,它的分子结构模型如图所示.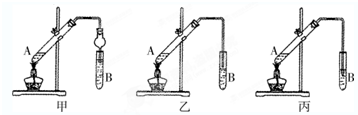
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com