
【题目】请根据官能团的不同对下列有机物进行分类(填序号)。

(1)芳香烃:_____________ ;(2)卤代烃:_____________;(3)醇:_______________ ;
(4)酚:_____________;(5)醛:_______________ ;(6)酮:_____________;
(7)羧酸:_____________ ;(8)酯:_____________。
科目:高中化学 来源: 题型:
【题目】在2L密闭容器内,800℃时反应:2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
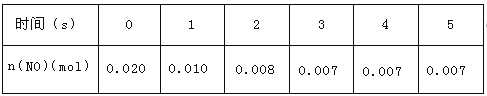
(1)下图表示NO2的变化曲线是_____。用O2表示从0-2s内该反应的平均速率v=____。
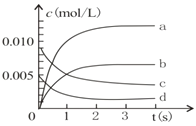
(2)能说明该反应己达到平衡状态的是_____(填字母序号,下同)。
a.v(NO2)=2v(O2)
b.容器内气体总物质的量保持不变
c.V逆(NO)=2v正(O2 )
d.容器内气体的密度保持不变
(3)为使该反应的反应速率增大,下列措施正确的是_____。
A.及时分离出NO2气体 B.适当升高温度
C.增大O2的浓度 D.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,NOx和SO2是雾霾的主要成分。
(一)NOx主要来源于汽车尾气。
已知:N2(g)+O2(g)![]() 2NO(g)△H=+180.50kJmol-1
2NO(g)△H=+180.50kJmol-1
2CO(g)+O2(g)![]() CO2(g)△H=-566.00kJmol-1
CO2(g)△H=-566.00kJmol-1
(1)为了减轻大气污染,人们提出在汽车尾气排气管口采用催化剂将NO和CO转化成无污染气体参 与大气循环.写出该反应的热化学方程式___________________________;
(2)T℃时,将等物质的量的NO和CO充人容积为2L的密闭容器中,保持温度和体积不变,反应过程(0-15min)中NO的物质的量随时间变化如下图所示.
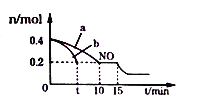
①T℃时该化学反应的平衡常数K=____________;平衡时若保持温度不变,再向容器中充入CO、N2各0.8mol,平衡将__________移动;(填“向左”、“向右”或“不”)
②图1中a、b分别表示在一定温度下,使用质量相同但表面积不同的催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是_______(填“a”或“b”)
③15min时,若改变外界反应条件,导致n(NO)发生如图所示的变化,则改变的条件可能是____________;
(二)SO2主要来源于煤的燃烧.燃煤烟气的脱硫减排是减少大气中含硫化合物污染的关健。
(3)用纯碱溶液吸收SO2可将其转化为HSO3-,该反应的离子方程式是________________;
(4)如图所示的电解装罝可将雾霾中的NO、SO2分别转化为NH4+和SO42-。
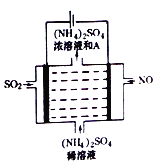
①写出物质A的化学式_________,阳极的电极反应式是________________;
②该电解反应的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T ℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示。

根据以上条件,回答下列问题:
(1)A与B反应生成C的化学方程式为 ,正反应为________(填“吸热”或“放热”)反应。
(2)在密闭容器中,加入2 mol A和6 mol B。
① 当反应达到平衡时, A和B的浓度比是_______;A和B的转化率之比是_______。
② 升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量________。(填“变大”、“变小”或“不变”)
③ 当达到平衡时,充入氩气,并保持压强不变,平衡将____(填“正向”、“逆向”或“不”)移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水是一种重要的自然资源,是人类赖以生存不可缺少的物质。请回答下列问题:
(1)水质优劣直接影响人体健康。天然水在净化处理过程中加入的混凝剂可以是_______________(填两种物质的名称),其净水作用的原理是_______________________。
(2)水的净化与软化的区别是______________________________________。
(3)硬度为1°的水是指每升水含10 mg CaO或与之相当的物质(如7.1 mg MgO)。若某天然水中c(Ca2+)=1.2×10-3mol·L-1,c(Mg2+)=6×10-4mol·L-1,则此水的硬度为________。
(4)若(3)中的天然水还含有c(HCO3-)=8×10-4mol·L-1,现要软化10 m3这种天然水,则需先加入Ca(OH)2_______g,后加入Na2CO3_______g。
(5)如图是电渗析法淡化海水的原理图,其中电极A接直流电源的正极,电极B接直流电源的负极。
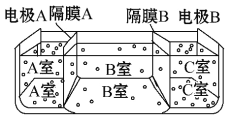
①隔膜A是________(填“阴”或“阳”)离子交换膜;
②某种海水样品,经分析含有大量的Na+、Cl-以及少量的K+、SO42-。若用上述装置对该海水进行淡化,当淡化工作完成后,A、B、C三室中所得溶液(或液体)的pH分别为pHa、pHb、pHc,则其大小顺序为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下图装置进行实验,并回答下列问题

(1)判断装置的名称:A池为 B池为 。
(2)铜极为______极,电极反应式为 。
(3)B装置中,C1与C2均为石墨棒,石墨棒C1为___极,电极反应式为 ,石墨棒C2附近发生的实验现象为 。
(4)当C2极析出224mL(标准状态)气体时,锌的质量减少 g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年10月5日,从瑞典斯德哥尔摩传来令人振奋的消息:中国女科学家屠呦呦获得2015年诺贝尔生理学或医学奖。理由是她发现了青蒿素,这种药品可以有效降低疟疾患者的死亡率。青蒿素的一种化学合成部分工艺流程如下:

已知:羰基![]() H可发生反应应
H可发生反应应![]()
回答下列问题:
(1)青蒿素的含氧官能团名称: 和过氧基;
(2)写出A发生加聚反应的化学方程式 ;
(3)反应B→C,实际上可看作两步进行,依次发生的反应类型是 ;
(4)写出由苯甲醛和氯乙烷为原料,制备苄基乙醛(![]() CH2CH2CHO)的合成路线流程图;无机试剂任用,合成路线流程图示例如下:CH3CH2OH
CH2CH2CHO)的合成路线流程图;无机试剂任用,合成路线流程图示例如下:CH3CH2OH![]() H2C=CH2
H2C=CH2![]() H2C Br-CH2 Br
H2C Br-CH2 Br
。
(5)写出E发生水解反应的化学方程式 。
(6)写出HC(OCH3)3只属于醇的同分异构体的结构简式(同一个碳原子上不能同时连接两个羟基) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强。25℃时氯气-氯水体系中存在以下平衡关系:
Cl2(g) ![]() Cl2(aq) K1=10-1.2
Cl2(aq) K1=10-1.2
Cl2(aq)+ H2O ![]() HClO + H+ +Cl- K2=10-3.4
HClO + H+ +Cl- K2=10-3.4
HClO ![]() H+ + ClO- Ka=?
H+ + ClO- Ka=?
其中,Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。下列表述正确的是

A.氯处理饮用水时,在夏季的杀菌效果比在冬季好
B.用氯处理饮用水时,pH=7.5时杀菌效果比pH=6.5时好
C.在氯处理水体系中,c(HClO) +c(ClO-) =c(H+)-c(OH-)
D.Cl2(g)+ H2O ![]() 2H+ + ClO- + Cl- ,K=10-12.1
2H+ + ClO- + Cl- ,K=10-12.1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常见金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,
它们之间存在如下转化关系(图中有些反应的产物和反应的条件没有全部标出)。其中B是地壳中含量居第一的金属元素,C是当今产量和用量最多的金属。请回答下列问题:
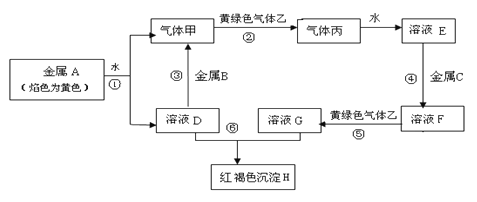
(1)写出金属B和气体丙的化学式 、 。
(2)写出反应①的化学反应方程式 。
(3)沉淀H的化学式为 。
(4)往溶液G中滴入KSCN溶液,现象是——————————————————
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com