
| 实验步骤 | 设计这一步骤的目的 |
| 1.将配制的氢氧化钠溶液加热 | |
| 2.在加热后的溶液中滴入酚酞,并在上方滴一些植物油 | |
| 实验方法 | 可能观察到的现象和结论 |
| 方案一:分别配制不同物质的量浓度的氢氧化钠溶液,然后各滴加数滴酚酞溶液。 | 物质的量浓度大的溶液中酚酞红色消失 证明 |
| 方案二:向原红色消失的溶液中加 (填试剂名称) | 红色重新出现,则说明红色消失与氢氧化钠物质的量浓度大小有关 |


科目:高中化学 来源:不详 题型:实验题
| 方法 | 需测定的数据 |
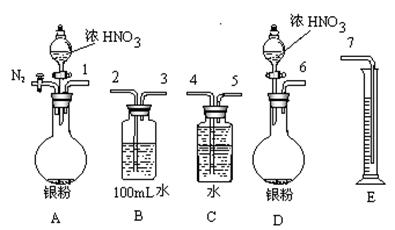
| ① | 测定产生的H2的体积 |
| ② | |
| 实验操作 | 预期现象和结论 |
| 步骤1: | |
| 步骤2: | |
| …… | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| | 滴定前读读数/mL | 滴定后读数/mL |
| 第一次 | | |
| 第二次 | 0.10 | 18.00 |
| 第三次 | 0.20 | 18.30 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
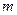 。
。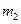 。
。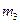 。
。| A.纯碱溶液 | B.烧碱溶液 | C.明矾溶液 | D.稀硫酸 |
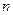 H2O),对FeSO4的制备 (填“有”、“无”)影响,理由是(用离子方程式回答) 。
H2O),对FeSO4的制备 (填“有”、“无”)影响,理由是(用离子方程式回答) 。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验操作 | 预期现象与结论 |
| 步骤1: | |
| 步骤2: | |
| 步骤3: | |
| … | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
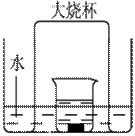
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.64 g SO2含有氧原子数为1NA |
| B.物质的量浓度为0.5 mol·L-1的MgCl2溶液,含有Cl-数为1NA |
| C.标准状况下,22.4 L H2O的分子数为1NA |
| D.常温常压下,14 g N2含有分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 实验内容 | 实验现象 | 实验结论 |
(1)Na、Mg(条)、K与水反应 | 同一周期自左而右元素原子失电子的能力逐渐______;同一主族自上而下元素原子失电子能力依次______. | |
(2)Mg、Al与酸反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com