
【题目】草酸晶体的组成可表示为H2C2O4·xH2O,为测定x值,进行下述实验:①称取Wg草酸晶体配成100.0mL水溶液 ②取25.0mL所配草酸溶液置于锥形瓶中,加入适量稀H2SO4后,用浓度为amol/L KMnO4溶液滴定。滴定时,所发生的反应为:
2KMnO4 +5H2C2O4 +3H2SO4=K2SO4 +10CO2+2MnSO4 +8H2O 回答下列问题:
(1)实验①中,为配制准确物质的量浓度的草酸溶液,所需用到的仪器是天平(含砝码)、烧杯、药匙、胶头滴管和 _______、 __________ 。
(2)实验②中,滴定时,KMnO4溶液应装在_______式滴定管中(填“酸”或“碱”)
(3)若滴定用的KMnO4溶液因久置而部分变质,浓度偏低,则实验结果所测定的x值将_____(填“偏高”,“偏低”,“无影响”)。
(4)在滴定过程中起指示剂作用的是______,当KMnO4溶液与草酸反应后,怎样判断滴定终点____________________________________________________________________________.
(5)若达到滴定终点时,共用去amol/LKMnO4溶液VmL,则实验测得所配草酸溶液的物质的量浓度为_______;由此计算出草酸晶体中的x值是__________。(结果用a,v, W表示)
【答案】 玻璃棒 100mL容量瓶 酸式滴定管 偏低 KMnO4 溶液由无色变成淡紫色且半分钟之后不褪色 ![]() mol/L
mol/L 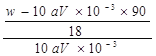 或者
或者![]()
【解析】(1)配制准确物质的量浓度的草酸溶液,所需用到的仪器是天平(含砝码)、烧杯、药匙、胶头滴管和玻璃棒、 100mL容量瓶。
(2) KMnO4溶液是强氧化剂,应装在酸式滴定管中。碱式滴定管上有橡胶管,易被氧化剂氧化。
(3)若滴定用的KMnO4溶液因久置而部分变质,浓度偏低,则滴定时消耗标准高锰酸钾溶液的体积将偏大,相当于样品中草酸的含量偏高,所以实验结果所测定的x值将偏低。
(4)因为反应物中KMnO4溶液是紫红色的,反应后生成的硫酸锰溶液接近无色,所以不用另加催化剂,在滴定过程中起指示剂作用的是KMnO4,溶液由无色变成淡紫色且半分钟之后不褪色时即达滴定终点.
(5)若达到滴定终点时,共用去amol/LKMnO4溶液VmL,则由两者反应的化学方程式可得,25mL草酸溶液中n(H2C2O4)= ![]() ,则实验测得所配草酸溶液的物质的量浓度为
,则实验测得所配草酸溶液的物质的量浓度为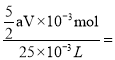
![]() mol/L.由此计算出Wg草酸晶体中n(H2C2O4)=
mol/L.由此计算出Wg草酸晶体中n(H2C2O4)= ![]() ,所以m(H2C2O4)=
,所以m(H2C2O4)= ![]() g/mol=0.9aV g,由草酸晶体的化学式得x:1=n(H2O): n(H2C2O4)=
g/mol=0.9aV g,由草酸晶体的化学式得x:1=n(H2O): n(H2C2O4)= ![]() :
:![]() ,化简得x=
,化简得x=![]() 。
。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】已知:pKa=lgKa,25℃时,H2SO3的pKa1=1.85,pKa2=7.19。常温下,用0.1mol·L1NaOH溶液滴定20mL0.1mol·L1 H2SO3溶液的滴定曲线如下图所示(曲线上的数字为pH)。下列说法不正确的是( )

A. a点所得溶液中:2c(H2SO3)+c(SO32-)=0.1mol·L1
B. b点所得溶液中:c(H2SO3)+c(H+)=c(SO32-)+c(OH-)
C. c点所得溶液中:c(Na+)>3c(HSO3-)
D. d点所得溶液中:c(Na+)>c(SO32-)> c(HSO3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】慢心律是一种治疗心律失常的药物,它的合成路线如下:

(1)由B→C的反应类型为 。
(2)C分子中有2个含氧官能团,分别为 和 (填官能团名称)。
(3)写出A与浓溴水反应的化学方程式 。
(4)由A制备B的过程中有少量副产物E,它与B互为同分异构体,E的结构简式为 。
(5)写出同时满足下列条件的D的一种同分异构体的结构简式 。
①属于α-氨基酸;
②是苯的衍生物,且苯环上的一氯代物只有两种;
③分子中含有两个手性碳原子。
(6)已知乙烯在催化剂作用下与氧气反应可以生成环氧乙烷(![]() )。写出以邻甲基苯酚(
)。写出以邻甲基苯酚(  )和乙醇为原料制备
)和乙醇为原料制备  的合成路线流程图(无机试剂任用)。
的合成路线流程图(无机试剂任用)。
合成路线流程图示例如下:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁分别是乙烷、乙烯、乙炔、苯中的一种;
①甲、乙能使溴的四氯化碳溶液褪色。乙与等物质的量的H2反应生成甲,甲与等物质的量的H2反应生成丙。
②丙既不能使溴的四氯化碳溶液褪色,也不能使KMnO4酸性溶液褪色。
③丁能使溴水褪色的原因与甲能使溴水褪色的原因不同,丁也不能使KMnO4酸性溶液褪色,但丁在一定条件下可与溴发生取代反应。相同条件下,丁蒸气的密度是乙密度的3倍。
据以上叙述完成下列问题:
(1)写出甲的结构简式__________、乙的结构式____________、丙分子中含有的化学键类型是__________;
(2)写出丁与液溴在催化剂作用下发生取代反应的方程式_________________;
(3)写出甲使溴的四氯化碳溶液褪色的化学方程式_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知硝酸银与氯化钾反应生成硝酸钾和不溶于水的氯化银,化学方程式为AgNO3+KCl=AgCl↓+KNO3。将含有少量氯化钾的硝酸钾固体提纯,某学生如图所示的实验操作。回答下列问题:

(1)将样品置于烧杯中,加入适量的水溶解,同时用玻璃棒搅拌,搅拌的作用是___________。
(2)向溶液中加入适量的________溶液,使氯化钾转化为沉淀。
(3)将混合液进行过滤,过滤装置和操作如图所示,指出图中的两处错误:①__________________;②______________________。
(4)为了从液体中得到硝酸钾晶体,可选用的两种结晶方法是:① __________________________ ;②______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制硫酸中,SO2的催化氧化是一个可逆反应:2SO2+O2 ![]() 2SO3 ,设该反应在一定条件下,10min达到一定限度,在反应物和生成物之间建立一种动态平衡(即化学平衡),填空:
2SO3 ,设该反应在一定条件下,10min达到一定限度,在反应物和生成物之间建立一种动态平衡(即化学平衡),填空:
SO2 | O2 | SO3 | |
反应开始时的浓度(mol·L-1) | 3.0 | 1.5 | 0 |
10min后的浓度(mol·L-1) | |||
平均反应速率 (mol·L-1·min-1) | 0.1 |
___________、______________、________________、____________、_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于碘水的下列说法中正确的是
A. 碘水中的分子只有水分子和碘分子B. 碘水呈紫黑色
C. 碘水能与氢氧化钠溶液反应D. 碘水不能与硝酸银溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上测量SO2、N2、O2混合气体中SO2含量的装置如右图。反应管中装有碘的淀粉溶液。SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2 +2H2O==H2SO4+2HI

(1)混合气体进入反应管后,量气管内增加的水的体积等于__________的体积(填分子式)。
(2)反应管内的溶液蓝色消失后,没有及时停止通气,则测得的SO2含量_____(填“偏高”、“偏低”或“不受影响”)。
(3)反应管内的碘的淀粉溶液也可以用_______________代替(填写物质名称)。
(4)若碘溶液体积为V![]() mL,浓度为cmol·L
mL,浓度为cmol·L![]() 。N2与O2的体积为V
。N2与O2的体积为V![]() mL(已折算为标准状况下的体积)。用c、V
mL(已折算为标准状况下的体积)。用c、V![]() 、V
、V![]() 表示SO2的体积百分含量为:_________________。
表示SO2的体积百分含量为:_________________。
(5)将上述装置改为简易实验装置,除导管外,还需选的仪器为________(选下列仪器编号)。
a.烧杯 b.试管 c.广口瓶 d.容量瓶 e.量筒 f.单孔塞 g.双孔塞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)根据下列图文回答问题:

![]()


越王勾践的青铜剑 高钙豆奶粉 ![]() 的分子结构 干冰
的分子结构 干冰
①青铜剑属于__________(填“纯金属”或“合金”)。
②高钙豆奶粉的“钙”指的是__________(填“元素”、“原子”、或“分子”)。
③![]() 是由__________构成的。④干冰可用于______________(填一例)。
是由__________构成的。④干冰可用于______________(填一例)。
(2)根据下图中自制汽水的配料回答问题。

①柠檬酸的pH____7(填“<”、“=”或“>”),能使紫色石蕊溶液变为__________色。
②配料中富含维生素的是________,小苏打的化学式是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com