
【题目】![]() 环己酮是一种重要的有机化工原料。实验室合成环己酮的反应如下:
环己酮是一种重要的有机化工原料。实验室合成环己酮的反应如下:

环己醇和环己酮的部分物理性质见下表:
物质 | 相对分子质量 | 沸点(℃) | 密度(g·cm-3,20℃) | 溶解性 |
环己醇 | 100 | 161.1 | 0.9624 | 能溶于水和醚 |
环己酮 | 98 | 155.6 | 0.9478 | 微溶于水,能溶于醚 |
现以20 mL环己醇与足量Na2Cr2O7和硫酸的混合液充分反应,制得主要含环己酮和水的粗产品,然后进行分离提纯。分离提纯过程中涉及的主要步骤(未排序):
a.蒸馏,除去乙醚后,收集151~156℃馏分;
b.水层用乙醚(乙醚沸点34.6 ℃,易燃烧)萃取,萃取液并入有机层;
c.过滤;
d.往液体中加入NaCl固体至饱和,静置,分液;
e.加入无水MgSO4固体,除去有机物中少量水。
回答下列问题:
(1)上述分离提纯步骤的正确顺序是__________ (填字母)。
(2)b中水层用乙醚萃取的目的是_______。
(3)以下关于萃取分液操作的叙述中,不正确的是__________。
A.水溶液中加入乙醚,转移至分液漏斗中,塞上玻璃塞,如图用力振荡
B.振荡几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振荡并放气后,手持分液漏斗静置待液体分层
D.分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗口上的小孔,再打开旋塞待下层液体全部流尽时,再从上口倒出上层液体
(4)在上述操作d中,加入NaCl固体的作用是__________。蒸馏除乙醚的操作中采用的加热方式为________。
(5)蒸馏操作时,一段时间后发现未通冷凝水,应采取的正确方法是______。
【答案】d b e c a 使水层中少量的有机物进一步被提取,提高产品的产量 ABC 降低环己酮的溶解度,增加水层的密度,有利于分层 水浴加热 停止加热,冷却后通自来水
【解析】
(1)环己酮的提纯时应首先加入NaCl固体,使水溶液的密度增大,将水与有机物更容易分离开来,然后向有机层中加入无水MgSO4,出去有机物中少量的水,然后过滤,除去硫酸镁晶体,再进行蒸馏即可;
(2)环己酮在乙醚中的溶解度大于在水中的溶解度,且乙醚和水不互溶,则乙醚能作萃取剂,从而提高产品产量;
(3)根据萃取、分液的实验步骤和操作注意事项分析;
(4)NaCl能增加水层的密度,降低环己酮的溶解,有利于分层;乙醚的沸点较低,所以蒸馏时温度不宜太高;
(5)为防止冷凝管炸裂,应该停止加热。
(1)环己酮的提纯时应首先加入NaCl固体,使水溶液的密度增大,水与有机物更容易分离开,然后向有机层中加入无水MgSO4,除去有机物中少量的水,然后过滤,除去硫酸镁晶体,再进行蒸馏即可,故答案为:d b e c a;
(2)环己酮在乙醚中的溶解度大于在水中的溶解度,且乙醚和水不互溶,则乙醚能作萃取剂,能将水中的环己酮萃取到乙醚中,从而提高产品产量,故答案为:使水层中少量的有机物进一步被提取,提高产品的产量;
(3)A、水溶液中加入乙醚,转移至分液漏斗,塞上玻璃塞,应该倒转过来然后用力振荡,只有如此才能充分混合,故A错误;
B、放气的方法为:漏斗倒置,打开旋塞放气,而不是打开玻璃塞,故B错误;
C、经几次振摇并放气后,分液漏斗放置在铁架台上静置待液体分层,而不是手持分漏斗静置液体分层,不符合操作规范性,故C错误;
D、分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗上的小孔,利用压强差使液体流出,再打开旋塞待下层液体全部流尽时,为防止产生杂质,再从上口倒出上层液体,故D正确;
ABC正确,故答案为:ABC;
(4)NaCl能增加水层的密度,降低环己酮的溶解,且有利于分层;乙醚的沸点较低,所以蒸馏时温度不宜太高,所以应该采用水浴加热,故答案为:降低环己酮的溶解度,增加水层的密度,有利于分层;水浴加热;
(5)如果直接将冷水连接冷凝管,馏分温度如果急剧冷却会导致冷凝管炸裂,为防止冷凝管炸裂,应该停止加热,冷却后通自来水,故答案为:停止加热,冷却后通自来水。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】如图所示,某同学设计一个燃料电池并探究氯碱工业原理和粗铜的精炼原理, 其中乙装置中 X 为阳离子交换膜。

根据要求回答相关问题:
(1)写出负极的电极反应式_____
(2)写出石墨电极的电极反应式_____________
(3)反应一段时间后,乙装置中生成氢氧化钠主要在_________(填“铁极”或“石墨极”)区。
(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为_________,反应一段时间,硫酸铜溶液浓度将_____(填“增大”“减小”或“不变”)。
(5)若在标准状况下,有 2.24 L 氧气参加反应,则乙装置中铁电极上生成的气体的分子数目为_____;丙装置中阴极析出铜的质量为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以H2、O2、熔融盐Na2CO3组成燃料电池,采用电解法制备 Fe(OH)2,装置如右图所示,其中电解池两极材料分别为铁和石墨,通电一段时间后,右侧玻璃管中产生大量的白色沉淀。则下列说法正确的是
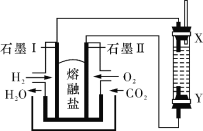
A. 石墨电极Ⅱ处的电极反应式为O2+4e-=2O2-
B. X是铁电极
C. 电解池中有1mol Fe溶解,石墨Ⅰ耗H2 22.4 L
D. 若将电池两极所通气体互换,X、Y两极材料也互换, 实验方案更合理。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同分异构体和同系物是两个不同的概念,观察下面列出的几种物质的分子式或结构简式,回答下列问题。
①CO(NH2)2 ②NH4CNO ③CH3CH2CH3 ④CH3CH2CH2CH3 ⑤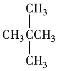 ⑥
⑥![]() ⑦
⑦![]() ⑧
⑧![]()
(1)互为同分异构体的是_________;
(2)互为同系物的是___________;
(3)实际上是同种物质的是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用铁质容器盛装冷的浓硫酸。为研究铁质材料与浓硫酸的反应,某学习小组进行了以下探究活动:
[探究一]
(1)甲同学将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是________________。
(2)甲同学另称取铁钉10.0 g放入25.0 mL浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。甲同学认为X中可能含有Fe3+也可能含有Fe2+。若要确认此结论,应用_________选填序号)。
a. KSCN溶液 b. 铁粉和KSCN溶液 c. 氨水 d. 酸性KMnO4溶液
(3)乙同学取448 mL(标准状况)气体Y通入足量溴水中,溴水褪色,发生反应的离子方程式为:______,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33 g。由此推知气体Y中SO2的体积分数为_____。
[探究二]
分析乙同学实验中SO2体积分数的结果,丙同学认为气体Y中除水蒸气外还可能含有Z和W气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
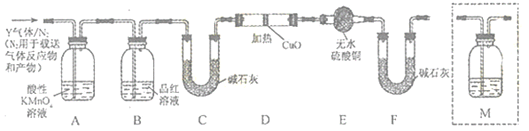
(4)装置B中试剂的作用是____________。
(5)丙同学认为用上图中的D、E、F装置可证明气体Y中还含有Z,则Z气体为_______(化学式),证明Z气体的实验现象为__________;F装置的作用是_________
(6)认为气体Y中还含有W的理由是__________(用化学方程式表示)。为确认W的存在,需在装置中添加M于_______(选填序号)。
a. A之前 b. A-B间 c. B-C间 d. C-D间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种香豆素的衍生物结构如图所示,关于该有机物说法正确的是( )
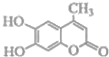
A.该有机物分子式为 C10H10O4
B.1mol该有机物与 H2发生加成时最多消耗H2 5 mol
C.1mol该有机物与足量溴水反应时最多消耗Br23 mol
D.1mol该有机物与 NaOH 溶液反应是最多消耗NaOH 3 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气质量评价的主要污染物为PM10、PM2.5、SO2、NO2、O3和CO等物质.其中,NO2与SO2都是形成酸雨的主要物质.在一定条件下,两者能发生反应:NO2(g)+SO2(g)SO3(g)+NO(g)
完成下列填空:
(1)在一定条件下,将等物质的量的NO2、SO2气体置于体积固定的密闭容器中发生反应,下列能说明反应已经达到平衡状态的是______.
a.v(NO2)生成=v(SO2)消耗 b.混合物中氧原子个数不再改变
c.容器内气体颜色不再改变 d.容器内气体平均相对分子质量不再改变
(2)当空气中同时存在NO2与SO2时,SO2会更快地转变成H2SO4,其原因是______.
(3)科学家正在研究利用催化技术将NO2和CO转变成无害的CO2和N2,反应的化学方程式:2NO2(g)+4CO(g)![]() 4CO2(g)+N2(g)+Q(Q>0),若在密闭容器中充入NO2和CO,下列措施能提高NO2转化率的是______.
4CO2(g)+N2(g)+Q(Q>0),若在密闭容器中充入NO2和CO,下列措施能提高NO2转化率的是______.
A.选用高效催化剂 B.充入NO2C.降低温度 D.加压
(4)请写出N原子最外层电子轨道表达式______,写出CO2的电子式______.
(5)关于S、N、O、C四种元素的叙述正确的是______.
A.气态氢化物均为极性分子 B.最高化合价均等于原子最外层电子数
C.单质一定为分子晶体 D.原子最外层均有两种不同形状的电子云
(6)写出一个能够比较S元素和C元素非金属性强弱的化学反应方程式:______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验室利用氢氧化钠、盐酸分离铁粉和铝粉混合物,物质转化关系如图所示:

下列说法不正确的是( )
A. x为NaOH溶液,y为盐酸
B. a→b发生的反应为:AlO2-+H++H2O═Al(OH)3↓
C. b→c→Al的反应条件分别为:加热、电解
D. a、b、c既能与酸又能与碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有4种碳骨架如下的烃,下列说法正确的是( )
a.![]() b.
b.![]() c.
c.![]() d.
d.![]()
①a和d是同分异构体 ②b和c是同系物
③a和d都能发生加聚反应 ④只有b和c能发生取代反应
A.①②B.①④C.②③D.①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com