
【题目】为有效控制雾霾,各地积极采取措施改善大气质量,研究并有效控制空气中的氮氧化物、碳氧化物含量显得尤为重要。
Ⅰ.氮氧化物研究
(1)一定条件下,将2molNO与2molO2置于恒容密闭容器中发生反应2NO(g)+O2(g)![]() 2NO2(g),下列各项能说明反应达到平衡状态的是____________。
2NO2(g),下列各项能说明反应达到平衡状态的是____________。
a.体系压强保持不变 b.混合气体密度保持不变
c.NO和O2的物质的量之比保持不变 d.每消耗2molNO同时生成2 molNO2
(2)汽车内燃机工作时会引起N2和O2的反应:N2+ O2![]() 2NO,是导致汽车尾气中含有NO的原因之一。在T1、T2温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如右图所示,根据图像判断反应N2(g)+ O2(g)
2NO,是导致汽车尾气中含有NO的原因之一。在T1、T2温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如右图所示,根据图像判断反应N2(g)+ O2(g)![]() 2NO(g)的△H____0(填“>”或“<”)。
2NO(g)的△H____0(填“>”或“<”)。

(3)NOx是汽车尾气中的主要污染物之一。汽车发动机工作时会引发N2和O2反应,
其能量变化如图所示:
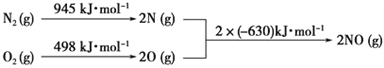
写出该反应的热化学方程式:________________________________。
Ⅱ.二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物。综合治理其污染是坏境化学当前的重要研究内容之一。
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(s)+O2(g)![]() 2SO3(g),某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如下图所示。根据图示回答下列问题:
2SO3(g),某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如下图所示。根据图示回答下列问题:
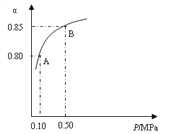
①将2.0 molSO2和1.0molO2置于10 L密闭容器中,反应达平衡后,体系总压强为0.10MPa。该反应的平衡常数等于__________。
②平衡状态由A变到B时,平衡常数K(A)_______K(B)(填“>”、“<”或“=”)。
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移的电子总数为__________(阿伏加德罗常数的值用NA表示),放出的热量为___________kJ。
【答案】 ac △H>0 N2(g)+O2(g)=2NO(g) △H=+183.kJ·mol-1 800L·mol-1 = 1.60NA(或1.6NA) 173.4
【解析】Ⅰ.(1)一定条件下,将2molNO与2molO2置于恒容密闭容器中发生反应2NO(g)+O2(g)![]() 2NO2(g)。a.正反应是气体分子数减少的方向,所以体系压强保持不变时,达到平衡; b.混合气体密度始终不变,所以密度不变不能说明达到平衡;c.NO和O2的物质的量之比保持不变,达到平衡;d.每消耗2molNO同时生成2 molNO2,不能说明正反应速率等于逆反应速率,不一定达到平衡。能说明反应达到平衡状态的是ac。
2NO2(g)。a.正反应是气体分子数减少的方向,所以体系压强保持不变时,达到平衡; b.混合气体密度始终不变,所以密度不变不能说明达到平衡;c.NO和O2的物质的量之比保持不变,达到平衡;d.每消耗2molNO同时生成2 molNO2,不能说明正反应速率等于逆反应速率,不一定达到平衡。能说明反应达到平衡状态的是ac。
(2)由图可知,T2先达到平衡,所以T1<T2。由T1升高到T2,氮气的体积分数减小了,说明升高温度后,该化学平衡向正反应方向移动,则可判断反应N2(g)+ O2(g)![]() 2NO(g)为吸热反应,△H>0。
2NO(g)为吸热反应,△H>0。
(3) 由图可知,该反应的△H=945kJ/mol+498kJ/mol-2![]() 630kJ/mol=183kJ/mol,所以该反应的热化学方程式为N2(g)+O2(g)=2NO(g) △H=+183.kJ·mol-1。
630kJ/mol=183kJ/mol,所以该反应的热化学方程式为N2(g)+O2(g)=2NO(g) △H=+183.kJ·mol-1。
Ⅱ.(1)①将2.0 molSO2和1.0molO2置于10 L密闭容器中,反应达平衡后,体系总压强为0.10MPa。由图可知,SO2的平衡转化率为0.80,则SO2、O2、SO3的变化量为1.6mol、0.80mol、1.6mol,SO2、O2、SO3的平衡量为0.40mol、0.20mol、1.6mol,SO2、O2、SO3的平衡浓度为0.040mol/L、0.020mol/L、0.16mol/L,该反应的平衡常数等于![]() 800L·mol-1。
800L·mol-1。
②平衡状态由A变到B时,平衡常数K(A)=K(B)。
(2)由CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ·mol-1和CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1可得,2CH4(g)+4NO2(g)= 2N2(g)+2CO2(g)+4H2O(g)△H=-1734kJ·mol-1,所以2mol CH4完全反应后,转移电子16mol、放出热量1734kJ。因此,若用标准状况下4.48 L CH4(即0.2mol)还原NO2至N2,整个过程中转移的电子总数为1.60NA(或1.6NA),放出的热量为173.4kJ。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】为纪念日军侵华战争中死难的中国同胞,中国政府设立12月13日为国家公祭日。在侵华史上,日军曾使用芥子气(化学式C4H8Cl2S)屠杀中国军民,下列对芥子气的说法正确的是
A. 有机物 B. 碱 C. 盐 D. 单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究: 查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体生成.
(1)摩擦剂中氢氧化铝的定性检验 取适量牙膏样品,加水成分搅拌、过滤.
①往滤渣中加入过量NaOH溶液,过滤.氢氧化铝与NaOH溶液反应的离子方程式是
②往①所得滤液中先通入过量二氧化碳,再加入过量稀盐酸.观察到的现象是;
(2)牙膏样品中碳酸钙的定量测定 利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.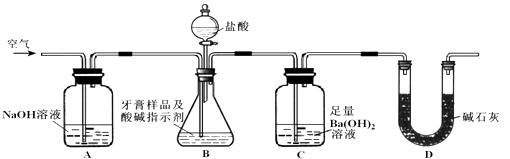
依据实验过程回答下列问题:
①实验过程中需持续缓缓通入空气.其作用除了可搅拌B、C中的反应物外,还有:
②C中反应生成BaCO3的离子方程式是
③下列各项措施中,不能提高测定准确度的是(填标号)
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A﹣B之间增添盛有浓硫酸的洗气装置
d.在B﹣C之间增添盛有饱和碳酸氢钠溶液的洗气装置
④实验中准确称取8.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g.则样品中碳酸钙的质量分数为(BaCO3的摩尔质量为197g/mol)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铍和铝的性质相似,下列关于铍的推断中,正确的是( )
A.铍与铝在周期表中处在同一主族
B.氢氧化铍可以溶于水
C.氧化铍既可以与强酸反应,又可以与强碱反应
D.氯化铍的化学式为BeCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 溴水中有下列平衡Br2+H2O![]() HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
B. 合成氨反应,为提高氨的产率,理论上应采取降低温度的措施
C. 反应CO(g)+NO2(g) ![]() CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深
CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深
D. 对于反应2HI(g) ![]() H2(g)+I2 (g),达平衡后,缩小容器体积可使体系颜色变深
H2(g)+I2 (g),达平衡后,缩小容器体积可使体系颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用FeSO4还原MnO4-,若还原5×10-3 mol MnO4-,消耗10 mL 2.5 mol·L-1 FeSO4溶液,则Mn元素在还原产物中的化合价是
A. +1 B. +2
C. +4 D. +5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种光化学电池的结构如图所示,电池总反应为:AgCl(s)+Cu+(aq)===Ag(s)+Cu2+(aq)+Cl-(aq),下列关于该电池在工作时的说法中正确的是
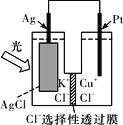
A. 生成108 g银,转移电子个数为1 mol
B. Cu+在负极发生氧化反应
C. Ag电极活泼,Ag失电子发生氧化反应
D. Cl-由负极迁移到正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带、海藻中丰富的碘元素主要以碘化钾的形式存在.化学小组欲用海带制取少量碘单质,先将海带烧成灰,再用水浸泡一段时间(让碘化物充分溶解),得到海带灰悬浊液,然后按以下流程提取单质碘(已知:2I﹣+Cl2=2Cl﹣+I2).
(1)过程 ①中使用的玻璃仪器;
(2)过程②中充入适量Cl2的目的是;
(3)提取碘的过程中实验操作③的名称: , 选择的有机试剂可以是(填序号);
A.酒精 B.四氯化碳 C.醋酸 D.苯
(4)过程③中有以下操作.
①倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,放正分液漏斗;
②把50mL碘水和15mL有机溶剂加入分液漏斗中,并盖好玻璃塞;
③将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
④把盛有溶液的分液漏斗放在铁架台的铁圈中,静置、分层;
⑤从分液漏斗上口倒出上层液体.
⑥旋开分液漏斗下面的活塞,用烧杯接收下层液体;
⑦检验分液漏斗活塞和上口的玻璃塞是否漏液;
操作顺序正确的是(填字母).
A.⑦①②③④⑤⑥
B.⑦②①④③⑥⑤
C.⑦①②④③⑥⑤
D.⑦②①③④⑥⑤
(5)过程 ④从含碘的有机溶液中提取碘并回收有机溶剂,还需要经过蒸馏、冷凝(如图).则冷水的流向为 . 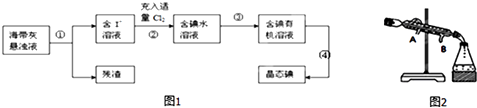
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com