
һ�������´��ڷ�Ӧ��CO(g)��H2O(g) CO2(g)��H2(g)��������Ӧ���ȡ�����������ͬ��2 L���ݾ���(�����û����������)�ܱ��������ڢ��г���1 mol CO��1 mol H2O���ڢ��г���1 mol CO2��1 mol H2���ڢ��г���2 mol CO��2 mol H2O��700 �������¿�ʼ��Ӧ���ﵽƽ��ʱ������˵����ȷ����( )
CO2(g)��H2(g)��������Ӧ���ȡ�����������ͬ��2 L���ݾ���(�����û����������)�ܱ��������ڢ��г���1 mol CO��1 mol H2O���ڢ��г���1 mol CO2��1 mol H2���ڢ��г���2 mol CO��2 mol H2O��700 �������¿�ʼ��Ӧ���ﵽƽ��ʱ������˵����ȷ����( )
A��������������Ӧ������ͬ
B����������CO��ת��������������CO2��ת����֮��С��1
C����������CO�����ʵ������������е���
D���������з�Ӧ��ƽ�ⳣ����ͬ
B
��������
���������A�����������Ǵ�����Ӧ���淴Ӧ�����෴�ķ���ʼ���еġ��÷�Ӧ������ӦΪ���ȷ�Ӧ����Ӧ�ں��ݾ����ܱ��������Է�Ӧ���У����Դﵽƽ��ʱ������Ӧ���ʲ�����ͬ������B������Ӧ������ͬ���¶��½��У�����������CO��ת��������������CO2��ת����֮�͵���1���������ڷ�Ӧ���ں��ݾ����ܱ��������Է�Ӧ���У�����ת���ʵĺͱ�С��1.��ȷ��C���������з�Ӧ������Ӧ����ʼ�����ŷ�Ӧ�Ľ��У��¶����ߡ������¶ȣ���ѧƽ�������ƶ��������������Ǵ��淴Ӧ����ʼ�����ŷ�Ӧ�Ľ��У��������¶Ȼή�͡������¶ȣ���ѧƽ������ȷ�Ӧ�����ƶ���CO�����ʵ������������Զ��ﵽƽ��ʱ��������CO�����ʵ������������еĴ���D���������и����ʵ����ʵ���Ũ����������Ũ�Ȼ�ѧƽ�������ƶ����������¶����ߡ������¶ȣ���ѧƽ�������ȷ�Ӧ�����ƶ��������������з�Ӧ��ƽ�ⳣ������ͬ������
���㣺������Ũ�ȡ��¶ȶԿ��淴Ӧ�ĸ����ʵĻ�ѧƽ�ⳣ����Ũ��ת���ʵ�Ӱ���֪ʶ��


 Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015�찲��ʡ��У�����о��������һ��������ѧ�Ծ��������棩 ���ͣ��ƶ���
����������E�����������Ƹ���ԭ���Ը�Ѫѹ��ҩ��ϳ�·�����£�
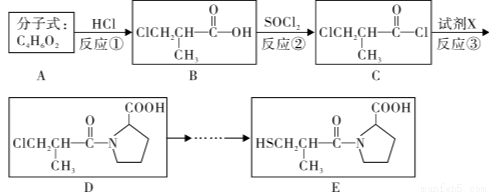
��1��A��ϵͳ���� ��B�й����ŵ������� ��B��C�ķ�Ӧ������ ��
��2��C��Dת������һ������HCl�����Լ�X�ķ���ʽ ��
��3��D��NaOH����Һ�з�����ȥ��Ӧ�����ữ��IJ���Y�ж���ͬ���칹�壬д��ͬʱ������������������Y��ͬ���칹��Ľṹ��ʽ �� ��
a�����������ʾ�����к��б��������������ĸ�ȡ�����Ҳ�����
b���˴Ź���������ʾ��������6�ֲ�ͬ��������ԭ��
c������FeCl3��Һ������ɫ��Ӧ
��4��B������������Һ�е�ˮ������ữ����Է����ۺϷ�Ӧ��д���÷�Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�찲��������ѧͬ����ʱ�����˽�ѡ��4��2.3��ѧƽ���ƶ��Ծ��������棩 ���ͣ�ѡ����
���ܱ������н��з�Ӧ��H2(g)+Br2(g) 2HBr(g)����H<0���ﵽƽ�����ʹ��ɫ���Ӧ��ȡ�Ĵ�ʩ��(����)
2HBr(g)����H<0���ﵽƽ�����ʹ��ɫ���Ӧ��ȡ�Ĵ�ʩ��(����)
A�������¶�B�������¶� C������H2Ũ��D����Сѹǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�찲��������ѧͬ����ʱ�����˽�ѡ��4��1.3��ѧ��Ӧ�ȵļ��㣨�����棩 ���ͣ�ѡ����
��֪�Ȼ�ѧ����ʽ��SO2(g)+O2(g)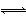 SO3(g)����H=-98��32 kJ��mol-1���������г���2 mol SO2��1 mol O2����ַ�Ӧ�����շų�������(����)
SO3(g)����H=-98��32 kJ��mol-1���������г���2 mol SO2��1 mol O2����ַ�Ӧ�����շų�������(����)
A��=196��64 kJB��=98��32 kJ C��<196��64 kJD��>196��64 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�찲��ʦ���и߶���ѧ�����п��黯ѧ�Ծ��������棩 ���ͣ������
ijУ��ѧ�о���ѧϰС��ѧϰ�˻�ѧ��Ӧ�����������ݺ�CaCO3��ϡ����ķ�Ӧ���������̽�������������������£���CaCO3��״�������1L��1mol?L-1ϡ�����У���¼�����淴Ӧʱ��ı仯����CO2��������ʵ�����������Ƴ���ͼ���ߡ�������Һ������仯���Բ��ƣ�������������⣺
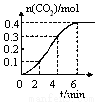
��1������ӿ�÷�Ӧ�����ʣ����Բ�ȡ�Ĵ�ʩ�� �� �������֣���
��2��0��2min�ڣ���HClŨ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ ���Ƚ�0��2min��2��4min��4��6min����ʱ��Σ���Ӧ���������� ��
��3�����ݶ��������ݣ����Ե�����0��6min�ڸ÷�Ӧ�Ļ�ѧ��Ӧ���ʵı仯��� ���������ֱ仯��ԭ���� ��
��4������ͼ�������ߵı仯���ƣ���8minʱ���÷�Ӧ�ķ�Ӧ����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�찲��ʦ���и߶���ѧ�����п��黯ѧ�Ծ��������棩 ���ͣ�ѡ����
һ���¶��£��ڹ̶��ݻ����ܱ������У����淴Ӧ��mA(g)��nB(g)  pC(g)��qD(g)����m��n��p��qΪ����������ʱ������״̬������ϵ��ѹǿ���ٷ����仯��������m mol A ͬʱ����q mol D���۸���ֵ����ʵ���Ũ�Ȳ��ٸı䣻����ϵ���ܶȲ��ٷ����仯���ݷ�Ӧ����v(A)��v(B)��v(C)��v(D)��m��n��p��q������ֵ������������ٸı䣻�߷�Ӧ������ƽ��Ħ���������ٷ����仯������һ����˵����Ӧ�Ѵﵽƽ��״̬����( )
pC(g)��qD(g)����m��n��p��qΪ����������ʱ������״̬������ϵ��ѹǿ���ٷ����仯��������m mol A ͬʱ����q mol D���۸���ֵ����ʵ���Ũ�Ȳ��ٸı䣻����ϵ���ܶȲ��ٷ����仯���ݷ�Ӧ����v(A)��v(B)��v(C)��v(D)��m��n��p��q������ֵ������������ٸı䣻�߷�Ӧ������ƽ��Ħ���������ٷ����仯������һ����˵����Ӧ�Ѵﵽƽ��״̬����( )
A���ڢۢܢ� B���ۢޢ� C���ڢۢ� D���ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�찲��ʦ���и߶���ѧ�����п��黯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й��Ȼ�ѧ����ʽ�����ۺ�������( )
| ʵ����ʵ | �Ȼ�ѧ����ʽ | ���� |
A | ��֪H+(aq)+OH-(aq)=H2O(l) ��H����57.3 kJ��mol-1����ϡ������ϡ����������Һ��� | H2SO4(aq)+Ba(OH)2(aq) =BaSO4(s)+ 2H2O(l) ��H����114.6 kJ��mol-1 | ��ȷ |
B | ������ϡ����������Һ��� | CH3COOH(aq)+NaOH(aq) =CH3COONa(aq)+H2O(l) ��H����57.3kJ��mol-1 | ����ȷ����Ϊ����״̬Ϊ��aq���������ǡ�l���� |
C | 160 g SO3����������ˮǡ����ȫ��Ӧ����H2SO4���ų�����260.6 kJ | SO3(g)+H2O(l)=H2SO4(aq) ��H����130.3 kJ��mol-1 | ����ȷ����Ϊ��Ӧ��Ϊ��H����260.6kJ��mol-1 |
D | ��֪25�桢101 kPa�£�120gʯī��ȫȼ�շų�����3935.1 kJ | C��s��+O2��g��=CO2��g�� ��H����393.51 kJ��mol-1 | ����ȷ��ͬ��������Ҫע���ƣ�C��ʯī�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���Ĵ�ʡ������ѧ���Ի�ѧ�Ծ��������棩 ���ͣ������
��ҵ��������Ȼ��(��Ҫ�ɷ���CH4)��H2O���и��������Ʊ��ϳ���(CO+H2)��CO��H2��һ�����������Ʊ���ȩ�����ѵȶ����л����֪CH4��H2��CO��ȼ����(��H)�ֱ�Ϊ��890.3 kJ��mol-1����285.8 kJ��mol-1�ͣ�283.0 kJ��mol-1��18.0 gˮ����Һ��ʱ�������仯Ϊ44.0 kJ��
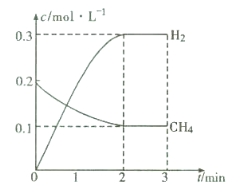
��1��д��������ˮ�����ڸ����·�Ӧ�ƺϳ������Ȼ�ѧ����ʽ ��
��2����һ�������£�������̶�Ϊ2 L���ܱ������г���0.40mol CH4(g)��0.60mol H2O(g)�����CH4(g)��H2(g)�����ʵ���Ũ����ʱ��仯��������ͼ��ʾ��3 minʱ�ı���������Ӧ���е�4 minʱ����ϵ�и����ʵ����ʵ������±���ʾ��
t��min | n(CH4)��mol | n(H2O)��mol | n(CO)��mol | n(H2)��mo1 |
4 | 0.18 | 0.38 | 0.22 | 0.66 |
��3��4min֮�䣬ƽ���� (��������桱)��Ӧ�����ƶ���3minʱ�ı�������� ��
��3����֪�¶ȡ�ѹǿ��̼ˮ��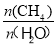 �Ը÷�Ӧ��Ӱ����ͼ��ʾ��
�Ը÷�Ӧ��Ӱ����ͼ��ʾ��
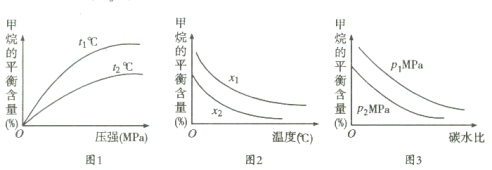
��ͼ1�У�����������ʾ�¶ȵĹ�ϵ:t1 t2(�>������<����=������ͬ)
��ͼ2�У�����������ʾ̼ˮ�ȵĹ�ϵ��x1 x2
��ͼ3�У�����������ʾѹǿ�Ĺ�ϵ��p1 p2
��4������Ȼ��(�������ʲ����뷴Ӧ)Ϊԭ�ϵ�ȼ�ϵ��ʾ��ͼ��ͼ��ʾ��
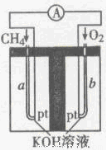
�ٷŵ�ʱ�������ĵ缫��ӦʽΪ
�ڼ���װ����ʢװ100.0 mL 3.0mol��L-1KOH��Һ���ŵ�ʱ���뷴Ӧ�������ڱ�״�������Ϊ8 960 mL���ŵ���Ϻ������Һ�и�����Ũ�ȵĴ�С��ϵΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���Ĵ�ʡ�ɶ���2012������Ի�ѧ�Ծ��������棩 ���ͣ������
(12��)ij��ҵ��ˮ����һ������Cr2O72����CrO42������
ȡ���ù�ҵ��ˮ��������и��ĺ�����
����I��ȡ25. 00 mL��ˮ�������ʺ�ϡ�����ữ��
�����������ĵ⻯����Һ�����˼���ָʾ����
����� ��o .1000 mol��L-1Na2S2O3��Һ�ζ�(I2+2Na2 S2O3= 2NaI+Na2S4O6)
�ﵽ�յ�ʱ������Һ24. 00 mL��
���������������Ӧ�����Һ�������´�������Ӧ���Һ
�ش���������
��1������I����ϡ�����ữ��Ŀ���� ��
��2��������з������·�Ӧ�������Ʋ���ƽ���ӷ���ʽ

�ò���������ָʾ���� ��
��3��������жϵζ��ﵽ�յ��������__ __��
��4������������������е�������____ ���δ�һ������
��5�����㹤ҵ��ˮ�и�Ԫ�صĺ����� mg/L.
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com