
【题目】下列关于化学与生产、生活的认识正确的是
A.禁止使用化学合成的化肥与农药,促进绿色食品和有机食品的生产
B.用Ba(OH)2处理含Cu2+的废水,可消除水中重金属离子的污染
C.煤经过气化和液化等物理变化可转化为清洁燃料
D.![]() 和CO2生成可降解聚合物
和CO2生成可降解聚合物 ![]() ,反应符合绿色化学的原则
,反应符合绿色化学的原则
科目:高中化学 来源: 题型:
【题目】2019年9月12日11时26分,我国在太原卫星发射中心用长征四号乙运载火箭,成功将资源一号02D卫星发射升空。资源一号02D卫星将为国家自然资源资产管理和生态监理工作提供稳定的数据保障,同时兼顾防灾减灾、环境保护、城乡建设、交通运输、应急管理等相关领域应用需求。
(1)卫星改变运行的路线时需要喷火消耗燃料,其燃料一般是肼(N2H4)。肼中N的化合价是___,肼在空气中燃烧的化学方程式如下,请用双线桥法标出该反应中电子转移的方向和数目___。
N2H4+O2![]() N2+2H2O
N2+2H2O
该反应中的氧化剂是___,被氧化的元素是___,每生成1molH2O转移电子___mol。
(2)近几年来,太原市在环境保护方面采取了一系列措施,其中的喷雾车、洒水车都是为了降低空气中的粉尘。含有粉尘的空气是否属于胶体___(填“是”或“否”),证明的方法是___,观察到的现象是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用CaSO4代替O2与燃料CO反应,既可以提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
①1/4CaSO4(s)+CO(g) ![]() 1/4CaS(s)+CO2(g) △H1=-47.3kJ/mol
1/4CaS(s)+CO2(g) △H1=-47.3kJ/mol
②CaSO4(s)+CO(g) ![]() CaO(s)+ CO2(g)+ SO2(g) △H2=+210.5kJ/mol
CaO(s)+ CO2(g)+ SO2(g) △H2=+210.5kJ/mol
③CO(g)![]() 1/2C(s)+1/2CO2(g) △H3=-86.2kJ/mol
1/2C(s)+1/2CO2(g) △H3=-86.2kJ/mol
(1)反应2 CaSO4(s)+7CO(g) ![]() CaS(s)+CaO(s)+C(s)+6CO2(g)+SO2(g)的△H=_______________(用△H1、△H2和△H3表示)。
CaS(s)+CaO(s)+C(s)+6CO2(g)+SO2(g)的△H=_______________(用△H1、△H2和△H3表示)。
(2)为减少副产物,获得更纯净的CO2,可在初始燃料中适量加入__________________。
(3)以反应①中生成的CaS为原料,在一定条件下经原子利用率100%的高温反应,可再生成CaSO4,该反应的化学方程式为___________;在一定条件下CO2可与对二甲苯反应,在其苯环上引入一个羧基,产物的结构简式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有11.2 g KOH的稀溶液与1 L 0.1 molL﹣1的H2SO4溶液反应,放出11.46 kJ的热量,下列热化学方程式正确的是
A. KOH(aq)+![]() H2SO4(aq) ===
H2SO4(aq) === ![]() K2SO4(aq)+H2O(l) ΔH =-11.46 kJmol﹣1
K2SO4(aq)+H2O(l) ΔH =-11.46 kJmol﹣1
B. 2KOH(aq)+H2SO4(aq) === K2SO4(aq)+2H2O(l) ΔH =-11.46 kJmol﹣1
C. 2KOH(aq)+H2SO4(aq) === K2SO4(aq)+2H2O(l) ΔH =+114.6 kJmol﹣1
D. KOH(aq)+![]() H2SO4(aq) ===
H2SO4(aq) === ![]() K2SO4(aq)+H2O(l) ΔH =-57.3 kJmol﹣1
K2SO4(aq)+H2O(l) ΔH =-57.3 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列各题:
(1)KOH的电子式:____________, CH(CH3)3的名称为:______________。
(2)有五种物质 :①Cu、②H2CO3、③BaSO4、④盐酸、⑤SO2,其中弱电解质是______(填序号,下同) ,非电解质是________________。
(3)钠与水反应的化学方程式为:_____________________。
已知在过量的FeSO4溶液中滴入几滴NaClO溶液,并加入过量H2SO4,溶液立即变黄,试写出该反应的离子方程式:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用Na2O2与H2O反应快速制取少量O2.用下面装置制取O2并演示Na在O2中的燃烧实验.
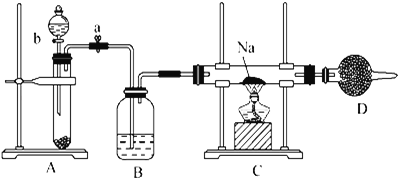
请回答下列问题:
(1)写出A装置中反应的化学方程式_____.
(2)B装置中盛放的试剂是_____.
(3)D装置中盛放的试剂是_____,其作用是_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】混合物分离和提纯常用下图装置进行,按要求回答下列问题:

(1)仪器①的名称__________。
(2)除去澄清石灰水中悬浮的CaCO3颗粒应选用_______(填字母,下同)。
(3)分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物应选用_______。
(4)用CCl4提取碘水中的碘单质应选用_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究和开发CO、CO2的应用及水体污染的治理是化学工作者研究的重要课题。
(1)水体常见污染物之一的氨氮主要指游离氨或铵盐,可以通入一定量的氯气,利用产生的HClO除去。已知: NH4++HClO=NH2Cl+H++H2O;ΔH=a kJ·mol-1
NH4++4HClO=NO3- +6H++4Cl-+H2O;ΔH=b kJ·mol-1。
2NH2Cl+HClO=N2+H2O+3H++3Cl-;ΔH=c kJ·mol-1
则2NH4++3HClO=N2+3H2O+5H++3Cl-;ΔH=_____ kJ·mol-1
(2)将CO2与金属钠组合设计成Na-CO2电池,很容易实现可逆的充、放电反应,该电池反应为4Na+3CO2![]() 2Na2CO3+C。放电时当电路中转移1mol电子时被还原的CO2的质量为_____;充电时,阳极的反应式为________
2Na2CO3+C。放电时当电路中转移1mol电子时被还原的CO2的质量为_____;充电时,阳极的反应式为________
(3)废水中重金属离子常用沉淀法除去,已知Ksp(NiS)=1.1×10-21,Ksp(CuS)=1.3×10-36,国家规定的排放标准:镍低于1.1×10-5 mol·L-1,铜低于7.8×10-5 mol·L-1。则需要控制溶液中S2-的浓度不低于_____________mol·L-1。
(4)NO易被O2氧化为NO2。其他条件不变时,NO的氧化率α(NO)与温度、压强的关系如图1所示(p1线在p2的上方)则p1__p2(填“>”、“<”或“=”);温度高于800℃时,α(NO)几乎为0的原因是____
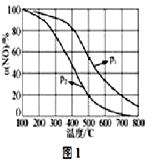
(5)环境中的有害物质常通过转化为CO2来降低污染,TiO2是一种性能优良的半导体光催化剂,能有效地将有机污染物转化为CO2等小分子物质。下图2为在TiO2的催化下,O3降解CH3CHO的示意图,则该反应的化学方程式为_____。
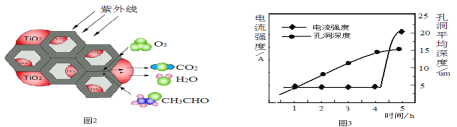
(6)用新型钛基纳米PbO2作电极可将苯、酚类等降解为CO2 和H2O。该电极可通过下面过程制备:将钛基板用丙酮浸泡后再用水冲洗,在钛板上镀上一层铝膜。用它做阳极在草酸溶液中电解,一段时间后,铝被氧化为氧化铝并同时形成孔洞。再用Pb(NO3)2溶液处理得纳米PbO2,除去多余的氧化铝,获得钛基纳米PbO2电极。电解时,电流强度和基板孔洞深度随时间变化如上图3所示,氧化的终点电流强度突然增加,其可能的原因是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值,下列说法正确的是
A. 在标准状况下,4.48L水中含有的分子数目为0.2NA
B. 0.1mol![]() 离子含有的电子、中子数均为1.0NA
离子含有的电子、中子数均为1.0NA
C. 一定条件下,0.1mol![]() 与0.3mol
与0.3mol![]() 充分反应后的0.1NA个分子
充分反应后的0.1NA个分子
D. 总物质的量为0.1mol的CaO和![]() 混合物中,所含离子总数为0.2NA
混合物中,所含离子总数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com