
【题目】将1mol纯净的氨基甲酸铵(NH2COONH4)置于特制的真空密闭容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其分解达到平衡:NH2COONH4 ![]() 2NH3(g)+CO2(g)(s-固态,g-气态)下列可以判断该反应己经达到化学平衡状态的是
2NH3(g)+CO2(g)(s-固态,g-气态)下列可以判断该反应己经达到化学平衡状态的是
A. 反应速率:v(正)=v(逆)=0 B. 有2molNH3生成
C. 气体的总体积保持不变 D. CO2的质量保持不变
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F、G七种元素,其中A、B、C、D、E、F为短周期元素且原子序数依次增大;A的最高正价与最低负价的代数和为零;B的最高价氧化物与C的氢化物在水中反应得到的生成物X既可与酸反应又可与碱反应;标准状况下,D2气体的密度约是1.43 g/L;E原子半径在同周期中除稀有气体外最大,F原子M层上的电子比K层多5个。金属G的合金在生活中用量最大,用途最广。
(1)画出元素F形成的简单离子结构示意图_______;
(2)若X为正盐,则其中所含的化学键类型有_______________;若X为酸式盐,则它与足量E的最高价氧化物对应水化物的稀溶液反应的离子方程式为_________________;
(3)以下三种说法中,可以验证B和F原子得电子能力强弱的是______________(填写编号)
a.比较这两种元素的常见单质的沸点
b.二者形成的化合物中,F元素的原子显负价
c.比较这两种元素的气态氢化物的稳定性
(4)向A和F形成的化合物的水溶液中加入少量G单质,反应后,再向溶液申加入A与D形成的化合物,发现溶液颜色变黄,请用离子方程式解释溶液变黄的原因____________。
(5)元素A和C的常见单质都是重要的化工原料,可发生反应:C2(g)+ 3A2 (g)![]() 2CA3 (g),且己知反应物总能量高于生成物总能量。
2CA3 (g),且己知反应物总能量高于生成物总能量。
①用电子式表示C2的形成过程________________。
②己知常温下拆开1 molA-A键、1 molA-C键、1mol![]() 键分别需要吸收的能量为a kJ、b kJ、c kJ,则按上述反应生成1molCA3的过程中的能量变化为:_________(填“吸收”或“放出”) ______kJ。
键分别需要吸收的能量为a kJ、b kJ、c kJ,则按上述反应生成1molCA3的过程中的能量变化为:_________(填“吸收”或“放出”) ______kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于丙烯(CH3﹣CH=CH2)的说法正确的( )
A.丙烯分子有7个δ键,1个π键
B.丙烯分子中3个碳原子都是sp3杂化
C.丙烯分子存在非极性键
D.丙烯分子中3个碳原子在同一直线上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在15 mL0.10 mol·L-1NaOH 溶液中逐滴加入 0.20 mol·L-1 的氢氰酸(HCN,一元弱酸)溶液,溶液的pH和加入的氢氰酸溶液的体积关系曲线如下图所示,有关粒子浓度大小关系正确的是

A. 在 A、B 间任意一点:c(Na+)﹥c(CN-)﹥c(OH-)﹥c(H+)
B. 在 B 点:c(Na+) = c(CN-)﹥c( OH-) = c(H+),且 a=7.5
C. 在 C 点:c(CN-)﹥c(Na+)﹥c(OH-)﹥c(H+)
D. 在 D 点:c(HCN) + c(CN-)﹥2c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.汽油、柴油和植物油都是碳氢化合物
B.乙醇可以被氧化为乙酸,二者都能发生酯化反应
C.甲烷、乙烯和苯在工业上都可通过石油分馏得到
D.含5个碳原子的有机物,每个分子中最多可形成4个C-C单键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温条件下,Al和Fe3O4反应生成Fe和Al2O3。下列说法正确的是

A. 该反应过程中的能量变化如图所示
B. 该反应条件下,Al的还原性弱于Fe
C. 1molFe3O4参与反应转移8×6.02×1023个电子
D. 实验室进行该反应时常加入KClO3作催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.欲提高氯水中HClO的浓度可往氯水加适量的碳酸钙粉末
B.形成酸雨的氧化物主要是SO2和氮的氧化物,CO2是造成温室效应的主要气体
C.水晶项链和餐桌上的瓷盘都是硅酸盐制品
D.大气中的N2可转化为NO,NO可转化为NO2、硝酸等;含硫物质在自然界中可转化为SO2等含硫化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中加入4molA、1.2molC和一定量的B三种气体,一定条件下发生反应,各物质的浓度随时间变化如甲图所示[已知t0~t1阶段保持恒温、恒容,且c(B)未画出]。乙图为t2时刻后改变反应条件,反应速率随时间的变化情况,已知在t2、t3、t4、t5时刻各改变一种不同的条件,其中t3时刻为使用催化剂。
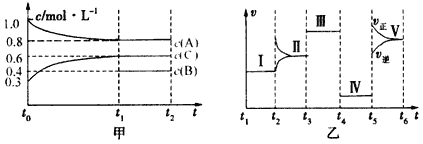
(1)若t1=15s,则t0~t1阶段的反应速率为v(C)= 。
(2)t4时刻改变的条件为 。
(3)已知t0~t1阶段该反应放出或吸收的热量为Q kJ(Q 为正值),试写出该反应的热化学方程式:__________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com