


科目:高中化学 来源: 题型:
3- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
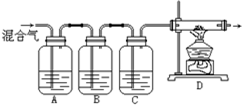 某学生设计一套实验装置如图所示,通过实验除去混在氮气中的氧气、二氧化碳、硫化氢和乙烯等气体,制得干燥的氮气.
某学生设计一套实验装置如图所示,通过实验除去混在氮气中的氧气、二氧化碳、硫化氢和乙烯等气体,制得干燥的氮气.| A | B | C | D | |
| 应加试剂 | ||||
| 所除杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
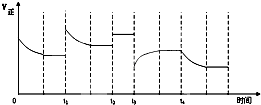 合成氨反应:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1,在反应过程中,正反应速率的变化如如图,下列说法正确的是( )
合成氨反应:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1,在反应过程中,正反应速率的变化如如图,下列说法正确的是( )| A、t1时增大了压强 |
| B、t2时同倍数增加N2、H2的物质的量 |
| C、t3时降低了温度 |
| D、t4时增大了c(NH3) |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醇、乙醛和乙酸都可以与钠反应生成氢气 |
| B、蛋白质水解的最终产物是葡萄糖 |
| C、苯和乙烯都可以使溴的四氯化碳溶液反应褪色 |
| D、可用碘检验淀粉是否水解完全 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①⑤ | B、②③④⑥⑦ |
| C、①②③④ | D、全部 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com