
(14分)A、B、C、D、E五种短周期元素,原子序数依次增大,B与C能层数相同,D与E能层数相同,C与D价电子结构相同,基态时B、C、D原子核外皆有2个未成对电子,A、E只有1个未成对电子,A能分别与B、C、D、E形成不同的分子。
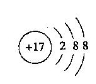
(1)写出基态时B的价电子排布图 ,E—的原子结构示意图 。
(2)写出BCD的电子式 ,E2C的结构式 。
(3)根据题目要求完成以下填空:
EC3—中心原子杂化方式 ;DC3中心原子杂化方式 ;
EC4—微粒中的键角 ;BC32—微粒的键角 ;
DE2分子的立体构型 ;B2A2分子的立体构型 。
(4)一种由A、B、C三种元素组成的分子A2BC2,该分子中σ键数目为 ,π键数目为 。
(5)根据等电子原理,指出与BC2互为等电子体的离子 (一种即可)
(14分)
(1) 2s 2p
| ↑↓ |
| ↑ | ↑ |
|
(2)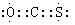 Cl—O—Cl
Cl—O—Cl
(3) sp3 sp2109°28ˊ 120° V形 直线形
(4) 4 1
(5)N3- 、AlO2-、 SCN-、CNO- 等 任意一种(2分)
【解析】
试题分析:A只有1个未成对电子,且A的原子序数在五种元素中最小,B、C是同周期元素,则A是H元素,B、C是第二周期元素,D、E是第三周期元素,E也只有1个未成对电子,结合E的原子序数和周期,判断E是Cl元素;C、D的价电子层结构相同,则C、D是同主族元素,基态时B、C、D原子核外皆有2个未成对电子,B的原子序数小于C,则B的2p能级有2个电子,C的2p能级有4个电子,所以B是C元素,C是O元素,则D是S元素。
(1)根据以上分析B是C元素,价电子排布图为
| ↑↓ |
| ↑ | ↑ |
|
2s 2p
E是Cl元素,Cl-的结构示意图为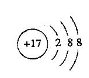
(2)BCD的化学式为COS,根据元素的价键原则,C与O、S分别形成双键,电子式为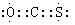 ;E2C的化学式为Cl2O,所以O分别与Cl原子形成一个共价键,结构式为Cl—O—Cl
;E2C的化学式为Cl2O,所以O分别与Cl原子形成一个共价键,结构式为Cl—O—Cl
(3)根据VSEPR理论,ClO3-的中心原子的价层电子对数=3+1/2(7+1-6)=4,所以中心原子杂化方式是sp3杂化;同理可计算SO3中心原子杂化方式是sp2杂化;ClO4—微粒中的中心原子的杂化方式是sp3杂化,无孤对电子,所以空间构型是正四面体型,键角是109°28ˊ;CO32—微粒的中心原子的杂化方式是sp2杂化,无孤对电子,所以空间构型是平面正三角形,键角是120°;SCl2分子中中心原子的杂化方式是sp3杂化,有2对孤对电子,所以立体构型是V型;C2H2分子中中心原子的杂化方式是sp杂化,立体构型是直线型;
(4)一种由A、B、C三种元素组成的分子A2BC2,化学式为CH2O2,该物质是甲酸,分子中含有4个σ键,1个π键;
(5)与CO2是等电子体的物质的化学式中也是三原子分子,价电子数是16,若为离子则是N3-、AlO2-、 SCN-、CNO- 等。
考点:考查元素的推断,电子排布图、结构示意图的书写,VSEPR理论的应用,键角、杂化方式、空间构型的判断,化学键的判断,等电子体的判断


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年四川省邛崃市高二上学期半期考试化学试卷(解析版) 题型:选择题
下列说法全部正确的是
①CH3—CH=CH2和CH2=CH2的最简式相同; ② CH≡CH和C6H6含碳量相同; ③苯乙烯和丁烯为同系物; ④正戊烷、异戊烷、新戊烷的沸点逐渐变低; ⑤标准状况下,11.2L的戊烷所含的分子数为0.5 NA (NA为阿伏加德罗常数)
A.①②③ B.②③④ C.①②④ D.③④⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省成都外国语学校高二上学期期中化学试卷(解析版) 题型:填空题
下表列出了前20号元素中的某些元素性质的有关数据(每空2分,共14分).

试回答下列问题:
(1)以上10种元素的原子中,失去核外第一个电子所需能量最少的是 (填编号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是(写分子式) 。某元素R的原子半径为1. 02×10-10m,该元素在周期表中位于 ;若物质Na2R3是一种含有非极性共价键的离子化合物,请你写出该化合物的电子式 。
(3)元素⑤的某种单质具有平面层状结构,同一层 中的原子构成许许多多的正六边形,此单质与熔融的②单质相互作用,形成某种青铜色的物质(其中的元素②用“●”表示),原子分布如图所示,
该物质的化学式为 。
(4)水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
①下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是__ ___(请用相应的编号填写)
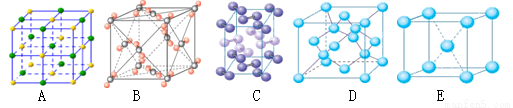
②将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。请写出生成此配合离子的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省成都外国语学校高二上学期期中化学试卷(解析版) 题型:选择题
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。下列对此现象说法正确的是
A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变
B.沉淀溶解后,将生成深蓝色的配合离子[Cu(H2O)4]2+
C.该实验能证明[Cu(NH3)4]2+比氢氧化铜稳定
D.在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省成都外国语学校高二上学期期中化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.乙烯中C=C键能是乙烷中C—C键能的2倍
B.氮气分子中含有1个σ键和2个π键
C.能够用来衡量化学键强弱的物理量有:键能、范德华力、氢键、晶格能
D.NH4+中4个N—H键的成键方式完全相同
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川成都树德协进中学高二10月阶段性考试化学试卷(解析版) 题型:选择题
BF3熔点和沸点都比较低,下列有关叙述不正确的是
A.BF3分子中键与键之间的夹角为120° B.BF3中心原子采用sp3杂化
C.BF3分子呈正三角形,中心原子无孤对电子 D.BF3分子立体结构与CO32-相同
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川成都树德协进中学高二10月阶段性考试化学试卷(解析版) 题型:选择题
基态原子的4s能级中只有1个电子的元素共有
A.1种 B.2种 C.3种 D.8种
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省长春市新高三起点调研考试化学试卷(解析版) 题型:填空题
(16分)Ⅰ、某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验,实验装置如图所示:
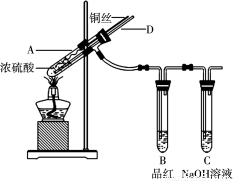
实验步骤:①先连接好装置,检验气密性,加入试剂;②加热A试管直到B中品红褪色,熄灭酒精灯;
③将Cu丝上提离开液面。
(1)装置A中发生反应的化学方程式为 。
(2)拆除装置前,不需打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操作是 。
(3)若将B中品红溶液换成溴水,通入一段时间后溴水褪色,这说明了二氧化硫具有漂白性,你是否同意这个观点 ,(填“同意”或“不同意”),说明理由 (用离子方程式表示)。
Ⅱ、以浓硫酸、浓硝酸、粗铜、水和空气为原料可制得硫酸铜晶体。其过程如下图所示。
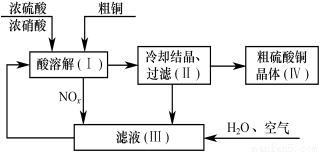
回答下列问题:
(4)配平在滤液(Ⅲ)中发生反应的化学方程式:
NOx+ H2O+ O2= HNO3
(5)写出制取硫酸铜的总反应方程式: 。
(6)在上述生产过程中,被循环使用的物质是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省长春外国语学校高一上学期期中化学试卷(解析版) 题型:填空题
阅读、分析下列两个材料:
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 溶解性 |
乙二醇 | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇 | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
根据上述材料,回答下列问题____(填写序号):
A、蒸馏法 B、萃取法
C、“溶解、结晶、过滤”的方法 D、分液法
(1)将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用_______。
(2)将乙二醇和丙三醇相互分离的最佳方法是__________。
(3)用CCl4提取溴水中的溴单质的最佳方法是_________.
(4)分离汽油和水的最佳方法是___________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com