
下列说法全部正确的是
①CH3—CH=CH2和CH2=CH2的最简式相同; ② CH≡CH和C6H6含碳量相同; ③苯乙烯和丁烯为同系物; ④正戊烷、异戊烷、新戊烷的沸点逐渐变低; ⑤标准状况下,11.2L的戊烷所含的分子数为0.5 NA (NA为阿伏加德罗常数)
A.①②③ B.②③④ C.①②④ D.③④⑤
科目:高中化学 来源:2014-2015学年天津市和平区高二上学期期中考试化学试卷(解析版) 题型:选择题
某化学反应其 ,则此反应在下列哪种情况下可自发进行
,则此反应在下列哪种情况下可自发进行
A.在任何温度下都能自发进行
B.在任何温度下都不能自发进行
C.仅在高温下自发进行
D.仅在低温下自发进行
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川邛崃市高二上学期第一次月考化学试卷(解析版) 题型:选择题
某主族元素的原子最外层电子排布是5S1,下列描述中正确的是
A.其单质常温下跟水反应不如钠剧烈
B.其原子半径比钾原子半径小
C.其碳酸盐易溶于水
D.其氢氧化物不能使氢氧化铝溶解
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川邛崃市高三上学期第一次月考化学试卷(解析版) 题型:选择题
已知Fe3O4可表示成(FeO?Fe2O3),水热法制备Fe3O4纳米颗粒的总反应为:
3Fe2++2S2O32-+O2+4OH—=Fe3O4+S4O62-+2H2O,下列说法不正确的是
A.参加反应的氧化剂与还原剂的物质的量之比为1:5
B.若有2molFe2+被氧化,则被Fe2+还原的O2为0.5mol
C.每生成1molFe3O4,则转移电子数为4mol
D.O2是氧化剂,S2O32-和Fe2+是还原剂
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省邛崃市高二上学期半期考试化学试卷(解析版) 题型:填空题
(11分)A、 X、Y、Z、R、W均为周期表中前四周期的元素,其中原子序数依次增大;A原子价电子排布式nsnnpn+1, X2-和Y+有相同的核外电子排布;Z的气态氢化物的沸点比其上一周期同族元素气态氢化物的沸点低;R的基态原子在前四周期元素的基态原子中单电子数最多;W为金属元素,X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实验室制取Z的气体单质。回答下列问题(相关回答均用元素符号表示):
(1)R基态原子的核外电子排布式是______________________。W在周期表中的位置是
(2)NH4Cl晶体中含有多种化学键,其中一定不含有的化学键是 (填字母)。
A.离子键 B.极性键 C.配位键 D.金属键
(3)A原子的第一电离能 (填“大于”、“小于”或“等于”)X原子的第一电离能;A元素的氢化物是一种易液化的气体,该气体易液化的原因是 。
(4)X与Y形成的化合物Y2X2的电子式 ,其晶体类型 。X与Y形成的化合物的晶胞如图所示,则该化合物的化学式为________(请用推断出的元素符号表示)。

(5)Z的某种含氧酸盐常用于实验室制取X形成的单质,此酸根离子的空间构型为___________ 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省邛崃市高二上学期半期考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.分子晶体中一定不含离子键,但一定存在共价键
B.金属与非金属元素形成的化合物一定是离子化合物
C.NCl3分子中所有的原子均为8电子稳定结构
D.NaHSO4晶体中阴、阳离子的个数比是1∶2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省邛崃市高二上学期半期考试化学试卷(解析版) 题型:选择题
有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是
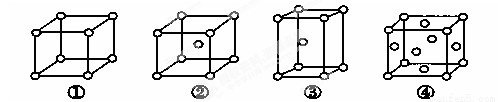
A.①为简单立方堆积②为六方最密堆积③为体心立方堆积④为面心立方最密堆积
B.每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个
C.晶胞中原子的配位数分别为:①6, ②8 ,③8, ④12
D.空间利用率的大小关系为:① < ② < ③ < ④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省高一10月月考化学试卷(解析版) 题型:选择题
下列各组中,、两种气体的分子数一定相等的是
A.温度相同,体积相同的O2 和 N2
B.温度相等,压强相等的N2和 C2H4
C.压强相同,质量相同的 O3和O2
D.体积相同,密度相等的CO 和N2和 C2H4
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川成都树德协进中学高二10月阶段性考试化学试卷(解析版) 题型:填空题
(14分)A、B、C、D、E五种短周期元素,原子序数依次增大,B与C能层数相同,D与E能层数相同,C与D价电子结构相同,基态时B、C、D原子核外皆有2个未成对电子,A、E只有1个未成对电子,A能分别与B、C、D、E形成不同的分子。
(1)写出基态时B的价电子排布图 ,E—的原子结构示意图 。
(2)写出BCD的电子式 ,E2C的结构式 。
(3)根据题目要求完成以下填空:
EC3—中心原子杂化方式 ;DC3中心原子杂化方式 ;
EC4—微粒中的键角 ;BC32—微粒的键角 ;
DE2分子的立体构型 ;B2A2分子的立体构型 。
(4)一种由A、B、C三种元素组成的分子A2BC2,该分子中σ键数目为 ,π键数目为 。
(5)根据等电子原理,指出与BC2互为等电子体的离子 (一种即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com