
【题目】1,2-二氯丙烷(CH2ClCHClCH3)是一种重要的化工原料,工业上可用丙烯加成法制备,主要副产物为3-氯丙烯(CH2=CHCH2Cl),反应原理为:
I.CH2=CHCH3(g)+Cl2(g)![]() CH2ClCHClCH3(g) H1=-134kJ·mol1
CH2ClCHClCH3(g) H1=-134kJ·mol1
II.CH2=CHCH3(g)+Cl2(g)![]() CH2=CHCH2Cl(g)+HCl(g) H2=-102kJ·mol1
CH2=CHCH2Cl(g)+HCl(g) H2=-102kJ·mol1
请回答下列问题:
(1)已知CH2=CHCH2Cl(g)+HCl(g)![]() CH2ClCHClCH3(g)的活化能Ea(正)为132kJ·mol1,则该反应的活化能Ea(逆)为___________kJ·mol1。
CH2ClCHClCH3(g)的活化能Ea(正)为132kJ·mol1,则该反应的活化能Ea(逆)为___________kJ·mol1。
(2)一定温度下,密闭容器中发生反应I和反应II,达到平衡后增大压强,CH2ClCHClCH3的产率____________(填“增大”“减小”或“不变”),理由是_____________________________。
(3)起始时向某恒容绝热容器中充入1mol CH2=CHCH3和1mol Cl2发生反应II,达到平衡时,容器内气体压强_________________(填“增大”“减小”或“不变”)。
(4)一定温度下,向恒容密闭容器中充入等物质的量的CH2=CHCH3(g)和Cl2(g)。在催化剂作用下发生反应I,容器内气体的压强随时间的变化如下表所示。
时间/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
压强/kPa | 80 | 74.2 | 69.4 | 65.2 | 61.6 | 57.6 | 57.6 |
①用单位时间内气体分压的变化来表示反应速率,即![]() ,则前120min内平均反应速率v(CH2ClCHClCH3)=__________kPa·min1。(保留小数点后2位)。
,则前120min内平均反应速率v(CH2ClCHClCH3)=__________kPa·min1。(保留小数点后2位)。
②该温度下,若平衡时HCl的体积分数为![]() ,则丙烯的平衡总转化率
,则丙烯的平衡总转化率____________;反应I的平衡常数Kp=____________________kPa1(Kp为以分压表示的平衡常数,保留小数点后2位)。
【答案】164 增大 反应I是一个气体物质的量减小的反应,达到平衡后增大压强,反应I正向移动,CH2ClCHClCH3的产率增大 增大 0.09 74% 0.21
【解析】
(1)已知:I.CH2=CHCH3(g)+Cl2(g)![]() CH2ClCHClCH3(g) H1=-134kJ·mol1
CH2ClCHClCH3(g) H1=-134kJ·mol1
II.CH2=CHCH3(g)+Cl2(g)![]() CH2=CHCH2Cl(g)+HCl(g) H2=-102kJ·mol1
CH2=CHCH2Cl(g)+HCl(g) H2=-102kJ·mol1
根据盖斯定律I–II得到CH2=CHCH2Cl(g)+HCl(g)![]() CH2ClCHClCH3(g) H=H1
CH2ClCHClCH3(g) H=H1![]() H2=-32kJ·mol1,且H=Ea(正)
H2=-32kJ·mol1,且H=Ea(正)![]() Ea(逆),则Ea(逆)=164kJ·mol1;
Ea(逆),则Ea(逆)=164kJ·mol1;
(2)恒温恒压密闭装置中,根据平衡移动原理,增大压强平衡向气体粒子数目减小的方向进行,该反应往正向移动,故CH2ClCHClCH3的产率增大;
(3)根据气体状态方程PV=nRT,V、n是定值,R是常数,压强随T增大而增大,由于容器是绝热恒容,与外界没有热量交换,对于反应II正反应放热,体系吸收热量,绝热容器的温度升高,故体系压强增大;
(4)①恒温恒容的密闭装置,初始通入等物质的反应物初始体系总压80 kPa,,120min总压为69.4 kPa,减小量为10.6 kPa,根据反应I方程分析CH2ClCHClCH3分压10.6 kPa,根据![]() ,v(CH2ClCHClCH3)=
,v(CH2ClCHClCH3)=![]() kPa·min1;
kPa·min1;
②设初始充入等物质的量的CH2=CHCH3和Cl2均为1mol,平衡时刻CH2ClCHClCH3为xmol,生成CH2=CHCH2Cl和HCl均为ymol,由于压强之比等于气体物质的量之比,有![]() ,得x=0.56mol,又有平衡时HCl的体积分数为
,得x=0.56mol,又有平衡时HCl的体积分数为![]() ,有
,有![]() =
=![]() ,得y=0.18mol,因此平衡时刻CH2=CHCH3和Cl2均为0.26mol,CH2ClCHClCH3为0.56mol,CH2=CHCH2Cl和HCl均为0.18mol,混合气体的总物质的量为1.44mol,故丙烯平衡总转化率
,得y=0.18mol,因此平衡时刻CH2=CHCH3和Cl2均为0.26mol,CH2ClCHClCH3为0.56mol,CH2=CHCH2Cl和HCl均为0.18mol,混合气体的总物质的量为1.44mol,故丙烯平衡总转化率![]()
![]() 100%=74%;反应I中CH2=CHCH3和Cl2物质的量分数均为
100%=74%;反应I中CH2=CHCH3和Cl2物质的量分数均为![]() ,且分压均为57.6×
,且分压均为57.6×![]() kPa,CH2ClCHClCH3物质的量分数
kPa,CH2ClCHClCH3物质的量分数![]() ,且分压为57.6×
,且分压为57.6×![]() kPa,则Kp=
kPa,则Kp=
![]() 0.21 kPa1。
0.21 kPa1。


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
【题目】取 1LFeCl3 溶液腐蚀铜板制作电路板,反应后在此残留液中慢慢加入铁粉,溶液中 Fe2+的浓度变化如图所示(加入固体引起的体积变化忽略不计),下列说法错误的是
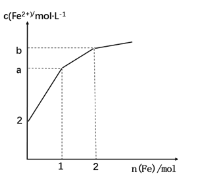
A.当n(Fe)=0.5mol 时,发生的离子反应为 Fe+2Fe3+=3Fe2+
B.当 n(Fe)=1.5mol 时,溶液中发生的总反应离子方程式为4Fe3++Cu2++3Fe=7Fe2++Cu
C.当n(Fe)=1mol 时,溶液中 c(Fe2+)=5 mol·L-1
D.腐蚀之前原溶液中n(Fe3+)=4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S为二元弱酸。20℃时,向0.100mol·L-1的Na2S溶液中缓慢通入HCl气体(忽略溶液体积的变化及H2S的挥发)。下列指定溶液中微粒的物质的量浓度关系一定正确的是( )
A.c(Cl-)=0.100mol·L-1的溶液中:c(OH-)-c(H+)=c(H2S)-2c(S2-)
B.通入HCl气体之前:c(S2-)>c(HS-)>c(OH-)>c(H+)
C.c(HS-)=c(S2-)的碱性溶液中:c(Cl-)+c(HS-)>0.100mol·L-1+c(H2S)
D.pH=7的溶液中:c(Cl-)=c(HS-)+2c(H2S)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于烃的说法正确的是

A. 该烃分子中共面的碳原子最多为14个
B. 该烃分子中共直线的碳原子只有为4个
C. 该烃存在顺反异构
D. 1mol 该烃与溴水反应时最多可以消耗6molBr2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表一部分,列出了九种元素在周期表中的位置:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ |
请用化学用语回答下列问题
(1)在上述元素中,金属性最强的是________。
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是________(填物质化学式)。写出⑥和⑧的最高价氧化物对应的水化物反应的离子方程式________。
(3)只由④形成的18电子微粒。________。
(4)写出②的最高价氧化物的电子式________。
(5)用电子式表示⑦和⑨形成的化合物的形成过程________。
<>(6)表中元素③和⑤可形成一种相对分子质量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构式________。查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验过程中产生的现象与图形相符合的是( )
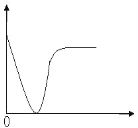
A. 稀硫酸滴加到 B a ( O H ) 2 溶液中(横坐标是稀硫酸的体积,纵坐标为溶液的导电能力)
B. 铁粉加到一定量 CuSO4 溶液中(横坐标是铁粉的质量,纵坐标为沉淀质量)
C. CO2 通入一定量 NaOH 溶液中(横坐标是 CO2 的体积,纵坐标为溶液的导电能力)
D. 稀盐酸滴加到一定量 NaOH 溶液中(横坐标是稀盐酸的体积,纵坐标为钠离子物质的量)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
I.CO2可以被NaOH溶液捕获,若所得溶液c(HCO3-)∶c(CO32-)=2∶1,溶液pH=_____。(室温下,H2CO3的K1=4×10-7;K2=5×10-11)
II.CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)
2CO(g)+2H2(g)
(1)已知上述反应中相关的化学键键能数据:
化学键 | C-H | C=O | H-H |
|
键能/kJ/mol | 413 | 745 | 436 | 1075 |
则该反应的ΔH=___________。分别在V L恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1 mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是___________(填“A”或“B”)。
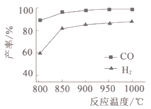
(2)按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图1所示。此反应优选温度为900℃的原因是____________。
(3)在T1温度时,将CH4和CO2各1.0 mol充入2 L密闭恒容容器中,充分反应达到平衡后,若CH4转化率为40%,则
①容器内的压强与起始压强之比为___________;
②此温度下,若该容器中含有CH4、CO2、H2、CO各1.0 mol,则此时反应所处的状态为___________(填“向正反应方向进行中”“向逆反应方向进行中”或“平衡状态”)
③欲使甲烷的平衡转化率提高,应采取的措施是___________(填标号)。
A.升高温度 B.降低温度 C.增大压强 D.减小压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种微生物燃料电池的结构示意图如下所示,关于该电池的叙述正确的是( )
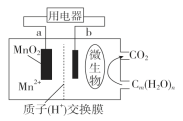
A. 电池工作时,电子由a流向b
B. 微生物所在电极区放电时发生还原反应
C. 放电过程中,H+从正极区移向负极区
D. 正极反应式为:MnO2+4H++2e-===Mn2++2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com