
����Ŀ��CO2��һ�����۵�̼��Դ�����ۺ����þ�����Ҫ���塣�ش��������⣺
I.CO2���Ա�NaOH��Һ������������Һc(HCO3-)��c(CO32-)=2��1����ҺpH=_____���������£�H2CO3��K1=4��10-7��K2=5��10-11��
II.CO2��CH4�����������Ƶúϳ�����CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)
2CO(g)+2H2(g)
(1)��֪������Ӧ����صĻ�ѧ���������ݣ�
��ѧ�� | C-H | C=O | H-H |
|
����/kJ/mol | 413 | 745 | 436 | 1075 |
��÷�Ӧ����H=___________���ֱ���V L�����ܱ�����A(����)��B(��ѹ���ݻ��ɱ�)�У�����CH4��CO2��1 mol�Ļ�����塣�������з�Ӧ��ƽ���ų������յ������϶����___________������A������B������
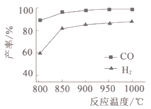
(2)��һ������ȼ���CH4��CO2���ں�ѹ�·�����Ӧ���¶ȶ�CO��H2���ʵ�Ӱ����ͼ1��ʾ���˷�Ӧ��ѡ�¶�Ϊ900���ԭ����____________��
(3)��T1�¶�ʱ����CH4��CO2��1.0 mol����2 L�ܱպ��������У���ַ�Ӧ�ﵽƽ�����CH4ת����Ϊ40%����
�������ڵ�ѹǿ����ʼѹǿ֮��Ϊ___________��
�ڴ��¶��£����������к���CH4��CO2��H2��CO��1.0 mol�����ʱ��Ӧ������״̬Ϊ___________������������Ӧ����������������淴Ӧ���������������ƽ��״̬����
����ʹ�����ƽ��ת������ߣ�Ӧ��ȡ�Ĵ�ʩ��___________(����)��
A.�����¶� B.�����¶� C.����ѹǿ D.��Сѹǿ
���𰸡�10 +120 kJ/mol B 900��ʱ���ϳ��������Ѿ��ϸߣ��������¶Ȳ������������ܺ����ߣ�����Ч�潵�� 1.4 ������Ӧ��������� A
��������
(I)����Na2CO3��Һ��������ˮ�ⳣ��Kh�����ƽ�ⳣ���Ĺ�ϵ���㣻
(II)(1)��Ӧ�ȵ��ڷ�Ӧ���ܻ�ѧ�����ܺ����������ܼ��ܺ͵IJ�÷�Ӧ������Ӧ�������������ķ�Ӧ���ȷ�Ӧ������ѹǿ��ƽ���ƶ���Ӱ�����ƽ���ƶ����жϷ�Ӧ���̵������仯��
(2)CH4��CO2�ں�ѹ�·�����Ӧ�������¶�������ƽ��ת���ʺͺϳɳɱ������жϣ�
(3)�ٸ������ʷ�Ӧת����ϵ����ƽ��ʱ����������ʵ��������������ݻ�����ʱ���������ʵ����ıȵ���ѹǿ�ȼ��㣻
���ȼ���T1�¶��µ�ƽ�ⳣ��K��Ȼ������ʱ�̵�Qc������K�Ƚϣ��жϷ�Ӧ���еķ���
�۸���ƽ���ƶ�ԭ�������жϡ�
(1)����Na2CO3��Һ��������ˮ�ⳣ��Kh= =
=![]() =2��10-4 mol/L������c(HCO3-)��c(CO32-)=2��1��������=
=2��10-4 mol/L������c(HCO3-)��c(CO32-)=2��1��������= �ɵ�2c(OH-)=2��10-4 mol/L����c(OH-)=1��10-4 mol/L��c(H+)=
�ɵ�2c(OH-)=2��10-4 mol/L����c(OH-)=1��10-4 mol/L��c(H+)=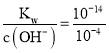 mol/L=10-10 mol/L������pH=10��
mol/L=10-10 mol/L������pH=10��
(II)(1)�÷�Ӧ�ķ�Ӧ�ȡ�H=(4��413+2��745)kJ/mol-(2��1075+2��436) kJ/mol=+120 kJ/mol��
�ɼ��÷�Ӧ������ӦΪ���������������ȷ�Ӧ��A�Ǻ��º�������½��еķ�Ӧ��B�Ǻ��º�ѹ�������ɱ䣬������B�У����ŷ�Ӧ�Ľ��У��������ݻ������൱������A��˵���൱�ڼ�Сѹǿ����ѧƽ�������ƶ�����������B���յ�����������A�ࣻ
(2)��Ӧ�ں�ѹ�½��У�����ͼʾ��֪����ѡ�¶�Ϊ900��������900��ʱ�ϳ����в�Ʒ�IJ����Ѿ��ϸߣ��������¶Ȳ������������ܺ����ߣ�����Ч�潵�ͣ����Ժ����¶�Ϊ900�棻
(3)����T1�¶�ʱ����CH4��CO2��1.0 mol����2 L�ܱպ��������У�������ӦCH4(g)+CO2(g)![]() 2CO(g)+2H2(g)������ƽ��ʱCH4ת����Ϊ40%����ƽ��ʱ����CO��H2�����ʵ�������2��0.4 mol=0.8 mol��ƽ��ʱn(CH4)=n(CO2)=(1.0-0.4) mol=0.6 mol��ƽ��ʱ����������ʵ���Ϊ0.6 mol+0.6 mol+0.8 mol+0.8 mol=2.8 mol����Ӧ��ʼʱ��������ʵ���Ϊ1.0 mol+1.0 mol=2.0 mol�����Ը���ѹǿ֮�ȵ������ʵ���֮�ȣ��������ڵ�ѹǿ����ʼѹǿ֮��Ϊ2.8 mol��2.0 mol=1.4��
2CO(g)+2H2(g)������ƽ��ʱCH4ת����Ϊ40%����ƽ��ʱ����CO��H2�����ʵ�������2��0.4 mol=0.8 mol��ƽ��ʱn(CH4)=n(CO2)=(1.0-0.4) mol=0.6 mol��ƽ��ʱ����������ʵ���Ϊ0.6 mol+0.6 mol+0.8 mol+0.8 mol=2.8 mol����Ӧ��ʼʱ��������ʵ���Ϊ1.0 mol+1.0 mol=2.0 mol�����Ը���ѹǿ֮�ȵ������ʵ���֮�ȣ��������ڵ�ѹǿ����ʼѹǿ֮��Ϊ2.8 mol��2.0 mol=1.4��
�ڸ��ݢټ����֪����ѧƽ�ⳣ���ǿ��淴Ӧ�ﵽƽ��״̬ʱ������������Ũ����֮������ַ�Ӧ��Ũ����֮���ıȣ��ڴ��¶��µĻ�ѧƽ�ⳣ��K=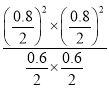 =
=![]() =0.284���ڴ��¶��µ�Qc=
=0.284���ڴ��¶��µ�Qc=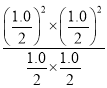 =0.25<K���ʷ�Ӧ������Ӧ������У�
=0.25<K���ʷ�Ӧ������Ӧ������У�
��CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)������Ӧ�����������������ȷ�Ӧ��
2CO(g)+2H2(g)������Ӧ�����������������ȷ�Ӧ��
A.�����¶ȣ���ѧƽ�������ȵ�����Ӧ�����ƶ���CH4��ת������ߣ�A�������⣻
B.�����¶ȣ���ѧƽ������ȵ��淴Ӧ�����ƶ���CH4��ת���ʽ��ͣ�B���������⣻
C.����ѹǿ����ѧƽ�������������С���淴Ӧ�����ƶ���CH4��ת���ʽ��ͣ�C���������⣻
D.��Сѹǿ����ѧƽ��������������������Ӧ�����ƶ���CH4��ת������ߣ�����Сѹǿ���»�ѧ��Ӧ���ʼ�С��ʹ����Ч�ʽ��ͣ�D���������⣻
�ʺ���ѡ����A��


 ������ϵ�д�
������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧʵ��С��ͬѧ��������װ���Ʊ���������̽������������(������������ȥ)����ش�

(1)ʵ�����Ʊ������Ļ�ѧ����ʽΪ__________��
(2)��װ��B�ռ�����ʱ��Ӧѡ�����Ľ�������_____(ѡ�a����b��)����˵��ѡ���������___________��
(3)��װ��B�е�ֹˮ��c�����۲쵽Բ����ƿ�ڲ����˺�ɫ��Ȫ����˵���������е�������_________��_________��
(4)Ϊ��ֹ��Ⱦ����������װ��(ʢ�ŵ�Һ���Ϊˮ)���������ն��ఱ������_____(�����)��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1��2-���ȱ���(CH2ClCHClCH3)��һ����Ҫ�Ļ���ԭ�ϣ���ҵ�Ͽ��ñ�ϩ�ӳɷ��Ʊ�����Ҫ������Ϊ3-�ȱ�ϩ(CH2=CHCH2Cl)����Ӧԭ��Ϊ��
I��CH2=CHCH3(g)+Cl2(g)![]() CH2ClCHClCH3(g) H1=-134kJ��mol1
CH2ClCHClCH3(g) H1=-134kJ��mol1
II��CH2=CHCH3(g)+Cl2(g)![]() CH2=CHCH2Cl(g)+HCl(g) H2=-102kJ��mol1
CH2=CHCH2Cl(g)+HCl(g) H2=-102kJ��mol1
��ش��������⣺
(1)��֪CH2=CHCH2Cl(g)+HCl(g)![]() CH2ClCHClCH3(g)�Ļ��Ea(��)Ϊ132kJ��mol1����÷�Ӧ�Ļ��Ea(��)Ϊ___________kJ��mol1��
CH2ClCHClCH3(g)�Ļ��Ea(��)Ϊ132kJ��mol1����÷�Ӧ�Ļ��Ea(��)Ϊ___________kJ��mol1��
(2)һ���¶��£��ܱ������з�����ӦI�ͷ�ӦII���ﵽƽ�������ѹǿ��CH2ClCHClCH3�IJ���____________���������С�����䡱����������_____________________________��
(3)��ʼʱ��ij���ݾ��������г���1mol CH2=CHCH3��1mol Cl2������ӦII���ﵽƽ��ʱ������������ѹǿ_________________���������С�����䡱����
(4)һ���¶��£�������ܱ������г�������ʵ�����CH2=CHCH3(g)��Cl2(g)���ڴ��������·�����ӦI�������������ѹǿ��ʱ��ı仯���±���ʾ��
ʱ��/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
ѹǿ/kPa | 80 | 74.2 | 69.4 | 65.2 | 61.6 | 57.6 | 57.6 |
���õ�λʱ���������ѹ�ı仯����ʾ��Ӧ���ʣ���![]() ����ǰ120min��ƽ����Ӧ����v(CH2ClCHClCH3)=__________kPa��min1��(����С�����2λ)��
����ǰ120min��ƽ����Ӧ����v(CH2ClCHClCH3)=__________kPa��min1��(����С�����2λ)��
�ڸ��¶��£���ƽ��ʱHCl���������Ϊ![]() �����ϩ��ƽ����ת����
�����ϩ��ƽ����ת����____________����ӦI��ƽ�ⳣ��Kp=____________________kPa1(KpΪ�Է�ѹ��ʾ��ƽ�ⳣ��������С�����2λ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±��ж����ӷ���ʽ�����ۺ�������
ѡ�� | ��ѧ��Ӧ�������ӷ���ʽ | ���� |
A | H2SO4��Һ��Ba(OH)2��Һ��Ӧ�� H++ SO42-+Ba2++OH | ��ȷ |
B | ��̼��þ��Һ�м�������ϡ��� CO32-+2H+ | ����̼��þ��Ӧд��������ʽ |
C | ���ˮ�еμӱ��͵��Ȼ�����Һ��Һ���Ϊ���ɫ��Fe3++3H2O | ��ȷ |
D | ��NaOH��Һ��ͨ������CO2��Ӧ��OH+CO2 | ��ȷ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���Ӧ���ڼӳɷ�Ӧ����
A. C3H8 + 5O2 ![]() 3CO2 + 4H2O
3CO2 + 4H2O
B. CH2 = CH2 + Br2 �� ![]()
C. 2CH3CH2OH + 2Na �� 2CH3CH2ONa + H2��
D. ![]() + HNO3
+ HNO3 ![]()
![]() + H2O
+ H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)����һ����Ҫ���л��������ṹ������������ء�
�������л�����������黥Ϊͬϵ�����______(����ĸ) ��
a.��ϩ b.���� c.��Ȳ
�������Լ������ڼ����������ϩ����______(����ĸ) ��
a.ˮ b.���Ȼ�̼ c.����KMnO4��Һ
�������л�������������ˮ����________��
a..�� b.���� c.�Ҵ�
(2) CH2=CH2��![]() ��CH3CH2OH��CH3COOCH2CH3��CH3COOH�������ǣ����У�
��CH3CH2OH��CH3COOCH2CH3��CH3COOH�������ǣ����У�
����ͨ����ѧ��Ӧʹ��ˮ��ɫ����____________��
���ܷ���ˮ�ⷴӦ����____________��
����������Cu(OH)2����Һ��Ӧ����ש��ɫ��������____________��
(3)�Ե���Ϊ��Ҫԭ�Ϻϳ�һ�־��й���ζ������C�ϳ�·����ͼ��ʾ��
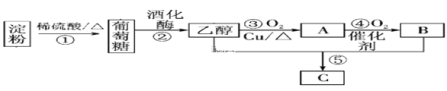
��ش��������⣺
��A�Ľṹ��ʽΪ____________��
��B�����еĹ���������Ϊ________��
�۷�Ӧ�ݷ���ʽ___________________________��
(4)��ϩ��ʯ�ͻ�������Ҫ����ԭ�ϣ���ҵ�Ͽ�����ϩ��ˮ��Ӧ���Ҵ����÷�Ӧ����Ϊ_______���仯ѧ����ʽΪ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ľ̿�ȿ���Ũ���ᷴӦ��Ҳ����Ũ���ᷴӦ����������Ӧ�Ĺ�ͬ����
A. ����������B. ľ̿������������
C. ������������̼D. ����ˮ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����ʵ�����Ʊ�����������װ�á�a�Թ��м���3mL95%���Ҵ���2mLŨ���ᡢ2mL�����b�Թ����DZ���̼������Һ�����Ӻ�װ�ã��þƾ��ƶ��Թ�a���ȣ����۲쵽�Թ�b������������ʱֹͣʵ�顣
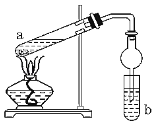
(1)��a�Թ��г��˼����Ҵ���Ũ����������⣬��Ӧ����__��Ŀ����__��
(2)�Թ�b�й۲쵽����Ҫ������__��
(3)ʵ�������θ���ܳ������������⣬��һ����Ҫ������__��
(4)����Na2CO3��Һ��������__��
(5)��Ӧ�������Թ����ռ����IJ�Ʒ�����Һ©���У�__��__��Ȼ���Һ���õ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����м������ʣ�
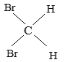
��16O2��18O3��35Cl��37Cl-�۽��ʯ��ʯī��12C��16C��1H2O��D2O��CH4��C7H16��C2H4��C3H6����ۺ���ά�آ�CH3CH2CH2CH3��![]() ��CH3CH(CH3)CH2CH2CH3��CH3CH2CH2(CH3)CHCH3
��CH3CH(CH3)CH2CH2CH3��CH3CH2CH2(CH3)CHCH3 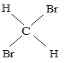 ��
��
![]() ��
��![]()
(1)��Ϊͬλ��___��
(2)��Ϊͬ��������___��
(3)��Ϊͬϵ��___��
(4)��Ϊͬ���칹��___��
(5)Ϊͬһ����___��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com